Содержание
- 2. Оборудование и реактивы Прибор для определения электропроводимости с лампочкой. Растворы кислот, щелочей, солей ( одинаковая нормальная
- 3. Теория электролитической диссоциации В Первой половине 19 века М. Фарадей ввел понятия об электролитах и неэлектролитах.
- 4. Электролиты- вещества, растворы которых проводят электрический ток. К ним относятся все растворимые: 1. соли 2.щелочи 3.кислоты
- 5. ФАРАДЕЙ Майкл 22 сентября 1791 г. – 25 августа 1867 г. Английский физик Майкл Фарадей родился
- 6. Для объяснения свойств водных растворов электролитов шведский ученый С. Аррениус (1859-1927) предложил теорию электролитической диссоциации. Согласно
- 7. Растворы веществ тогда становятся проводниками электрического тока, когда они содержат ионы (положительно или отрицательно заряженные частицы),
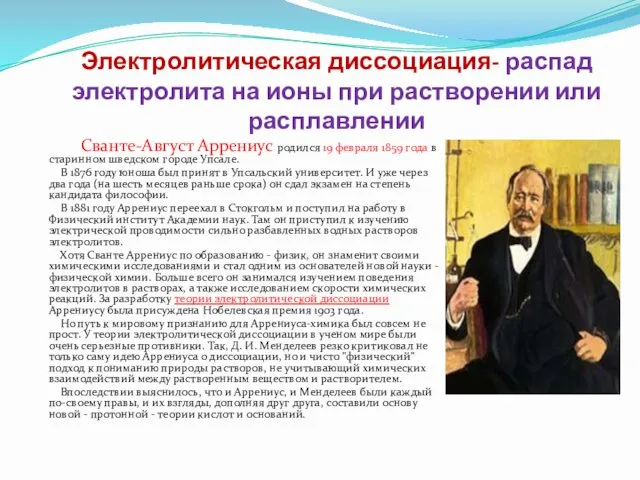
- 8. Электролитическая диссоциация- распад электролита на ионы при растворении или расплавлении Сванте-Август Аррениус родился 19 февраля 1859
- 9. Диссоциация- это распад электролита на ионы. Вывод (по Аррениусу): чтобы лампочка загорелась, цепь должна замкнуться через
- 10. Но эта теория не ответила на вопросы: почему одни вещества являются электролитами, а другие нет? Какова
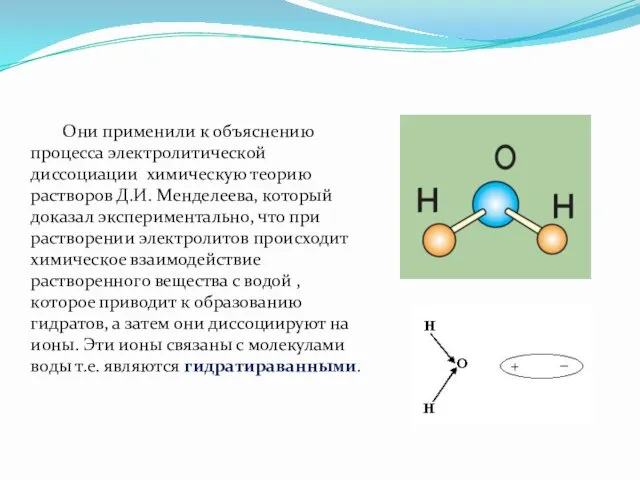
- 11. Они применили к объяснению процесса электролитической диссоциации химическую теорию растворов Д.И. Менделеева, который доказал экспериментально, что
- 12. МЕНДЕЛЕЕВ, Дмитрий Иванович 27 января (8 февраля) 1834 г. – 20 января (2 февраля) 1907 г.
- 13. КАБЛУКОВ, Иван Алексеевич 2 сентября 1857 г. – 5 мая 1942 г. Иван Алексеевич Каблуков –
- 14. Кистяковский Владимир Александрович Кистяковский Владимир Александрович [30.9(12.10).1865, Киев,—19.10.1952, Москва], советский физико-химик, академик АН СССР. Открыл зависимость
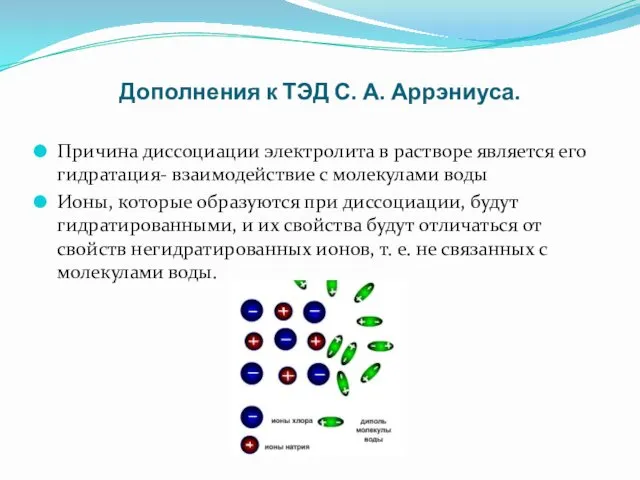
- 15. Дополнения к ТЭД С. А. Аррэниуса. Причина диссоциации электролита в растворе является его гидратация- взаимодействие с
- 16. Проникнуть в сущность процесса электролитической диссоциации помогло установление природы химической связи. Свойства негидратированных и гидратированных ионов
- 17. Гидратированные ионы в растворе находятся в постоянном хаотическом движении. Если в этот раствор поместить противоположно заряженные
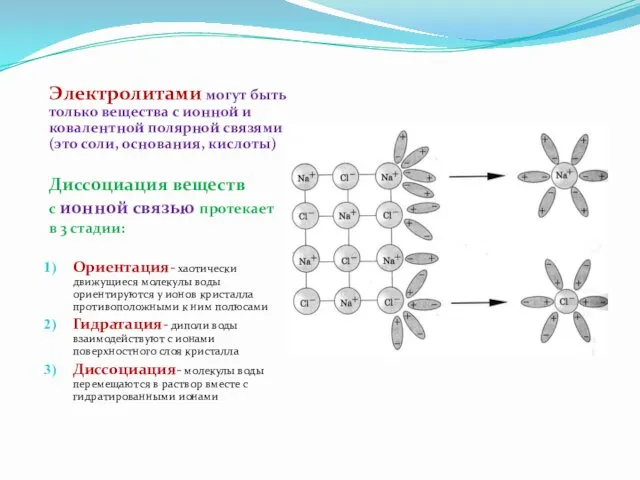
- 18. Электролитами могут быть только вещества с ионной и ковалентной полярной связями (это соли, основания, кислоты) Диссоциация
- 19. Диссоциация веществ с ковалентной полярной связью происходит несколько сложнее, например диссоциация хлороводорода в воде . 4
- 20. Современные представления Под электролитической диссоциацией понимают процесс распада электролитов на ионы под действием молекул воды, неводного
- 21. Закрепление материала Ионная связь Запишите уравнения диссоциации веществ: Хлорида меди(2); Нитрата натрия; Сульфата калия. Ковалентная связь
- 22. Сила электролитов Сильные и слабые электролиты Электролитическая диссоциация зависит от природы веществ-электролитов. Сильные электролиты- электролиты, которые
- 23. Слабые электролиты- электролиты, которые частично диссоциируют на ионы, т.к. в их растворах наряду с диссоциацией происходит
- 24. В растворах электролитов наряду с ионами присутствуют и молекулы. Поэтому растворы электролитов характеризуются степенью диссоциации (
- 25. Степень электролитической диссоциации зависит от концентрации электролита в растворе: Чем раствор концентрированнее, тем степень электролитической диссоциации
- 26. Степень электролитической диссоциации зависит от температуры раствора: Степень электролитической диссоциации растёт при нагревании: поскольку диссоциация- процесс
- 27. Вопросы к классу:
- 28. Материалы ЕГЭ Хлорид- ионы образуются при диссоциации в водном растворе вещества, имеющего формулу: 1)CL2 2)MgCL2 3)AgCL
- 29. В водном растворе ступенчато диссоциирует: 1)KOH 2)CuCL2 3)Ca(OH)2 4)Na2SO4 Ответ: 3 К электролитам относят все вещества
- 30. Электрический ток проводит: 1)Спиртовой раствор йода 2) Расплав парафина 3) Расплав ацетата натрия 4)Водный раствор глюкозы
- 31. Сильными электролитами являются все вещества группы: 1)KOH, HNO3, H2SO4 2)H2S, H2SO3, H2SO4 3)MgCL2, CH3COOH, NaOH 4)H2S,
- 32. Выводы Не все растворы проводят электрический ток, проводят только электролиты. Бывают сильные, средние и слабые электролиты.
- 34. Скачать презентацию










![Кистяковский Владимир Александрович Кистяковский Владимир Александрович [30.9(12.10).1865, Киев,—19.10.1952, Москва], советский](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/37029/slide-13.jpg)
















 Бронхиальная астма у детей
Бронхиальная астма у детей Человек и среда обитания. Природные опасности
Человек и среда обитания. Природные опасности Клинический случай Левамизолиндуцированная лейкоэнфефалопатия
Клинический случай Левамизолиндуцированная лейкоэнфефалопатия Атмосфера. Всероссийский конкурс
Атмосфера. Всероссийский конкурс Конструкционные материалы, применяемые при проектировании объектов топливно-энергетического комплекса
Конструкционные материалы, применяемые при проектировании объектов топливно-энергетического комплекса Удосконалення транспортно-експедиційного обслуговування населення у місті Луцьку
Удосконалення транспортно-експедиційного обслуговування населення у місті Луцьку Система технічного регулювання при виробництві та обігу драже
Система технічного регулювання при виробництві та обігу драже Кроссворд Профессии.
Кроссворд Профессии. Электронная игра Подбери по форме и цвету
Электронная игра Подбери по форме и цвету Как сделать эффективную презентацию?
Как сделать эффективную презентацию? Сто лет учительской династии
Сто лет учительской династии 23 февраля
23 февраля Аналіз мас-спектрів
Аналіз мас-спектрів Использование социальной сети ВКонтакте для совершенствования учебно-воспитательного процесса
Использование социальной сети ВКонтакте для совершенствования учебно-воспитательного процесса Geolika. Проект планировки территории планировочного района юго-восточной части г. Долинска
Geolika. Проект планировки территории планировочного района юго-восточной части г. Долинска Гуманизм: абстрактный или классовый, по роману А.А. Фадеева Разгром
Гуманизм: абстрактный или классовый, по роману А.А. Фадеева Разгром Техника описания различных легко-атлетических движений
Техника описания различных легко-атлетических движений Основные принципы ФГОС ДО
Основные принципы ФГОС ДО Получение азотной кислоты
Получение азотной кислоты Презентация Пасха
Презентация Пасха Стандарты информационной безопасности: Общие критерии
Стандарты информационной безопасности: Общие критерии Политический кризис Речи Посполитой
Политический кризис Речи Посполитой Родительское собрание 5 класс
Родительское собрание 5 класс Процесс постановки биотехнологической продукции на производство
Процесс постановки биотехнологической продукции на производство Размножение растений
Размножение растений Гайд по девушке для задрота
Гайд по девушке для задрота Симптомы и синдромы при заболеваниях печени
Симптомы и синдромы при заболеваниях печени Ощущения у детей с нарушением речи
Ощущения у детей с нарушением речи