Содержание
- 2. План лекции 1. Инструментальные методы анализа. Классификация методов. 2. Оптические методы анализа. Классификация оптических методов анализа.
- 3. КЛАССИФИКАЦИЯ ИНСТРУМЕНТАЛЬНЫХ МЕТОДОВ АНАЛИЗА Оптические методы Электрохимические методы Хроматографические методы Радиометрические методы Термические методы Масс-спектрометрические
- 4. КЛАССИФИКАЦИЯ ОПТИЧЕСКИХ МЕТОДОВ АНАЛИЗА По изучаемым объектам атомный и молекулярный спектральный анализ По характеру взаимодействия электромагнитного
- 5. По области электромагнитного спектра ультрафиолетовая (УФ) область – 200-400 нм (185-390 нм) видимая область – 400-760
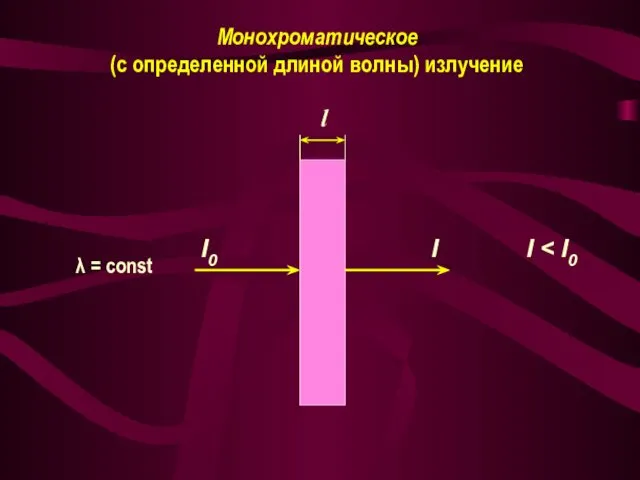
- 6. I0 I l Монохроматическое (с определенной длиной волны) излучение λ = const I
- 7. ПЕРВЫЙ ЗАКОН СВЕТОПОГЛОЩЕНИЯ (закон Бугера-Ламберта)
- 8. ВТОРОЙ ЗАКОН СВЕТОПОГЛОЩЕНИЯ (закон Бугера-Бера)
- 9. ОБЪЕДИНЕННЫЙ ОСНОВНОЙ ЗАКОН СВЕТОПОГЛОЩЕНИЯ (Бугера-Ламберта-Бера)
- 10. ПРИЧИНЫ ОТКЛОНЕНИЯ ОТ ОСНОВНОГО ЗАКОНА СВЕТОПОГЛОЩЕНИЯ Физико-химические факторы. Инструментальные.
- 11. фотоколориметрический анализ; спектрофотометрический метод. Оба метода основаны на основном законе светопоглощения. МЕТОДЫ АБСОРБЦИОННОГО АНАЛИЗА
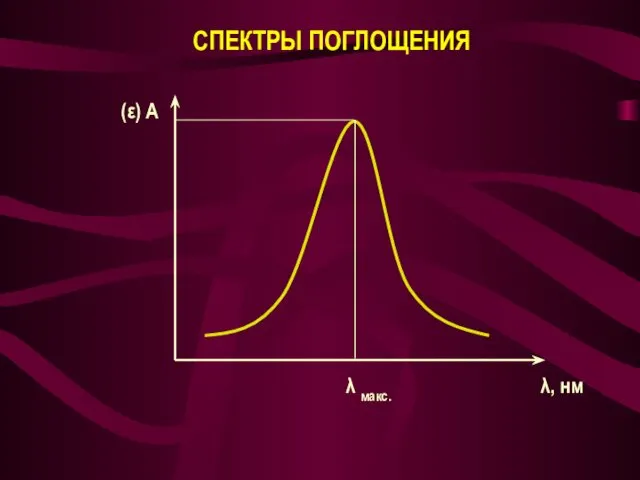
- 12. СПЕКТРЫ ПОГЛОЩЕНИЯ λ макс. λ, нм (ε) А
- 13. УСЛОВИЯ ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ фотометрическая реакция (если необходимо); выбор аналитической длины волны; выбор толщины поглощающего слоя; использование
- 14. РЕФРАКТОМЕТРИЯ
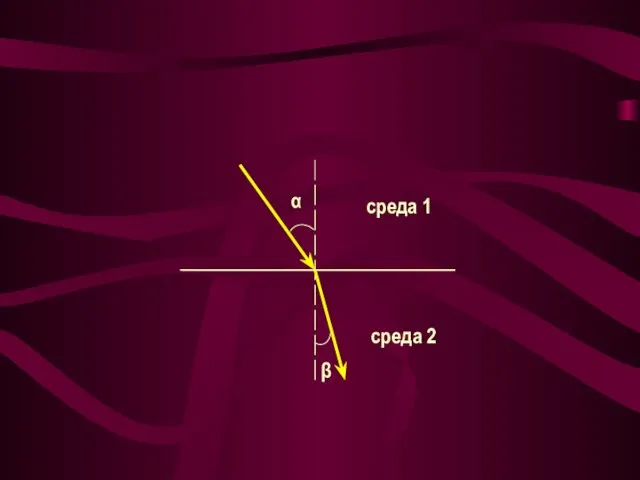
- 15. среда 1 среда 2 α β
- 16. Закон Снеллиуса
- 17. СПОСОБЫ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ По калибровочному графику По таблицам По рефрактометрическому фактору
- 18. ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- 19. КЛАССИФИКАЦИЯ ЭЛЕКТРОХИМИЧЕСКИХ МЕТОДОВ АНАЛИЗА Потенциометрический анализ. Кондуктометрический анализ. Вольтамперометрический анализ. Кулонометрический анализ. По способу применения электрохимических
- 20. Ep – измеряемая ЭДС реакции; Eo – стандартная ЭДС реакции (разность стандартных электродных потенциалов); R –
- 21. КЛАССИФИКАЦИЯ ЭЛЕКТРОДОВ ПО НАЗНАЧЕНИЮ индикаторные электроды; стандартные электроды сравнения.
- 22. КЛАССИФИКАЦИЯ ПОТЕНЦИОМЕТРИЧЕСКИХ МЕТОДОВ АНАЛИЗА 1. Прямая потенциометрия: - рН-метрия; - ионометрия. 2. Потенциометрическое титрование.
- 23. ОПРЕДЕЛЕНИЕ КОНЦЕНТРАЦИИ ВЕЩЕСТВА В ПРЯМОЙ ПОТЕНЦИОМЕТРИИ 1. Метод градуировочного графика. 2. Метод добавок стандарта.
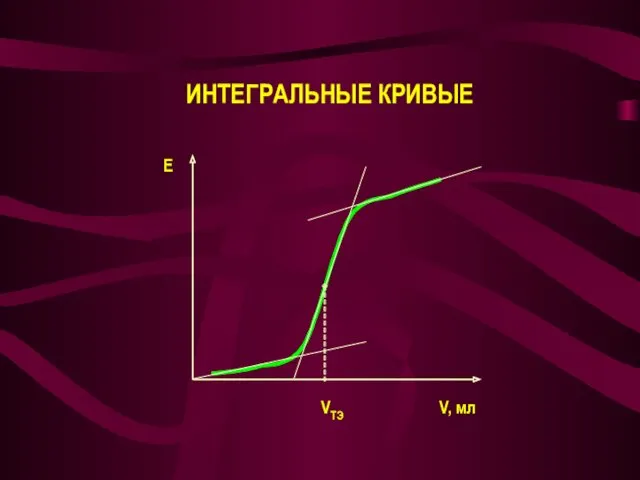
- 24. ИНТЕГРАЛЬНЫЕ КРИВЫЕ VTЭ V, мл
- 25. КОНДУКТОМЕТРИЧЕСКИЙ АНАЛИЗ (КОНДУКТОМЕТРИЯ) основан на использовании зависимости между электропроводностью растворов электролитов и их концентрацией
- 26. ПРЯМАЯ КОНДУКТОМЕТРИЯ МЕТОДЫ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ В ПРЯМОЙ КОНДУКТОМЕТРИИ расчетный метод метод градуировочного графика
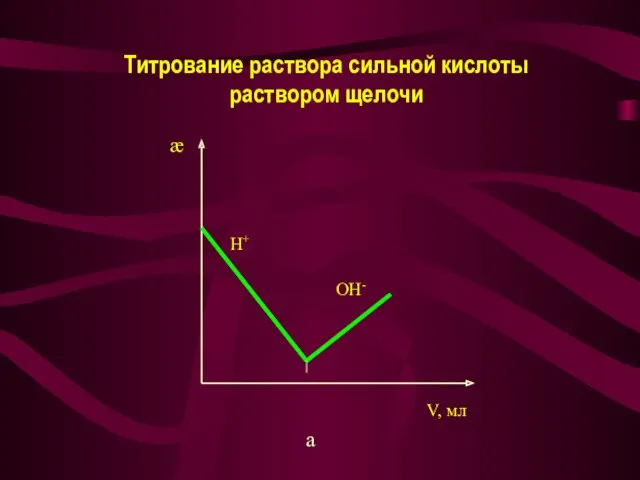
- 27. Титрование раствора сильной кислоты раствором щелочи а
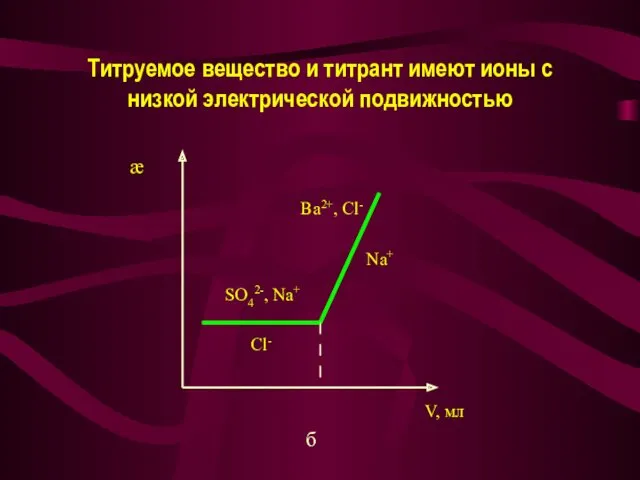
- 28. Титруемое вещество и титрант имеют ионы с низкой электрической подвижностью б
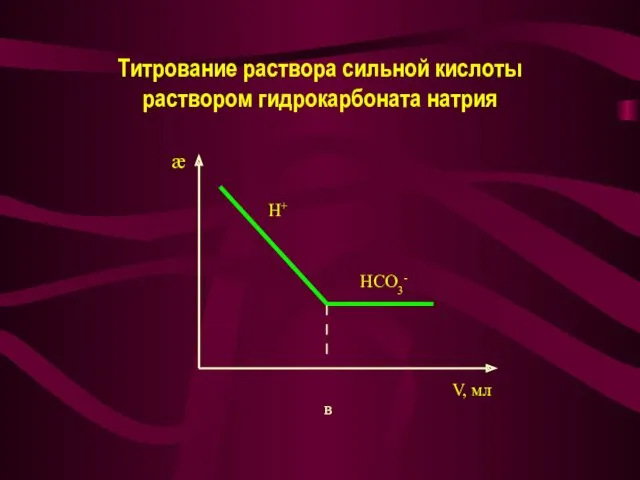
- 29. Титрование раствора сильной кислоты раствором гидрокарбоната натрия V, мл
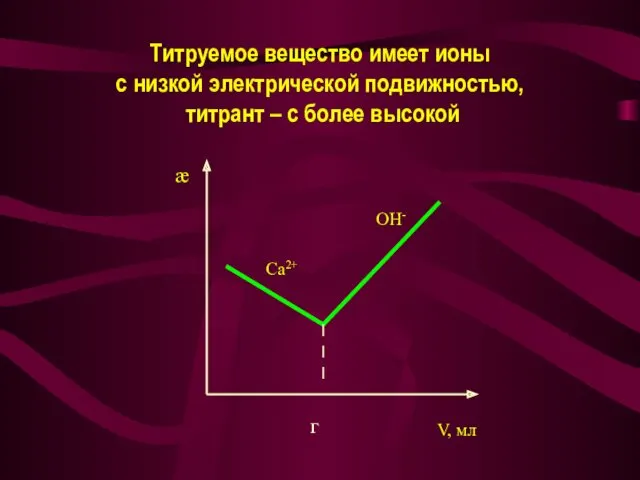
- 30. Титруемое вещество имеет ионы с низкой электрической подвижностью, титрант – с более высокой V, мл
- 31. ПОЛЯРОГРАФИЧЕСКИЙ АНАЛИЗ (ПОЛЯРОГРАФИЯ) основан на использовании зависимости силы тока, протекающего при электролизе раствора, от концентрации электродноактивных
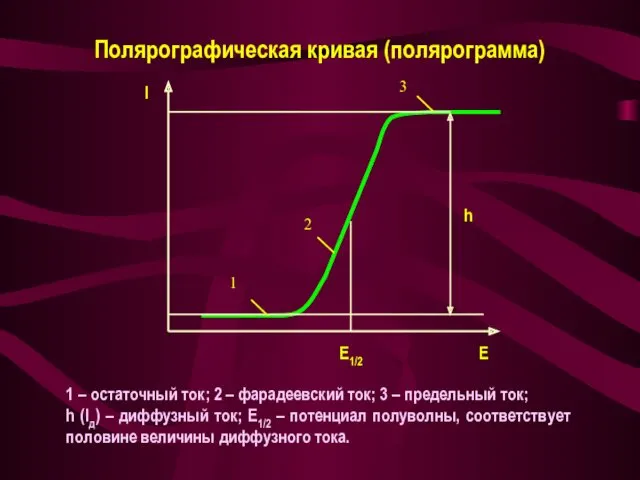
- 32. Полярографическая кривая (полярограмма) 1 – остаточный ток; 2 – фарадеевский ток; 3 – предельный ток; h
- 33. АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 34. КРИВЫЕ АМПЕРОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
- 35. КУЛОНОМЕТРИЧЕСКИЙ АНАЛИЗ (КУЛОНОМЕТРИЯ) основан на использовании зависимости между массой вещества, прореагировавшего при электролизе в электрохимической ячейке,
- 36. ЗАКОН ЭЛЕКТРОЛИЗА ФАРАДЕЯ
- 37. ИОНООБМЕННАЯ ХРОМАТОГРАФИЯ
- 39. Скачать презентацию











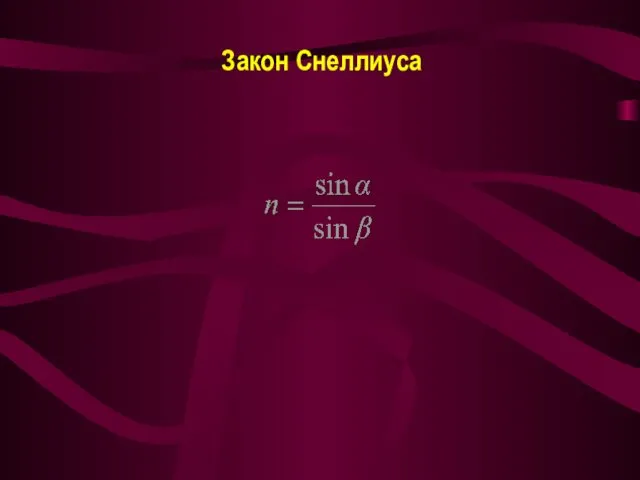















 Презентация к уроку физики Первый закон термодинамики
Презентация к уроку физики Первый закон термодинамики Потенциал. Решение задач
Потенциал. Решение задач Молекулярная физика. Молекулярно-кинетическая теория. Масса и размеры молекул
Молекулярная физика. Молекулярно-кинетическая теория. Масса и размеры молекул Определение элементного состава вещества методом рентгенофлуоресцентной спектроскопии
Определение элементного состава вещества методом рентгенофлуоресцентной спектроскопии Теоретическая механика. Кинематика. Курс лекций
Теоретическая механика. Кинематика. Курс лекций Виды спектров
Виды спектров Класифікація плугів. Класифікація фрез. Лекція 3
Класифікація плугів. Класифікація фрез. Лекція 3 Положительные лучи. Определение истинных масс атомов. Изотопы. АФ1.5
Положительные лучи. Определение истинных масс атомов. Изотопы. АФ1.5 Зат құрылысының атомдық теориясы
Зат құрылысының атомдық теориясы Детекторы ионизирующих излучений. Сцинтилляционные методы детектирования ионизирующих излучений
Детекторы ионизирующих излучений. Сцинтилляционные методы детектирования ионизирующих излучений Теорема об изменении импульса механической системы
Теорема об изменении импульса механической системы Работа и мощность электрического тока. Единицы работы электрического тока
Работа и мощность электрического тока. Единицы работы электрического тока Основы слесарно-сборочных и электромонтажных работ. Резка
Основы слесарно-сборочных и электромонтажных работ. Резка Физико-технические основы электроэнергетики. Лекция 11
Физико-технические основы электроэнергетики. Лекция 11 Импульс тела. Закон сохранения
Импульс тела. Закон сохранения Температура
Температура Урок по теме Квантовые постулаты Бора, 11 класс
Урок по теме Квантовые постулаты Бора, 11 класс Сложные электрические цепи
Сложные электрические цепи Общие свойства ионизирующих излучений ядерного взрыва
Общие свойства ионизирующих излучений ядерного взрыва Средства конвективного нагрева
Средства конвективного нагрева Проявление сил тяжести и упругости живой природе
Проявление сил тяжести и упругости живой природе Терморазведка. Тепловое поле
Терморазведка. Тепловое поле Nucleul atomic
Nucleul atomic Гироскопические приборы и устройства. (Модуль 2.7)
Гироскопические приборы и устройства. (Модуль 2.7) Сұйықтардың беттік керілуі
Сұйықтардың беттік керілуі Расчет количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении
Расчет количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении Принципы радиосвязи
Принципы радиосвязи Механические колебания. Кинематика и динамика колебательного движения
Механические колебания. Кинематика и динамика колебательного движения