Содержание
- 2. Описание равновесных термодинамических процессов может быть выполнено с помощью метода термодинамических потенциалов, разработанного в 1873 -
- 3. В зависимости от выбора двух независимых параметров можно ввести термодинамические потенциалы, дифференцирование которых дает возможность определить
- 4. Использование в качестве независимых параметров V и S не очень удобно, так как величина энтропии не
- 5. Если процесс происходит при постоянном давлении (P = const), то учитывая формулу TdS = δQ, имеем
- 6. 3 Если в качестве независимых параметров выбрать объем V и температуру T Термодинамический потенциал Ψ(V,T) называется
- 7. Термодинамические потенциалы При описании необратимого процесса необходимо применять неравенство Если в системе происходит необратимый процесс, при
- 8. 4 При выборе в качестве независимых переменных давления P и температуры T и введения функции состояния
- 9. Между термодинамическими потенциалами могут быть установлены соотношения, позволяющие выразить одни потенциалы через другие. Уравнение Гиббса-Гельмгольца: Связь
- 10. Кроме химического потенциала можно так же ввести удельный термодинамический потенциал, рассчитанный на единицу массы вещества в
- 11. При обратимом адиабатическом расширении температура газа изменяется в соответствии с уравнением адиабаты. Для идеального газа: Эффект
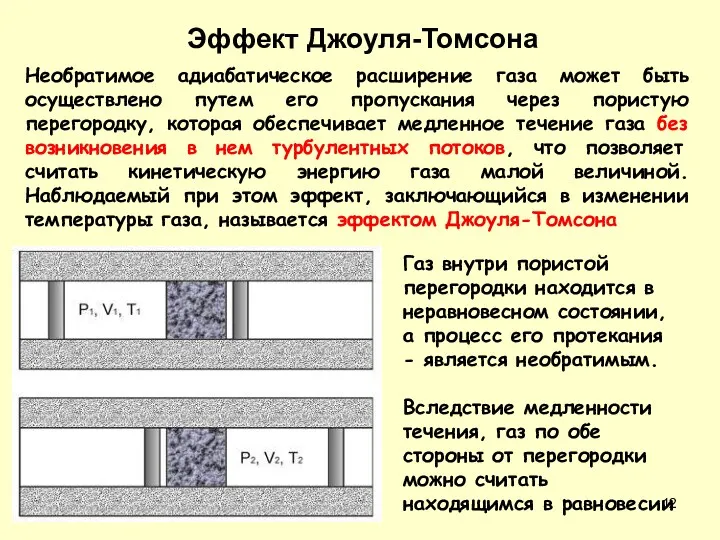
- 12. Необратимое адиабатическое расширение газа может быть осуществлено путем его пропускания через пористую перегородку, которая обеспечивает медленное
- 13. Давления P1 и P2 в обеих частях цилиндрической трубки поддерживались постоянными. Пусть при протекании через пористую
- 14. Из 1-го закона термодинамики, учитывая постоянство Р1 и Р2: Следовательно, рассматриваемый процесс является не только адиабатическим,
- 15. Полный дифференциал энтальпии: Тогда: Эффект Джоуля-Томсона Отсюда:
- 16. Из определений потенциала Гиббса: или для бесконечно малого изменения давления Подставляя полученные соотношения в выражение для
- 17. Если использовать идеальный газ, описываемый уравнением Клапейрона-Менделеева, то имеем: Следовательно, для идеального газа ΔT/ΔP = 0
- 18. Уравнение Ван-дер-Ваальса Рассмотрим применение в опыте Джоуля-Томсона газа Ван-дер-Ваальса, уравнение для одного моля которого имеет вид:
- 19. Выражая P из формулы уравнения В-д-В и подставляя в полученное выражение с последующим пренебрежением малыми слагаемыми
- 20. Эффект Джоуля-Томсона Процесс охлаждения газа может быть реализован так же с помощью обратимого адиабатического расширения. При
- 21. Эффект Джоуля-Томсона С учетом полученных выше можно записать: Для газов характерно изобарическое расширение при их нагревании.
- 23. Скачать презентацию



















 Зануление
Зануление Тормозная система КамАЗа
Тормозная система КамАЗа Модели простых сплошных сред
Модели простых сплошных сред Электрические цепи переменного тока. Лекция 2
Электрические цепи переменного тока. Лекция 2 Характеристики спектров кристаллов
Характеристики спектров кристаллов Виды топлива
Виды топлива Development of a high performance optical cesium beam clock for ground applications
Development of a high performance optical cesium beam clock for ground applications Система энергоснабжения и электрического пуска двигателя. Тема 21
Система энергоснабжения и электрического пуска двигателя. Тема 21 Атмосферное давление. Интегрированный урок
Атмосферное давление. Интегрированный урок Сила упругости
Сила упругости Сила. Графічне зображення сил
Сила. Графічне зображення сил Основы молекулярной и статистической физики
Основы молекулярной и статистической физики Тоқ көздері. Бөгде күштер
Тоқ көздері. Бөгде күштер Плавание тел
Плавание тел Ядерные реакторы
Ядерные реакторы Электрические цепи постоянного тока. (Лекция 1)
Электрические цепи постоянного тока. (Лекция 1) Теория электрических цепей
Теория электрических цепей Енераторларға техникалық қызмет көрсету және жөндеу
Енераторларға техникалық қызмет көрсету және жөндеу Свойства и строение жидкости
Свойства и строение жидкости Теплообменные процессы
Теплообменные процессы Bases of endoscopic surgery
Bases of endoscopic surgery 20181129_elektricheskoe_soprotivlenie.udelnoe_soprotivlenie
20181129_elektricheskoe_soprotivlenie.udelnoe_soprotivlenie Механика. Введение. Кинематика
Механика. Введение. Кинематика Энтропия. Второе начало термодинамики
Энтропия. Второе начало термодинамики Взаимодействие света с веществом. Лекция №8
Взаимодействие света с веществом. Лекция №8 Электрический ток
Электрический ток Физика горных пород. Жидкости и газы в горных породах
Физика горных пород. Жидкости и газы в горных породах Сила. Явление тяготения. Сила тяжести
Сила. Явление тяготения. Сила тяжести