Содержание
- 2. Основные понятия и определения Движущей силой адсорбции является стремление системы уменьшить свою поверхностную энергию за счет
- 3. Адсорбент (поглотитель) – вещество, на поверхности которого идет адсорбция. Адсорбат – вещество, которое адсорбируется на поверхности
- 4. Количественные способы выражения величины адсорбции 1. Абсолютная адсорбция (А) – количество вещества (моль) в поверхностном слое,
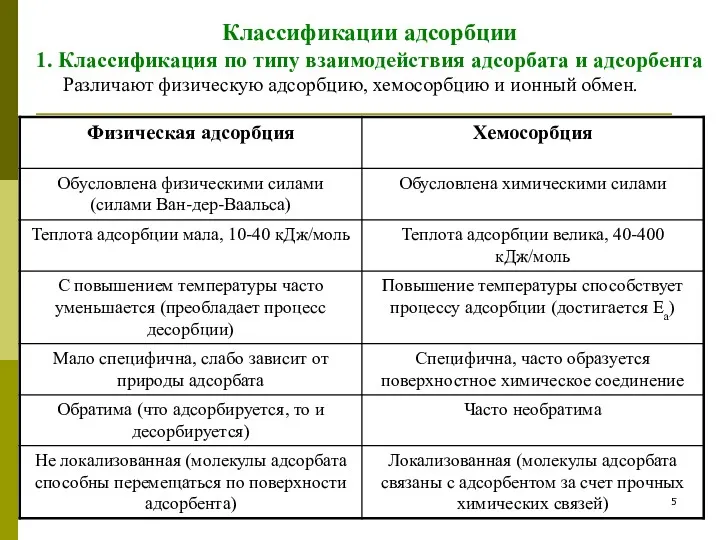
- 5. Классификации адсорбции 1. Классификация по типу взаимодействия адсорбата и адсорбента Различают физическую адсорбцию, хемосорбцию и ионный
- 6. Хемосорбция - процесс образования поверхностного химического соединения. Например: хемосорбция кислорода на угле, в результате окисления поверхностных
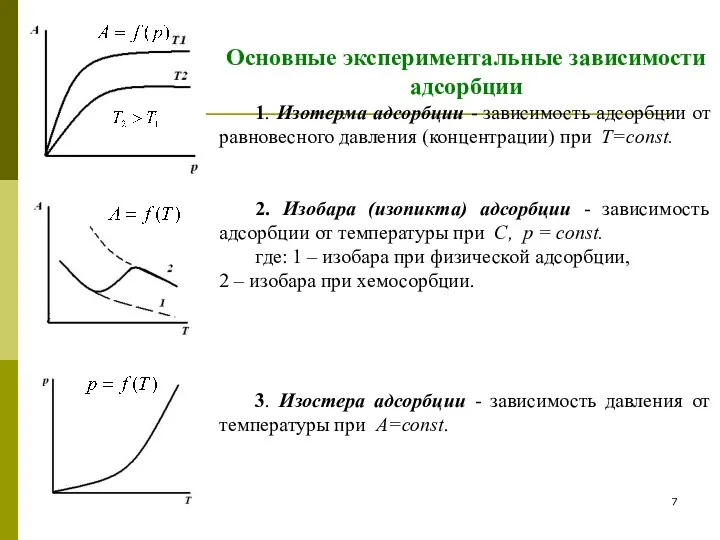
- 7. Основные экспериментальные зависимости адсорбции 1. Изотерма адсорбции - зависимость адсорбции от равновесного давления (концентрации) при Т=const.
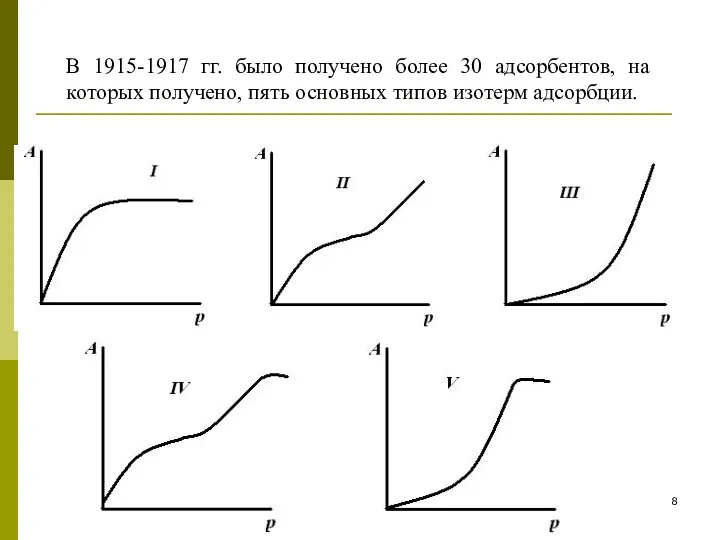
- 8. В 1915-1917 гг. было получено более 30 адсорбентов, на которых получено, пять основных типов изотерм адсорбции.
- 9. Адсорбция на границе твердое тело – газ Основные уравнения: Уравнение адсорбции Лэнгмюра (1915 г.) Величина А∞
- 10. Анализ уравнения адсорбции Лэнгмюра Изотерма Лэнгмюра в координатах А=f(p) Изотерма Лэнгмюра в координатах θ =f(p) I
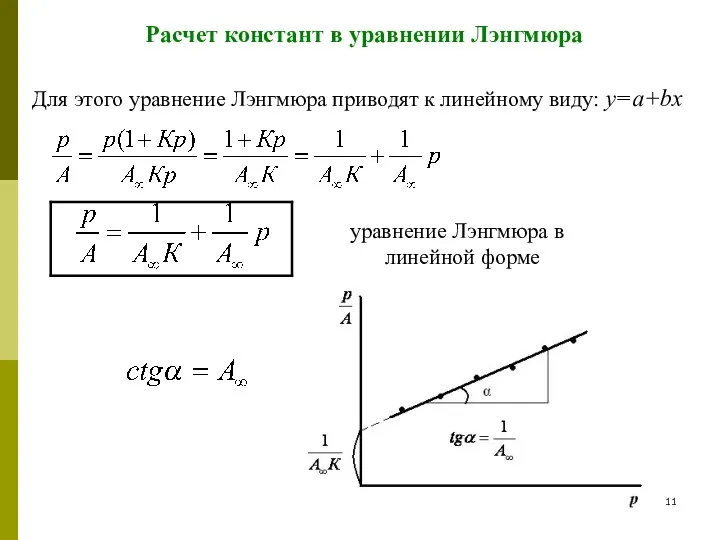
- 11. Расчет констант в уравнении Лэнгмюра Для этого уравнение Лэнгмюра приводят к линейному виду: y=a+bx уравнение Лэнгмюра
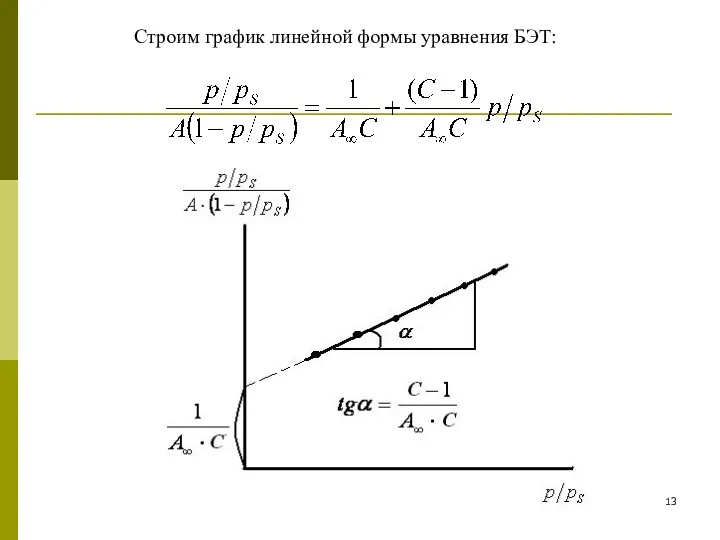
- 12. 2. Уравнение полимолекулярной адсорбции БЭТ. Современная обобщенная теория полимолекулярной адсорбции была развита в 1935-1940 гг. Брунауэром,
- 13. Строим график линейной формы уравнения БЭТ:
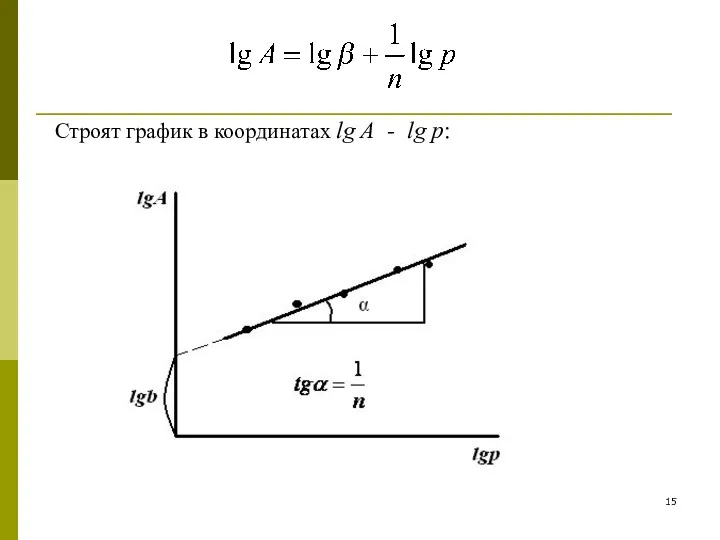
- 14. 3. Эмпирическое уравнение адсорбции Фрейндлиха Физический смысл констант: β – значение адсорбции при парциальном давлении газа,
- 15. Строят график в координатах lg A - lg p:
- 16. Особенность границы раздела : на границе раздела фаз нет активных центров, поверхность жидкости гладкая; молекулы адсорбата
- 17. Фундаментальное уравнение адсорбции Гиббса (вывод) Запишем объединенное уравнение первого и второго начал термодинамики для систем с
- 18. Фундаментальное адсорбционное уравнение Гиббса Уравнение теоретически применимо к любой границе раздела фаз, но в основном используется
- 19. Получим выражение, связывающее величину поверхностного натяжения с концентраций адсорбата. Для системы. состоящей из двух компонентов: растворителя
- 20. Анализ адсорбционного уравнения Гиббса Из уравнения Гиббса следует, что концентрирование вещества в поверхностном слое или, наоборот,
- 21. Свойства ПАВ и ПИВ Поверхностно-инактивные вещества а) σПИВ > σ0; б) ПИВ хорошо растворимы в растворителе
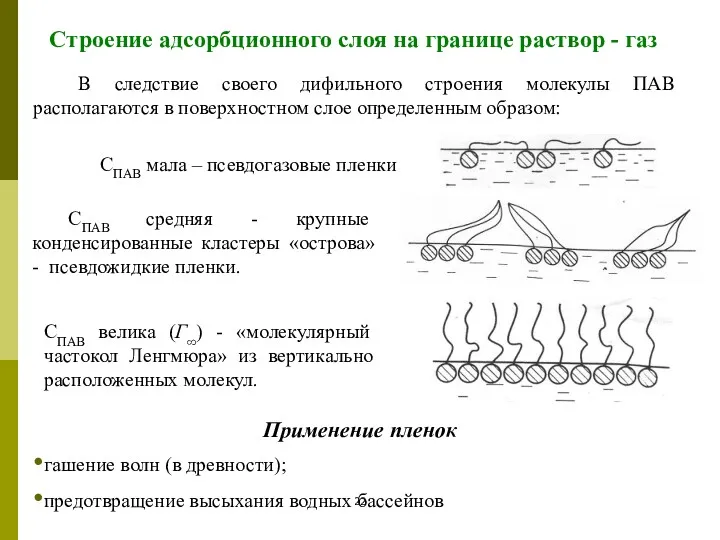
- 22. Строение адсорбционного слоя на границе раствор - газ В следствие своего дифильного строения молекулы ПАВ располагаются
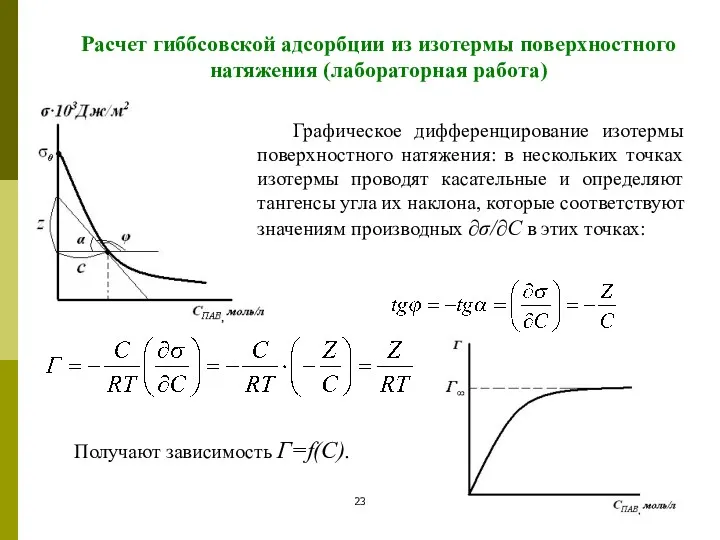
- 23. Расчет гиббсовской адсорбции из изотермы поверхностного натяжения (лабораторная работа) Графическое дифференцирование изотермы поверхностного натяжения: в нескольких
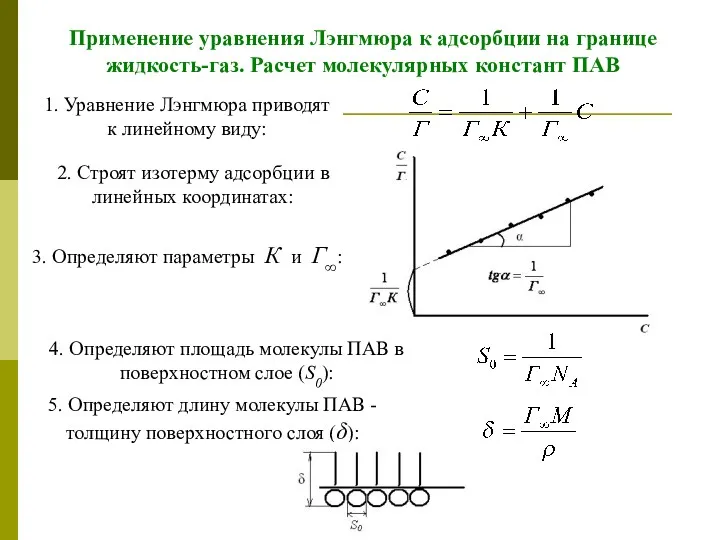
- 24. Применение уравнения Лэнгмюра к адсорбции на границе жидкость-газ. Расчет молекулярных констант ПАВ 1. Уравнение Лэнгмюра приводят
- 25. СПАВ мала: СПАВ средние: Эмпирическое уравнение Б.А.Шишковского (1908) где: В - константа для всего гомологического ряда,
- 26. Подставим уравнение Шишковского в дифференциальной форме в уравнение Гиббса: Физический смысл констант в уравнении Шишковского Отсюда:
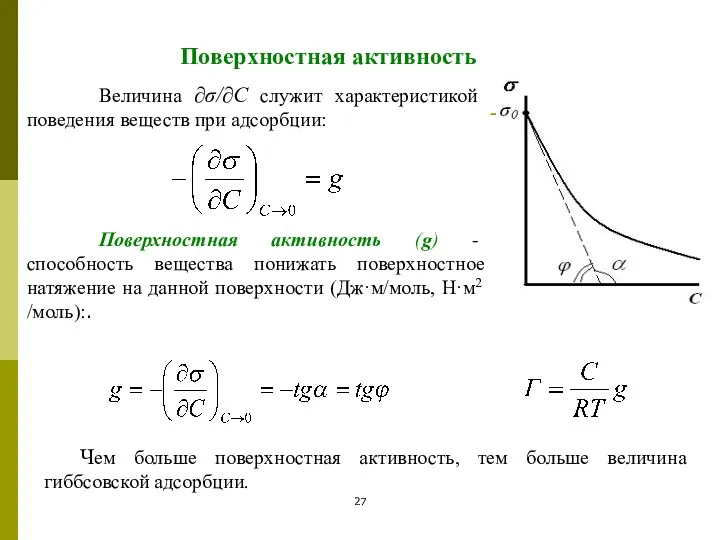
- 27. Поверхностная активность Величина ∂σ/∂С служит характеристикой поведения веществ при адсорбции: Поверхностная активность (g) - способность вещества
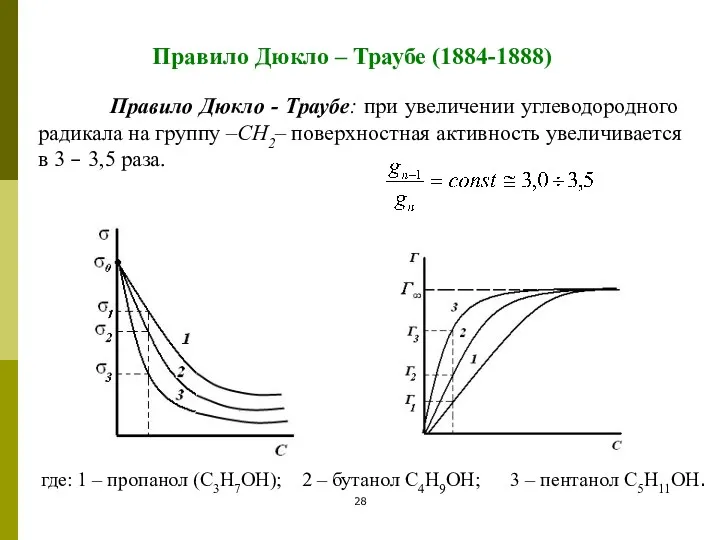
- 28. Правило Дюкло – Траубе (1884-1888) Правило Дюкло - Траубе: при увеличении углеводородного радикала на группу –СН2–
- 29. Границы применимости правила Дюкло – Траубе 1. Выполняется только для полярного растворителя. Если растворитель не полярный,
- 30. Работа адсорбции Работа адсорбции (Wадс) – работа перемещения 1 моль ПАВ из объема раствора в поверхностный
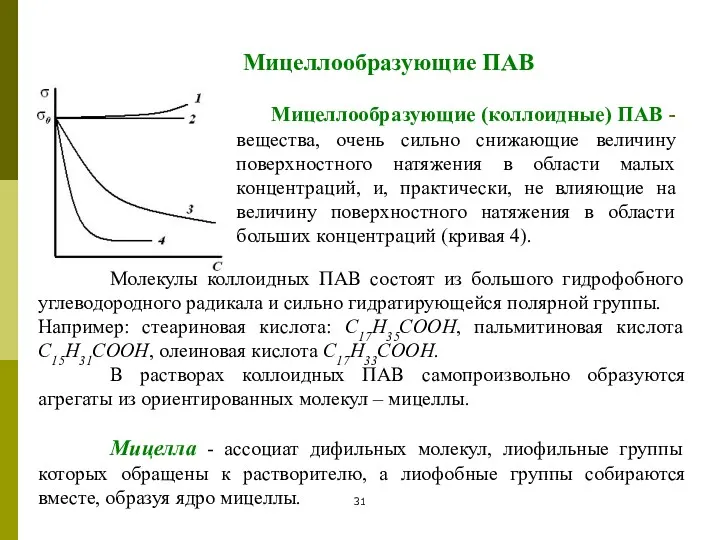
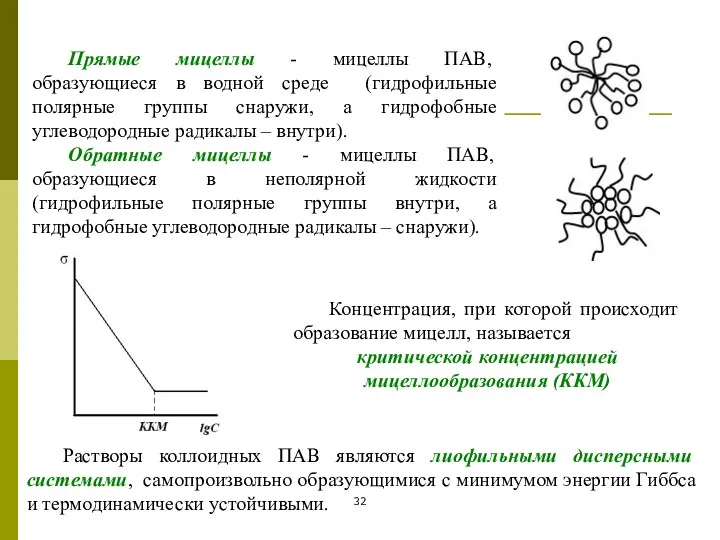
- 31. Мицеллообразующие ПАВ Мицеллообразующие (коллоидные) ПАВ - вещества, очень сильно снижающие величину поверхностного натяжения в области малых
- 32. Концентрация, при которой происходит образование мицелл, называется критической концентрацией мицеллообразования (ККМ) Прямые мицеллы - мицеллы ПАВ,
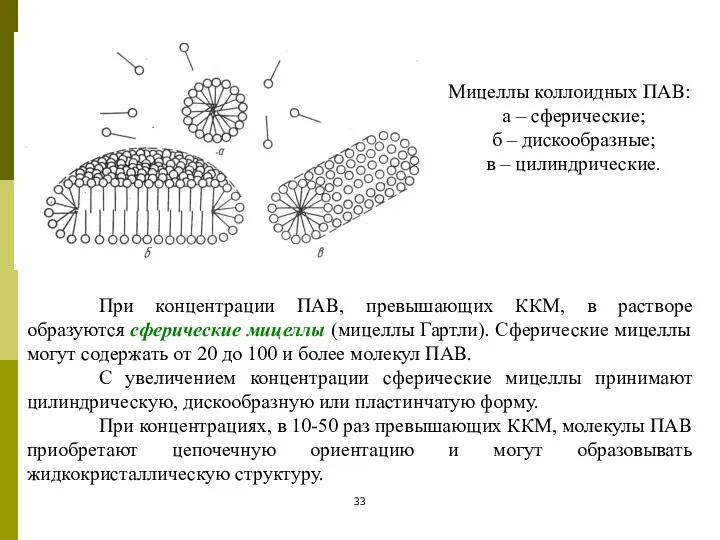
- 33. Мицеллы коллоидных ПАВ: а – сферические; б – дискообразные; в – цилиндрические. При концентрации ПАВ, превышающих
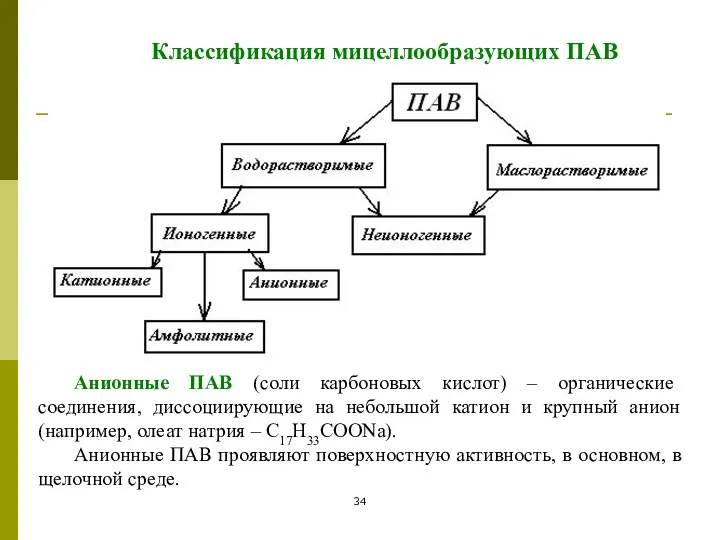
- 34. Классификация мицеллообразующих ПАВ Анионные ПАВ (соли карбоновых кислот) – органические соединения, диссоциирующие на небольшой катион и
- 35. Катионные ПАВ – органические вещества, диссоциирующие на анион (Cl– , SO42–) и поверхностно-активный катион (алифатические и
- 36. Солюбилизация Солюбилизация - явление растворения веществ в мицеллах ПАВ. В водных мицеллярных системах солюбилизируются вещества, нерастворимые
- 37. Адсорбция на границе твердое тело - раствор
- 38. Особенности адсорбции из растворов 1. Одновременно могут протекать два параллельных процесса: адсорбция молекул растворенного вещества; адсорбция
- 39. Молекулярная адсорбция – адсорбция на поверхности адсорбента молекул неэлектролитов. Правило уравнивания полярностей Ребиндера: вещество В будет
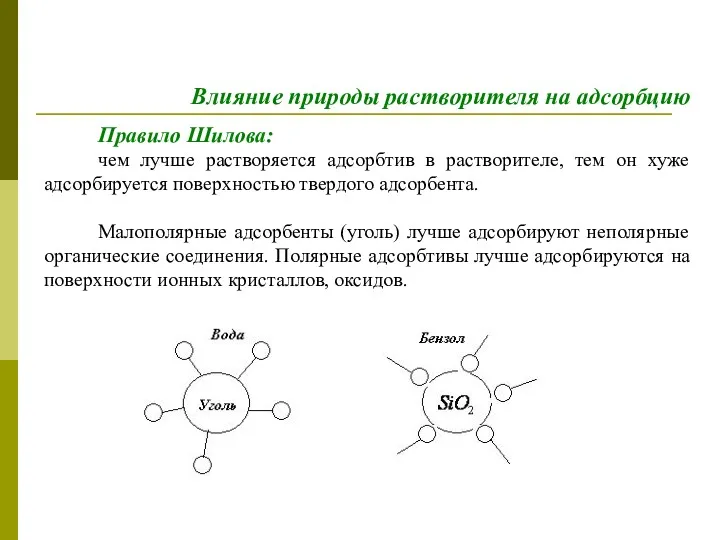
- 40. Правило Шилова: чем лучше растворяется адсорбтив в растворителе, тем он хуже адсорбируется поверхностью твердого адсорбента. Малополярные
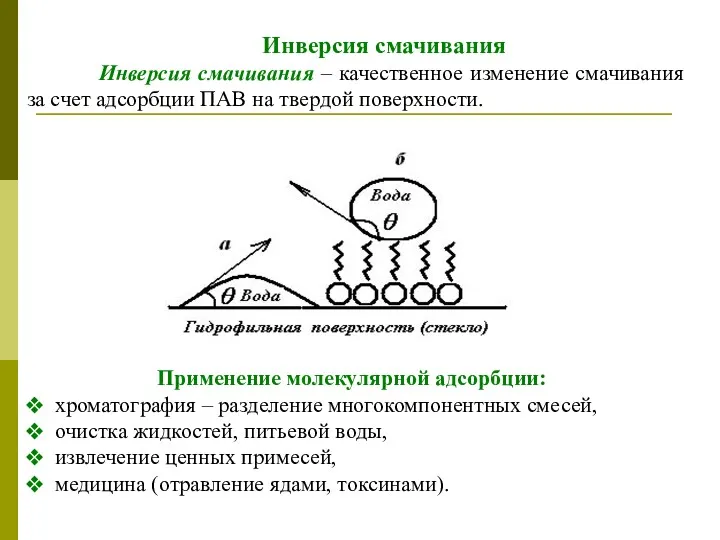
- 41. Инверсия смачивания Инверсия смачивания – качественное изменение смачивания за счет адсорбции ПАВ на твердой поверхности. Применение
- 42. Ионная адсорбция Ионная адсорбция – адсорбция сильных электролитов из водных растворов, обусловленная химическими и электростатическими силами.
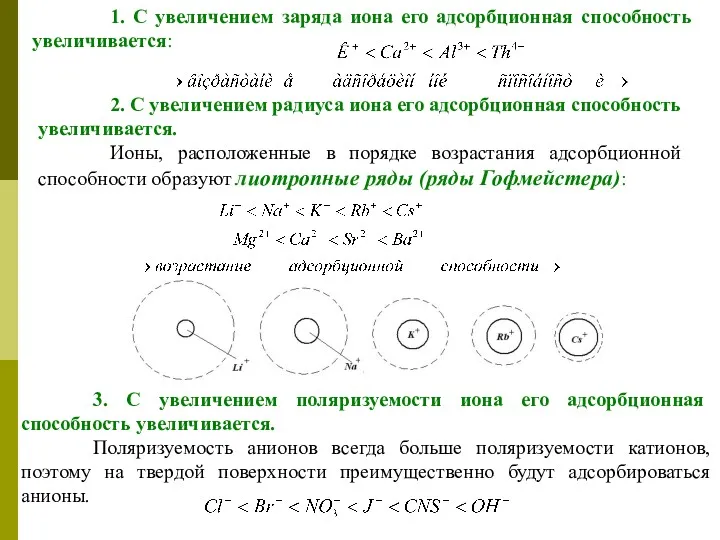
- 43. 1. С увеличением заряда иона его адсорбционная способность увеличивается: 2. С увеличением радиуса иона его адсорбционная
- 44. Ионообменная адсорбция. Ионный обмен Ионообменная адсорбция - процесс обмена ионов между раствором и ионообменником (сорбентом). Ионообменники
- 45. Уравнение изотермы ионного обмена Б.П.Никольского При z1=z2 =1 уравнение упрощается: Применение ионного обмена 1. Обессоливание (деминерализация)
- 46. Адсорбция на пористых адсорбентах Пористые адсорбенты – твердые тела, внутри которых имеются поры, обуславливающие наличие внутренней
- 47. макропористые тела (r > 200 нм), для количественного описания используют уравнения Лэнгмюра; мезопористые (переходнопористые) тела (r
- 48. Капиллярная конденсация на пористых адсорбентах Поры тонкопористых адсорбентов в результате капиллярной конденсации заполняются молекулами адсорбата уже
- 49. Конусообразная пора При смачивании адсорбатом стенок поры, на ее стенках образуется адсорбционная пленка жидкости и в
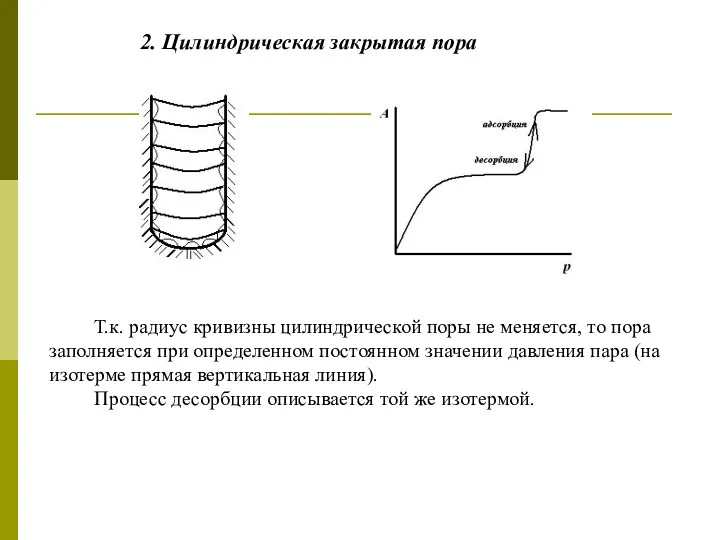
- 50. 2. Цилиндрическая закрытая пора Т.к. радиус кривизны цилиндрической поры не меняется, то пора заполняется при определенном
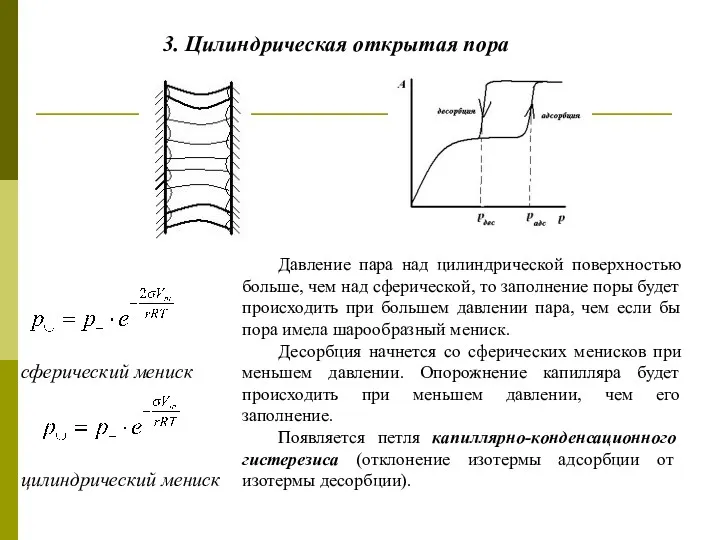
- 51. 3. Цилиндрическая открытая пора сферический мениск цилиндрический мениск Давление пара над цилиндрической поверхностью больше, чем над
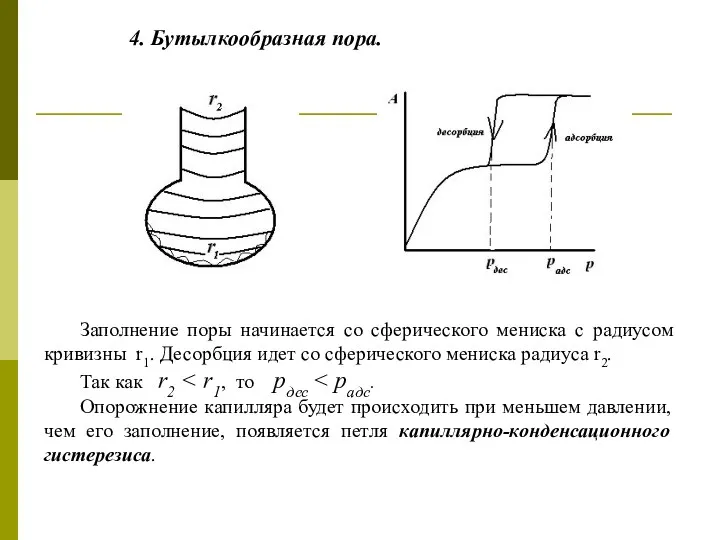
- 52. 4. Бутылкообразная пора. Заполнение поры начинается со сферического мениска с радиусом кривизны r1. Десорбция идет со
- 54. Скачать презентацию






























 Теория сплавов
Теория сплавов Биосенсорные системы
Биосенсорные системы Соли. Классификация
Соли. Классификация Основи. Склад, назви, класифікація, використання
Основи. Склад, назви, класифікація, використання Водород. Общая характеристика, получение, свойства
Водород. Общая характеристика, получение, свойства Арены. Бензол и его гомологи. Химия. 10 класс
Арены. Бензол и его гомологи. Химия. 10 класс Расчеты по химическим уравнениям. Алгоритм решения расчетных задач
Расчеты по химическим уравнениям. Алгоритм решения расчетных задач Химическая взрывчатка
Химическая взрывчатка Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Тағамдық қоспалардың функционалдық жүктелуі және олардың сипаттамасы
Тағамдық қоспалардың функционалдық жүктелуі және олардың сипаттамасы Тест по неорганической химии
Тест по неорганической химии Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Белки. Содержание белков в различных тканях
Белки. Содержание белков в различных тканях Водород. Химические свойства
Водород. Химические свойства Хлор
Хлор Пропилен-алкены(пропен)
Пропилен-алкены(пропен) Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Объемная доля газа в смеси. (Урок 16. 7 класс)
Объемная доля газа в смеси. (Урок 16. 7 класс) Современные тенденции развития химии
Современные тенденции развития химии Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Незвичайна вода
Незвичайна вода Химия. Викторина
Химия. Викторина Карбоновые кислоты. Свойства карбоновых кислот
Карбоновые кислоты. Свойства карбоновых кислот Соли аммония
Соли аммония Азотная кислота
Азотная кислота Керамические материалы
Керамические материалы Химическая промышленность и химические технологии
Химическая промышленность и химические технологии Задачи
Задачи