Содержание
- 2. Карбоновые кислоты – это производные углеводородов, содержащие в молекуле одну или несколько карбоксильных групп. карбонильная группа
- 3. Классификация карбоновых кислот 1. По числу карбоксильных групп: Одноосновные : CH3COOH уксусная Двухосновные : HOOC –
- 4. Общая формула одноосновных карбоновых кислот Номенклатура: К названию соответствующего предельного УВ прибавляется окончание - овая и
- 5. Физические свойства одноосновных карбоновых кислот Низшие карбоновые кислоты – жидкости с острым запахом, хорошо растворимые в
- 6. Химические свойства кислот Общие свойства карбоновых кислот аналогичны соответствующим свойствам неорганических кислот: Диссоциируют в водном растворе.
- 7. 1. Кислоты диссоциируют на ионы водорода и ионы кислотного остатка: 2. Реагируют с металлами: 2CH3COOH +
- 8. 3. Реагируют с основными и амфотерными оксидами и гидроксидами. 2HCOOH + MgO (HCOO)2Mg + H2O 2CH3COOH
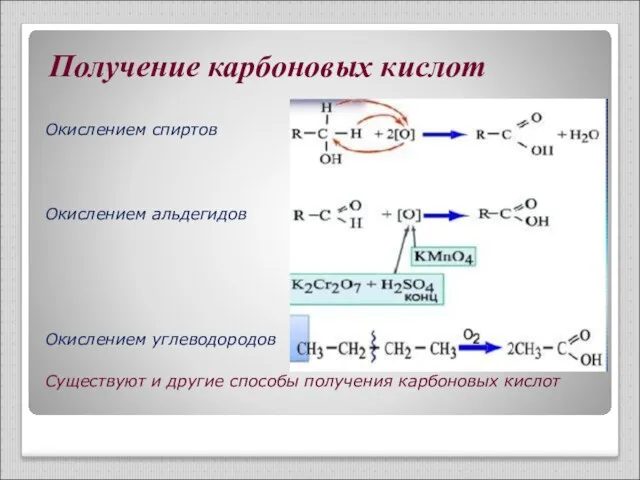
- 9. Получение карбоновых кислот Окислением спиртов Окислением альдегидов Окислением углеводородов Существуют и другие способы получения карбоновых кислот
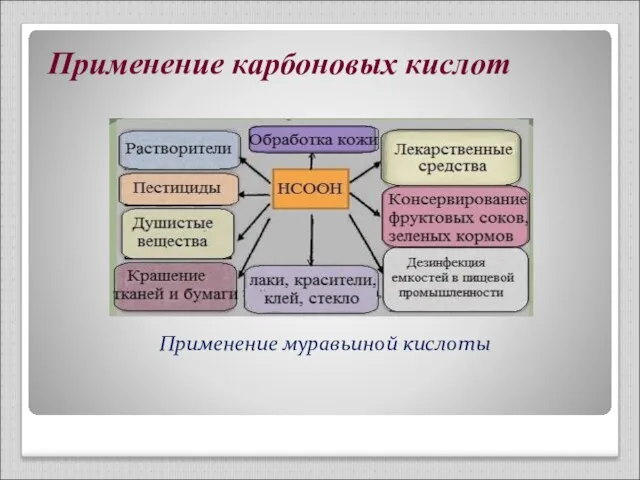
- 10. Применение карбоновых кислот Применение муравьиной кислоты
- 11. Уксусная кислота используется в химической промышленности
- 13. Скачать презентацию








 Иондар және олардың түзілуі
Иондар және олардың түзілуі Амины
Амины Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ
Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ Біологічна хімія з основами фізичної і колоїдної хімії
Біологічна хімія з основами фізичної і колоїдної хімії Білки та амінокислоти
Білки та амінокислоти Роль хімії у суспільстві
Роль хімії у суспільстві Общая схема радиолиза алифатических углеводородов. Радиолиз органических кислот. Радиолиз кетонов эфиров
Общая схема радиолиза алифатических углеводородов. Радиолиз органических кислот. Радиолиз кетонов эфиров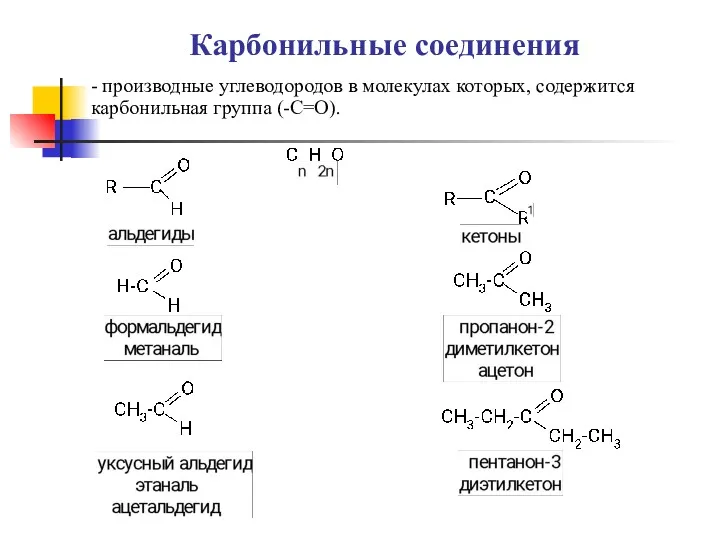 Карбоновые кислоты, альдегиды
Карбоновые кислоты, альдегиды Оксиды. Номенклатура, классификация, физические свойства
Оксиды. Номенклатура, классификация, физические свойства Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1
Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1 Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы”
Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы” Метаболизм нуклеотидов
Метаболизм нуклеотидов Серная кислота и её свойства. 9 класс
Серная кислота и её свойства. 9 класс Галогены. Химические свойства. Применение
Галогены. Химические свойства. Применение Пластмасса, пластикалық материалдар
Пластмасса, пластикалық материалдар Електролітична дисоціація. Електроліти та неелектроліти. Урок хімії в 9 класі
Електролітична дисоціація. Електроліти та неелектроліти. Урок хімії в 9 класі Сахар - вред или польза?
Сахар - вред или польза? Lesson 2 and 3. The chemistry of life
Lesson 2 and 3. The chemistry of life Жири як представники естерів. Класифікація жирів, їхні хімічні властивості
Жири як представники естерів. Класифікація жирів, їхні хімічні властивості Соли как производные кислот и оснований
Соли как производные кислот и оснований Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Фазовые диаграммы
Фазовые диаграммы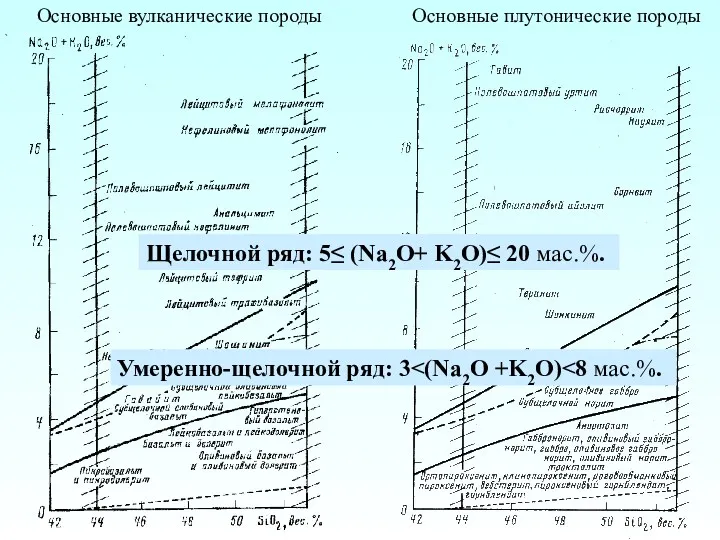 Основные вулканические породы. Основные плутонические породы
Основные вулканические породы. Основные плутонические породы λ-MnO2 as material with pseudocapacitive properties
λ-MnO2 as material with pseudocapacitive properties Электролиз Урок для 11 класса
Электролиз Урок для 11 класса Теории происхождения нефти
Теории происхождения нефти Полибутадиен
Полибутадиен Алкандар. Метан және оның құрылысы
Алкандар. Метан және оның құрылысы