Содержание
- 2. БІОЛОГІЧНА ХІМІЯ – наука, що вивчає хімічну природу сполук, які входять до складу живих організмів, їх
- 3. Фізична і колоїдна хімія Фізична хімія – вивчає зв'язок між хімічними і фізичними процесами, хімічні реакції,
- 4. Розчини – це фізико-хімічні системи, які складаються з двох і більше компонентів: один з них зазвичай
- 5. Класифікація розчинів За агрегатним станом розчинника: газоподібні (повітря, пар) рідкі (мінеральні води, водний розчин глюкози) тверді
- 6. За величиною молекулярної маси розчиненої речовини: низькомолекулярні (водні розчини кислот, лугів) високомолекулярні (розчини білків, нуклеїнових кислот)
- 7. Фізична хімія вивчає: 1. Дифузію 2. Осмос і осмотичний тиск 3. Каталіз 4. Властивості розчинів електролітів
- 8. Дифузія Дифузія (від лат. diffusio — розповсюдження, розтікання) — самовільний процес розподілення молекул, атомів, іонів, колоїдних
- 9. Траєкторії руху частин при дифузії представляють собою ламану лінію, так як під час переміщення частинка постійно
- 10. Швидкість дифузії Швидкість дифузії збільшується при підвищенні температури і градієнта концентрації і зменшується при збільшенні в'язкості
- 11. Дифузія широко розповсюджена в природі. Вона лежить в основі багатьох технологічних процесів — адсорбції, цементації, конденсації,
- 13. Осмос це одностороння дифузія розчинника через напівпроникну мембрану в сторону більшої концентрації розчиненої речовини (а значить
- 14. Онкотичним називають тиск, який створюється колоїдними частинками на напівпроникну мембрану. Часто онкотичним називають тиск, який створюється
- 15. Осмотичний тиск можна виміряти за допомогою осмометру, а також непрямими методами: кріоскопічним – основаним на вимірюванні
- 16. Розчини з осмотичним тиском, рівним осмотичному тиску клітин, і не призводять до зміни об'єму клітин. Найпростішим
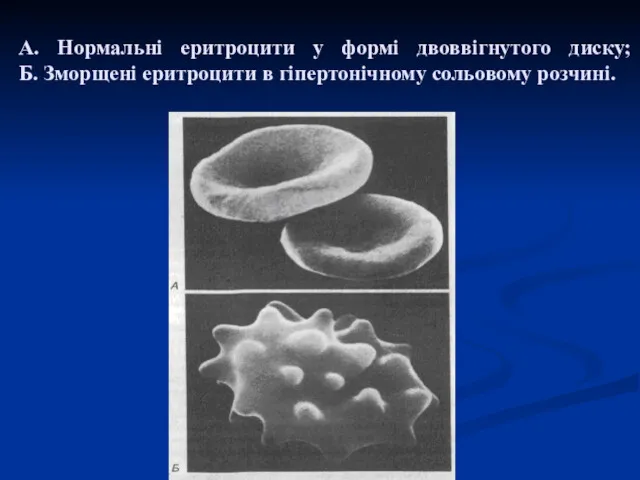
- 17. А. Нормальні еритроцити у формі двоввігнутого диску; Б. Зморщені еритроцити в гіпертонічному сольовому розчині.
- 18. Розчини з більш низьким осмотичним тиском, ніж у клітинах, тому в період ендосмосу розчинник через плазматичну
- 19. Для організму людини і тварин характерним є постійний осмотичний тиск — ізоосмія. Це виражається в осмотичному
- 20. Регуляція сталості осмотичного тиску за рахунок роботи органів виділення за допомогою деяких гормонів (гуморальний шлях регуляції)
- 21. Біологічна дія іонів це специфічний, якісний вплив іонів на клітини Висновки Жака Леба: Більш виражену біологічну
- 22. Дослідження Жака Леба створили передумови для створення фізіологічно еквіліброваних розчинів, тобто розчинів, які здатні довготривалий час
- 23. Дисоціація води Вода — універсальний розчинник для більшості мінеральних і органічних речовин. Організм тварини в середньому
- 24. Водневе число Кислотність, обумовлена наявністю в середовищі (або в розчині) вільних іонів Н+, називається активною кислотністю.
- 25. Водневе число є не зовсім зручним в практичному використанні, тому було запропоновано другий спосіб вираження концентрації
- 26. Методи визначення рН Колориметричний Електрометричний
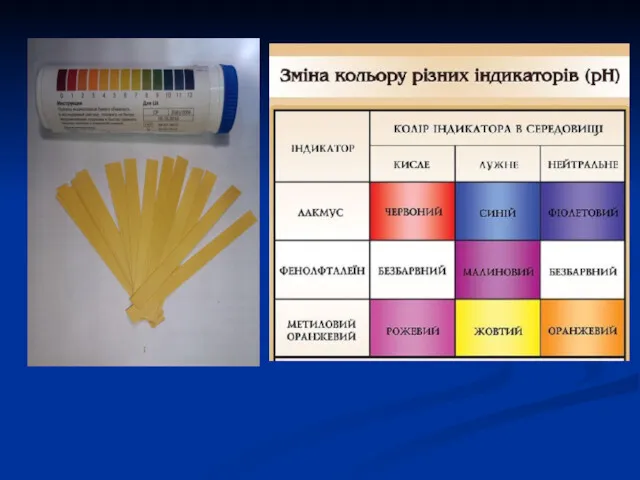
- 27. Колориметричний метод В основі лежить використання індикаторів. Індикатори – це слабкі органічні кислоти або основи, що
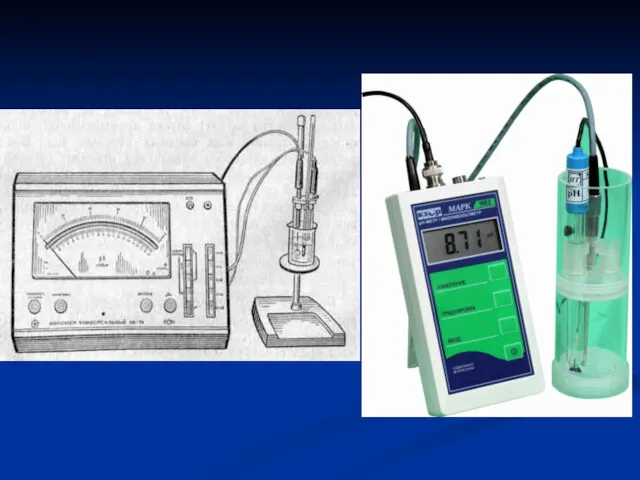
- 29. Електрометричний метод полягає у використанні спеціальних приладів – рН-метрів Їх робота основана на вимірюванні електрорухомої сили
- 31. рН крові деяких тварин Об'єкт дослідження рН Кров людини ............................................... 7,3—7,4 Кров різних ссавців……………. …………7,2—7,5 Птахів.............................................................7,2—7,5
- 32. Біологічна роль рН Концентрація Н+ і ОН– іонів дуже важлива для нормального функціонування живої системи, так
- 33. Буферні розчини це розчини, які здатні стійко підтримувати рН при додаванні невеликої кількості кислоти (або лугу),
- 34. Суміш СЛАБКОЇ основи та солі цієї основи з СИЛЬНОЮ кислотою. Наприклад: (амонійний буфер) Суміш СОЛЕЙ багатоосновної
- 35. Буферні розчини знаходяться у водах світового океану, ґрунтових розчинах та живих організмах. Буферні розчини виконують функції
- 36. Механізм дії При додаванні невеликої кількості НCl до ацетатного буферу змін рН в кислу сторону не
- 37. При додаванні невеликої кількості лугу (основи) до складу буферу відбувається реакція, в результаті якої спостерігається нейтралізація
- 38. Властивості буферів Буферність – здатність зберігати стабільність концентрації іонів Н+ при додаванні до буферного розчину певної
- 39. Буферна ємність – це сила буферної дії. Вона залежить від концентрації компонентів буфера: чим вище концентрація,
- 40. Значення сталості рН Концентрація іонів Н+ має важливе значення для перебігу багатьох біохімічних процесів в організмах
- 41. Причини ацидозу Внутрішні. Це порушення обміну речовин, що пов'язанні з утворенням великої кількості кислих продуктів. Наприклад,
- 42. При ацидозі розрізняють 2 види (або 2 стадії): Компенсований ацидоз – коли захворювання вже почало розвиватися,
- 44. Скачать презентацию






































 Сахар - вред или польза?
Сахар - вред или польза? Evolution of Isoconversional Methods
Evolution of Isoconversional Methods Кислородсодержащие соединения серы. Оксиды серы
Кислородсодержащие соединения серы. Оксиды серы Простые вещества металлы
Простые вещества металлы Химическая стойкость тугоплавких металлов в различных реагентах
Химическая стойкость тугоплавких металлов в различных реагентах Предельные одноатомные спирты
Предельные одноатомные спирты Геохимическая классификация элементов
Геохимическая классификация элементов Химические реакции. Реакции разложения
Химические реакции. Реакции разложения Магній. Знаходження в періодичній системі і основні характеристики
Магній. Знаходження в періодичній системі і основні характеристики Количественный учет влияния заместителя на реакционную способность и его использование для интерпретации механизмов реакций
Количественный учет влияния заместителя на реакционную способность и его использование для интерпретации механизмов реакций Мұнай. Мұнайдың шығу тарихы
Мұнай. Мұнайдың шығу тарихы Пестициды. Лекция
Пестициды. Лекция Предмет и задачи химии. Вещества и их свойства (продолжение)
Предмет и задачи химии. Вещества и их свойства (продолжение) Анионы. Группы анионов
Анионы. Группы анионов Кислородсодержащие соединения серы
Кислородсодержащие соединения серы Лигандообменные равновесия и процессы. Строение комплексных соединений
Лигандообменные равновесия и процессы. Строение комплексных соединений Стронций
Стронций Классификация химических реакций
Классификация химических реакций 20231012_metally.fizicheskie_svoystva
20231012_metally.fizicheskie_svoystva Матеріальний баланс процесу горіння
Матеріальний баланс процесу горіння Химические аспекты метаболизма лекарственных препаратов
Химические аспекты метаболизма лекарственных препаратов Атомно-кристаллическое строение материалов
Атомно-кристаллическое строение материалов Щелочноземельные металлы
Щелочноземельные металлы Электролитическая диссоциация
Электролитическая диссоциация Алкани, насичені вуглеводні
Алкани, насичені вуглеводні Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений
Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений Количество вещества. 8 класс
Количество вещества. 8 класс Химические волокна (7 класс)
Химические волокна (7 класс)