уксусную кислоту, этаналь, этанол, хлоропреновый каучук, клей ПВА и т.д.
Этен является сырьем для производства этанола, этиленгликоля, дихлорэтана, полиэтилена
Из пропена получают глицерин, ацетон, изопропанол, растворители, полипропилен
Метан является источником водорода для:
синтеза аммиака
получения синтез – газа, применяемого для промышленного синтеза углеводородов, спиртов, альдегидов и др. ОВ
сырье для производства органических веществ и материалов: альдегидов, кетонов, растворителей (тетрагалогенэтанов), исходных веществ для получения синтетических каучуков, поливинилхлорида и др.полимеров
сырье для производства органических веществ и материалов
топливо
горючее для дизельных и турбореактивных двигателей
основа смазочных масел
сырье для производства синтетических жиров
алкины
алкены
алканы
 Природные источники углеводородов
Природные источники углеводородов Водород. Свойства водорода
Водород. Свойства водорода Жесткость воды
Жесткость воды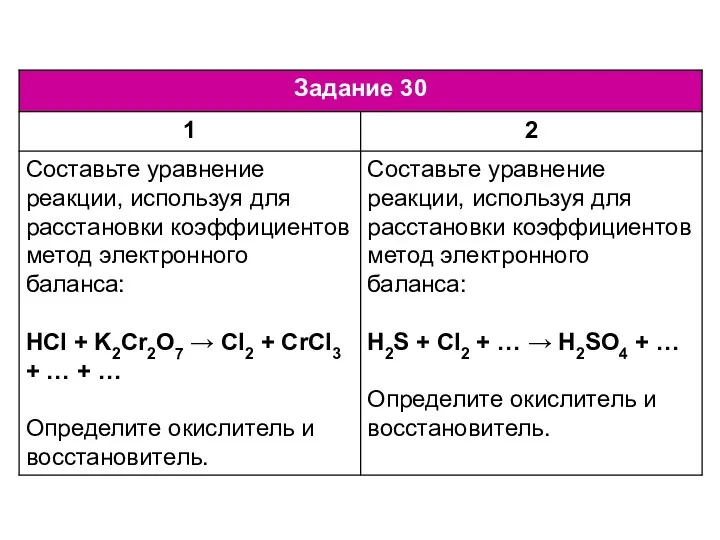 ЕГЭ по химии. Задание 30-34
ЕГЭ по химии. Задание 30-34 Технология переработки нефти. Синтез метил-трет-бутилового и трет-амилметилового эфиров. (Лекция 4.4)
Технология переработки нефти. Синтез метил-трет-бутилового и трет-амилметилового эфиров. (Лекция 4.4)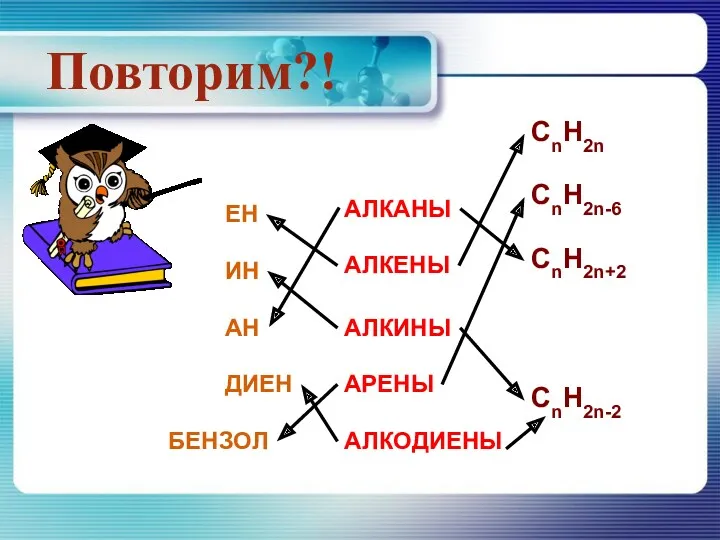 Органические вещества: производные углеводородов
Органические вещества: производные углеводородов Щелочные металлы
Щелочные металлы Основи. Склад, назви, класифікація, використання
Основи. Склад, назви, класифікація, використання Переработка газа. Первичная переработка нефти. Лекция 9
Переработка газа. Первичная переработка нефти. Лекция 9 Evolution of Isoconversional Methods
Evolution of Isoconversional Methods Бальзам-ополаскиватель для волос
Бальзам-ополаскиватель для волос Генетическая связь между классами неорганических веществ. 8 класс
Генетическая связь между классами неорганических веществ. 8 класс Р-элементы IV Группы Периодической Системы
Р-элементы IV Группы Периодической Системы Минералы и горные породы
Минералы и горные породы Электролитическая диссоциация. Вещества в растворах
Электролитическая диссоциация. Вещества в растворах Одноатомные и многоатомные спирты
Одноатомные и многоатомные спирты Чистые вещества и смеси
Чистые вещества и смеси 20231011_8_klass_binarnye_soedineniya
20231011_8_klass_binarnye_soedineniya Элементы кристаллохимии
Элементы кристаллохимии Оксиды. Формулы оксидов ( 8 класс)
Оксиды. Формулы оксидов ( 8 класс) Мило. Мийні засоби
Мило. Мийні засоби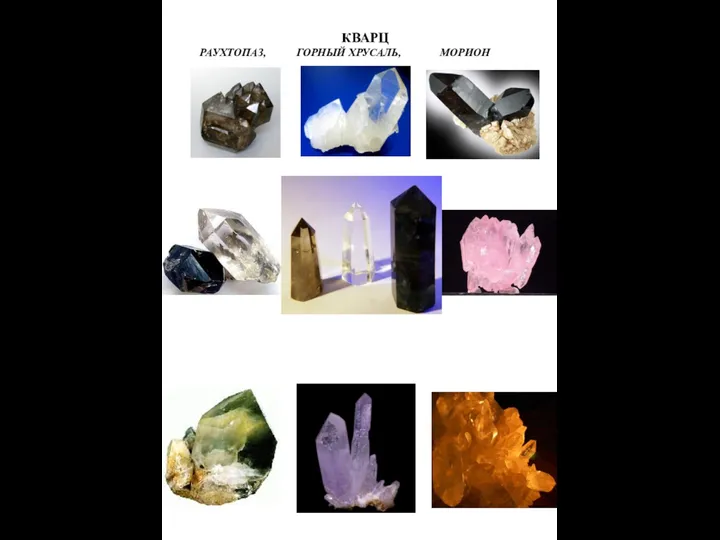 Кварц
Кварц Азотные удобрения
Азотные удобрения Натуральный каучук
Натуральный каучук Определение расхода воздуха на горение, количество и температуру продуктов
Определение расхода воздуха на горение, количество и температуру продуктов Применение здм к кислотно-основным равновесиям и их роль в аналитической химии
Применение здм к кислотно-основным равновесиям и их роль в аналитической химии Chemical Equilibrium. Topic 3.3
Chemical Equilibrium. Topic 3.3 Альдегиды и кетоны. Определение
Альдегиды и кетоны. Определение