Металлы Сu, Au, Ag не взаимодействуют с водой даже при нагревании.
Металлы
обладают электропроводностью и теплопроводностью.
Для металлов характерна металлическая кристаллическая решетка.
У атомов металлов на внешнем уровне 1-3 электрона.
У атомов металлов на внешнем уровне 1-3 электрона.
Металлы являются восстановителями и окислителями.
Для металлов характерна металлическая кристаллическая решетка.
Металлы обладают электропроводностью и теплопроводностью.
При взаимодействии с кислородом металлы принимают электроны.
Все металлы активно взаимодействуют с кислотами.
Металлы Сu, Au, Ag не взаимодействуют с водой даже при нагревании.
Мg, Be относятся к щелочноземельным металлам.
Убери лишнее о металлах



 Властивості та застосування полімерів
Властивості та застосування полімерів Техника безопасности в химической лаборатории и на уроках химии
Техника безопасности в химической лаборатории и на уроках химии Кондуктометрия. Кондуктометрия әдісі. Электрохимиялық әдістер
Кондуктометрия. Кондуктометрия әдісі. Электрохимиялық әдістер Применение центрифугирования
Применение центрифугирования Химические формулы. 8 класс
Химические формулы. 8 класс Оксиды. Химические свойства и получение оксидов
Оксиды. Химические свойства и получение оксидов Сплав золота и серебра - электрум
Сплав золота и серебра - электрум Углеводы. Моносахариды. Дисахариды. Полисахариды
Углеводы. Моносахариды. Дисахариды. Полисахариды Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды)
Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды) Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури
Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури Фосфор и его соединения
Фосфор и его соединения Дисперсные системы (продолжение)
Дисперсные системы (продолжение) Классификация и свойства природных энергоносителей
Классификация и свойства природных энергоносителей Оксиды и их классификация
Оксиды и их классификация Органическая химия
Органическая химия Органічні речовини в живій природі. Рівні структурної органшзації
Органічні речовини в живій природі. Рівні структурної органшзації Арены. Бензол и его гомологи
Арены. Бензол и его гомологи Экспертные системы распознавания химических веществ. Тест
Экспертные системы распознавания химических веществ. Тест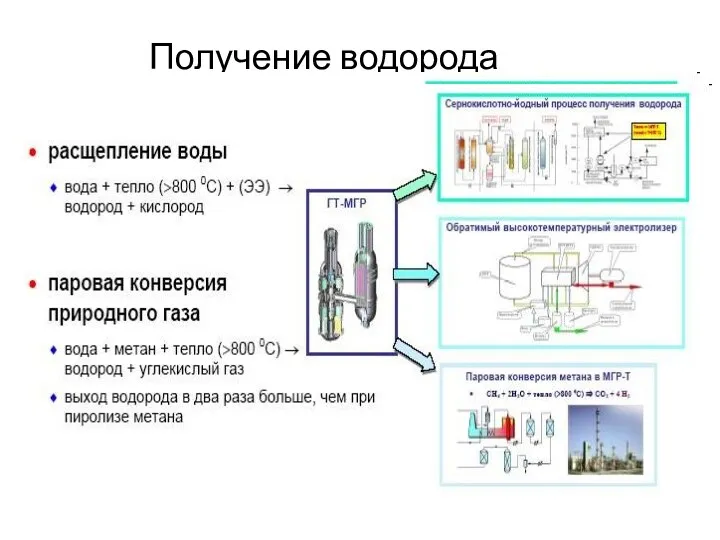 Получение водорода
Получение водорода Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Карбон қышқылдары
Карбон қышқылдары Решение задач на нахождение молекулярной формулы органических веществ
Решение задач на нахождение молекулярной формулы органических веществ Сутектік көрсеткіш ph. Тұздар гидролизі
Сутектік көрсеткіш ph. Тұздар гидролизі Пиролиз. Современная мировая структура сырья
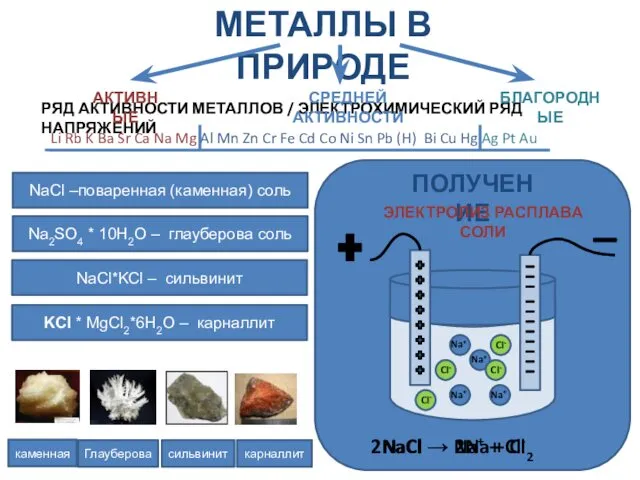
Пиролиз. Современная мировая структура сырья Нахождение металлов в природе. Общие способы получения металлов. 9 класс
Нахождение металлов в природе. Общие способы получения металлов. 9 класс Методы в химии
Методы в химии Бережём планету вместе. Нефть
Бережём планету вместе. Нефть Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии
Мицеллярные растворы ПАВ. Солюбилизация. Микроэмульсии