Слайд 2

Al
13
Алюминий
(лат. Aluminium)
3
8
2
26,9815
3s2 3p1
Был впервые получен датским физиком Х.К. Эрстедом в
1825 г. Название этого элемента происходит от латинского алюмен, так в древности назывались квасцы, которые использовали для крашения тканей. Латинское название, вероятно, восходит к греческому «халмэ» - рассол, соляной раствор.
Слайд 3

Al
13
Алюминий
(лат. Aluminium)
3
8
2
26,9815
3s2 3p1
Порядковый номер. Химический элемент III группы главной подгруппы
3-го периода.
Слайд 4

Al
13
Алюминий
(лат. Aluminium)
3
8
2
26,9815
3s2 3p1
Атомная масса элемента
Слайд 5
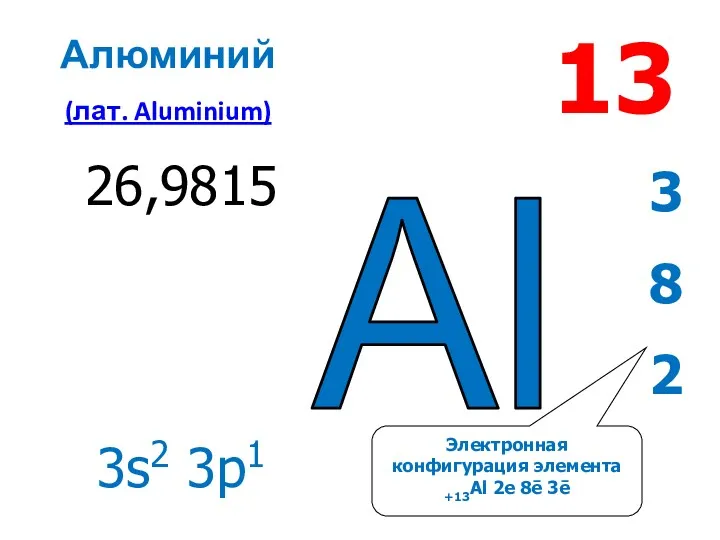
Al
13
Алюминий
(лат. Aluminium)
3
8
2
26,9815
3s2 3p1
Электронная конфигурация элемента +13Al 2е 8ē 3ē
Слайд 6
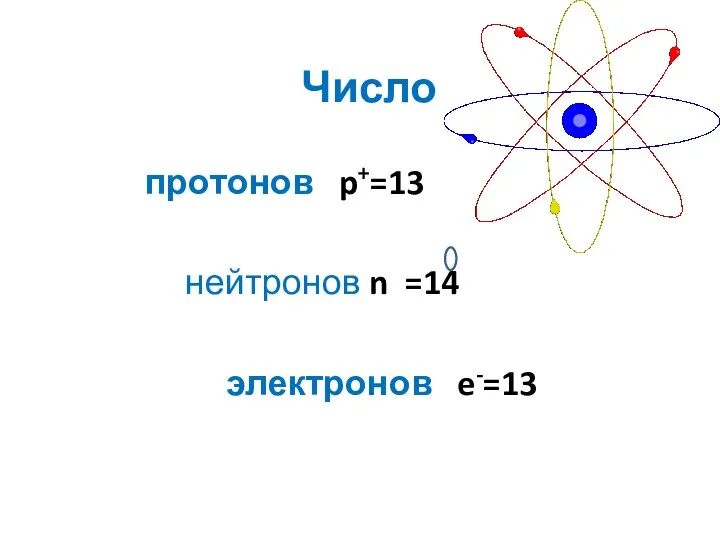
Число
протонов p+=13
нейтронов n =14
электронов e-=13
Слайд 7

ПРИРОДНЫЕ СОЕДИНЕНИЯ АЛЮМИНИЯ
АЛЮМОСИЛИКАТЫ
КОРУНД Al2O3 – прозрачные кристаллы
Слайд 8

Слайд 9

Алюминиевые руды (бокситы)
Слайд 10

Слайд 11

Слайд 12

Химические свойства алюминия
4Аl + 3O2 =
2Al + 3Br2 =
2Al + 3S
=
2Al + 6H2O =
2Al + 6HCl =
Al +CuSO4 =
2Al + 2NaOH + 6H2O=
Слайд 13

Химические свойства алюминия
4Аl + 3O2 = 2Al2O3
2Al + 3Br2 = 2AlBr3
2Al
+ 3S = Al2S3
2Al + 6H2O = 2Al(OH)3 + 3H2
2Al + 6HCl = 2AlCl3 + 3H2
2Al + 3CuSO4 =Al2 (SO4)3
2Al + 2NaOH + 6H2O=2Na[Al(OH)4]+3H2
Слайд 14
Слайд 15
Слайд 16

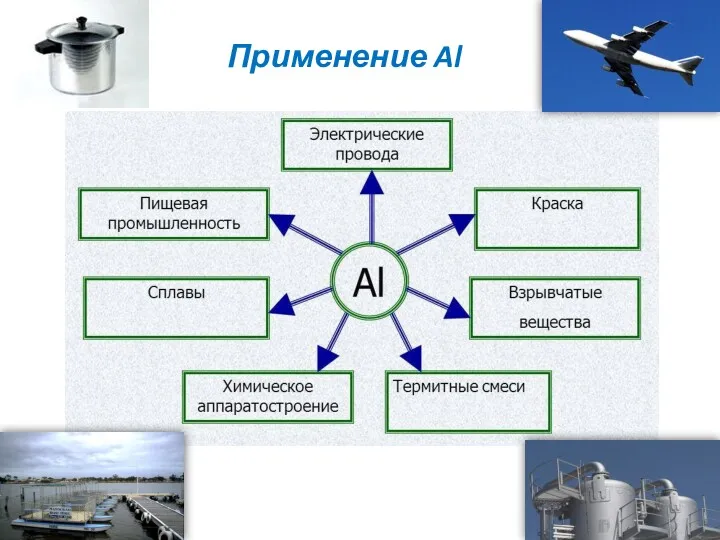
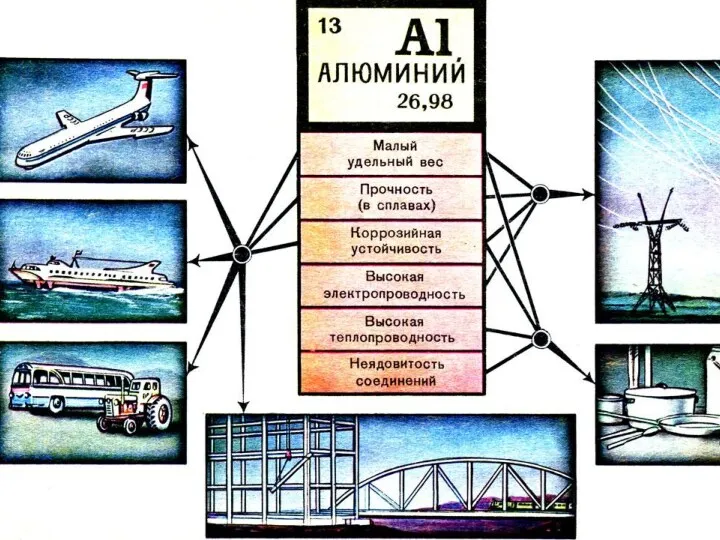
Алюминий и его сплавы широко применяют как конструкционный материал















 Химия в решении сырьевой проблемы
Химия в решении сырьевой проблемы Конструкционные материалы. Пластмассы
Конструкционные материалы. Пластмассы Классификация химических реакций
Классификация химических реакций Амінокислоти
Амінокислоти Электрохимические накопители энергии
Электрохимические накопители энергии Биохимия. Лекция 7. Углеводы
Биохимия. Лекция 7. Углеводы Кислоты. Яблочная кислота
Кислоты. Яблочная кислота Газы, применяемые при сварке
Газы, применяемые при сварке Марганец и его соединения
Марганец и его соединения Стан електронів у атомі
Стан електронів у атомі Значення хімічних процесів у природі
Значення хімічних процесів у природі Типы химических реакций
Типы химических реакций Алюминий и его соединения. Характеристика химического элемента: 3-й период, 3-я А подгруппа
Алюминий и его соединения. Характеристика химического элемента: 3-й период, 3-я А подгруппа Органическая химия. Лекция 13
Органическая химия. Лекция 13 Спектральные методы: атомная спектроскопия
Спектральные методы: атомная спектроскопия Свойства растворов и гетерогенных систем
Свойства растворов и гетерогенных систем Mechanistic insights into the aminolysis of 3,4-epoxysulfolane
Mechanistic insights into the aminolysis of 3,4-epoxysulfolane Презентация по химии по теме Решаем задачи Домашняя аптечка для 8, 9 класса
Презентация по химии по теме Решаем задачи Домашняя аптечка для 8, 9 класса Carbohydrates. Starch
Carbohydrates. Starch Техника безопасности на уроках химии
Техника безопасности на уроках химии Частицы вещества: молекула, атом, ион
Частицы вещества: молекула, атом, ион Понятие биогенности химических элементов
Понятие биогенности химических элементов Свинец и цинк в природе
Свинец и цинк в природе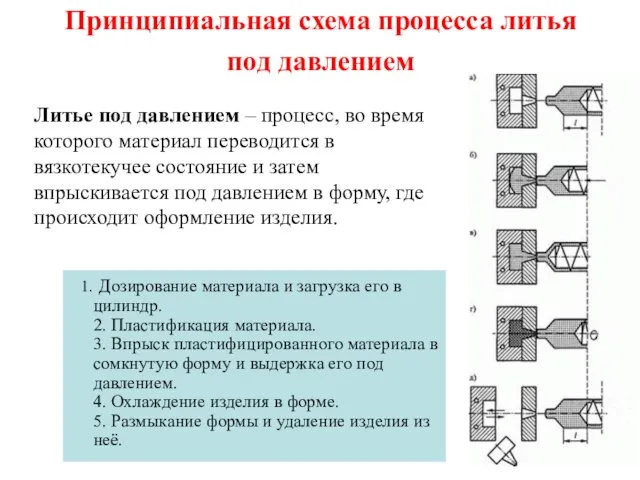 Принципиальная схема процесса литья под давлением
Принципиальная схема процесса литья под давлением Количественный анализ. Гравиметрия
Количественный анализ. Гравиметрия Чисті речовини та суміші. Способи розділення
Чисті речовини та суміші. Способи розділення Сполуки нітрогену з оксигеном
Сполуки нітрогену з оксигеном Carbohydrates and their metabolism. Digestion of carbohydrates
Carbohydrates and their metabolism. Digestion of carbohydrates