Содержание
- 2. Знать строение и свойства азотной кислоты и ее солей. Уметь составлять уравнения реакций, отражающие свойства этих
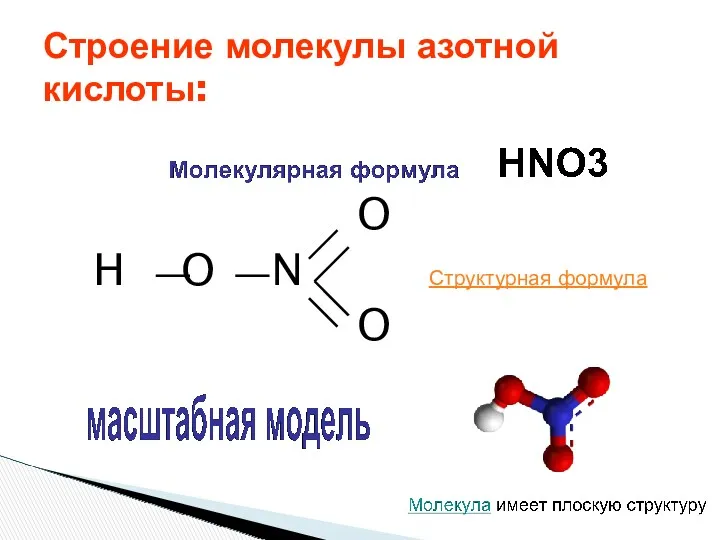
- 3. O H O N Структурная формула O Строение молекулы азотной кислоты:
- 4. Физические свойства Бесцветная, дымящаяся, неограниченно растворимая в воде жидкость, обладающая резким раздражающим запахом. t°пл.= -41°C; t°кип.=
- 5. Лабораторный способ: Действие конц. серной кислоты на кристаллические нитраты. Получение. KNO3 + H2SO4(конц) = KHSO4 +
- 6. Промышленный способ осуществляется в 3 этапа: Получение. 1) Окисление аммиака на платиновом катализаторе до NO 4NH3
- 7. ХИМИЧЕСКИЕ СВОЙСТВА - Общие с другими кислотами - - Специфические свойства
- 8. HNO3: Очень сильная кислота. Диссоциирует в водном растворе практически нацело. HNO3 = H++NO3- Общие химические свойства
- 9. 1. взаимодействует с основными и амфотерными оксидами. 2. взаимодействует с основаниями. 3. реагирует с солями (
- 10. Реагирует с основными и амфотерными оксидами CuO + 2HNO3 = Cu(NO3)2 + H2O CuO + 2H+
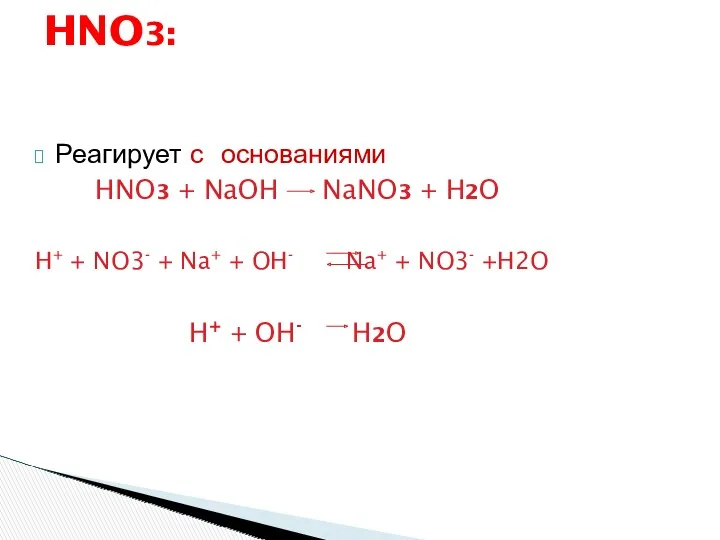
- 11. Реагирует с основаниями HNO3 + NaOH NaNO3 + H2O H+ + NO3- + Na+ + OH-
- 12. вытесняет слабые кислоты из их солей 2HNO3 + Na2CO3 2NaNO3 + H2O + CO2 2H+ +
- 13. Взаимодействие с металлами Взаимодействие с неметаллами Взаимодействие с органическими соединениями Разложение при нагревании Азотная кислота проявляет
- 14. При взаимодействии с металлами никогда не выделяется водород!! Специфические свойства азотной кислоты металл + HNO3 =
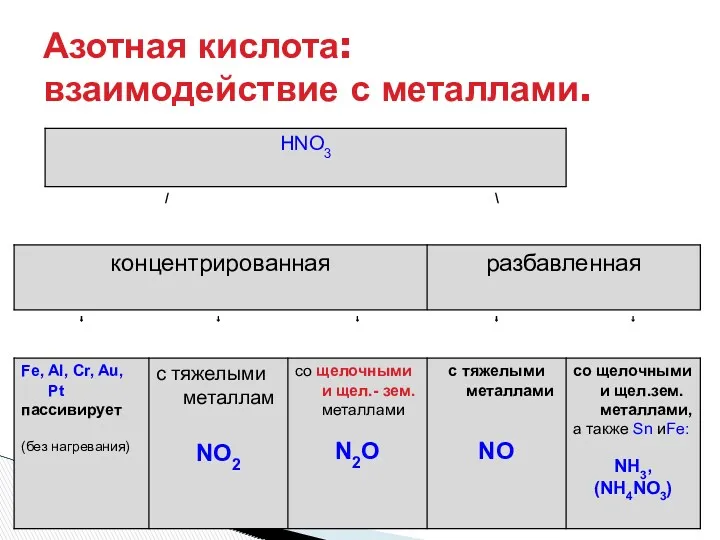
- 15. Азотная кислота: взаимодействие с металлами.
- 16. Большинство металлов реагируют с азотной кислотой с выделением азота или его оксидов в различных степенях окисления,
- 17. Азотная кислота превращается в NO (или в NO2); неметаллы окисляются до соответствующих кислот: HNO3 реагирует с
- 18. 1. Разлагается на свету и при нагревании: 4HNO3 = 2H2O + 4NO2 + O2 Азотная кислота
- 19. Окрашивает белки в желтый цвет ("ксантопротеиновая реакция") Реакции с органическими веществами:
- 20. Вещество + медные стружки + H2SO4(к.)+t0 NaNO3 + H2SO4(к.) = NaHSO4 + HNO3 4HNO3 + Cu
- 21. называются нитратами (селитрами) NaNO3 – нитрат натрия Cu(NO3)2 – нитрат меди(II) Соли азотной кислоты
- 22. 1) Нитраты щелочных металлов разлагаются до нитритов: 2NaNO3 = 2NaNO2 + O2 2) Нитраты менее активных
- 24. Скачать презентацию


















 Калийные удобрения
Калийные удобрения Мінерали та гірські породи
Мінерали та гірські породи Алкены. Строение алкенов, характерные типы химических реакций
Алкены. Строение алкенов, характерные типы химических реакций Железо. Нахождение в природе. Свойства железа
Железо. Нахождение в природе. Свойства железа Многоатомные спирты
Многоатомные спирты Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки
Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки Основные законы и понятия химии
Основные законы и понятия химии Экспериментально исследовательский проект Соль волшебница
Экспериментально исследовательский проект Соль волшебница Химия нефти и газа
Химия нефти и газа Транспортное обеспечение внесения удобрений
Транспортное обеспечение внесения удобрений Витамины. Ашылу тарихы
Витамины. Ашылу тарихы Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Комплексные соединения
Комплексные соединения Химический элементы в нашей жизни
Химический элементы в нашей жизни Валентность химических элементов
Валентность химических элементов Цинк и его соединения
Цинк и его соединения Золото. Виды золота
Золото. Виды золота Серная кислота и её свойства
Серная кислота и её свойства Классификация и свойства оксидов
Классификация и свойства оксидов Минерал лазурит. Месторождения
Минерал лазурит. Месторождения Альдегидтер мен спирттер
Альдегидтер мен спирттер Легированные стали
Легированные стали Общие понятия неорганической химии. Химические свойства основных классов неорганических веществ. Лекция 3
Общие понятия неорганической химии. Химические свойства основных классов неорганических веществ. Лекция 3 Технологии создания и обработки кристаллических материалов
Технологии создания и обработки кристаллических материалов Фосфор и его соединения. 9 класс
Фосфор и его соединения. 9 класс Инструменты и приспособления для химической завивки волос
Инструменты и приспособления для химической завивки волос Общая электронная теория восстановления и окисления металлов
Общая электронная теория восстановления и окисления металлов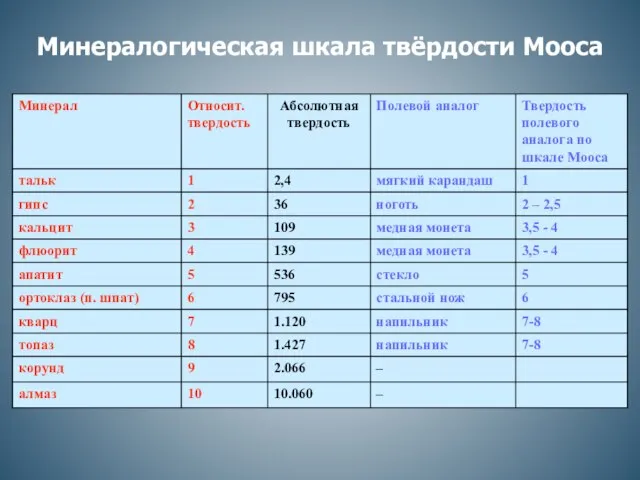 Минералогическая шкала твёрдости Мооса
Минералогическая шкала твёрдости Мооса