Содержание
- 2. Дисперсными называют гетерогенные системы , в которых одно вещество в виде очень мелких частиц равномерно распределено
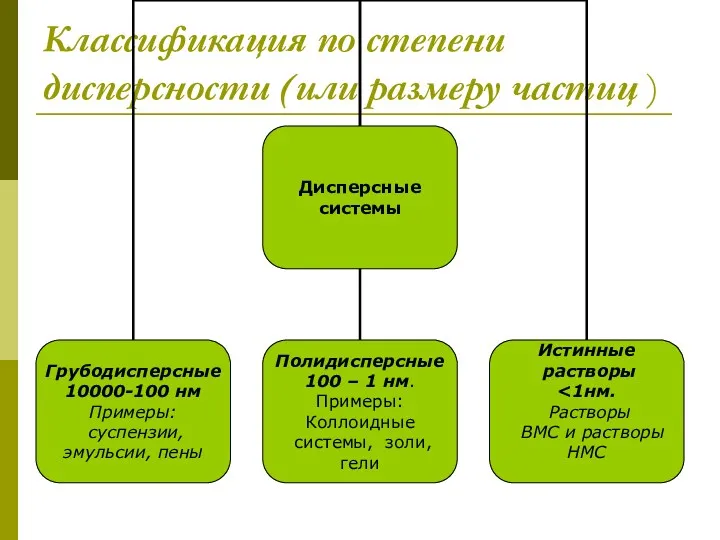
- 3. Классификация по степени дисперсности (или размеру частиц )
- 4. Суспензии – это грубодисперсные системы, в которых дисперсная фаза состоит из твердых частиц, взвешенных в жидкой
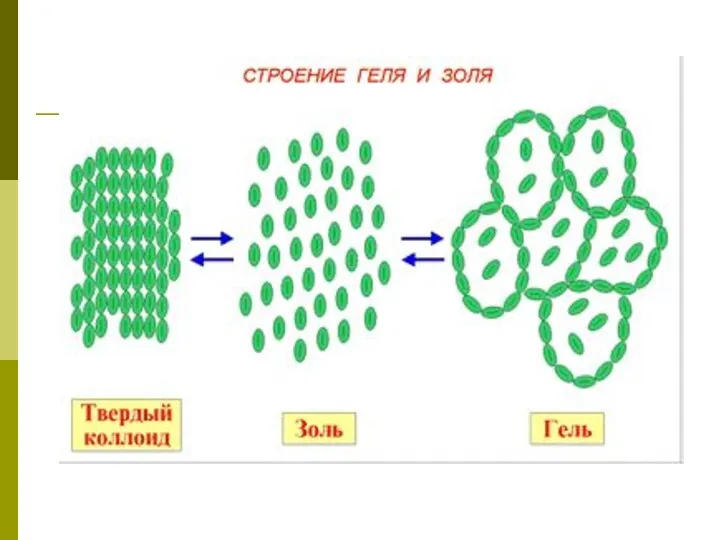
- 5. Коллоидные системы- это такие дисперсные системы, в которых размер частиц фазы от 100 до 1 нм
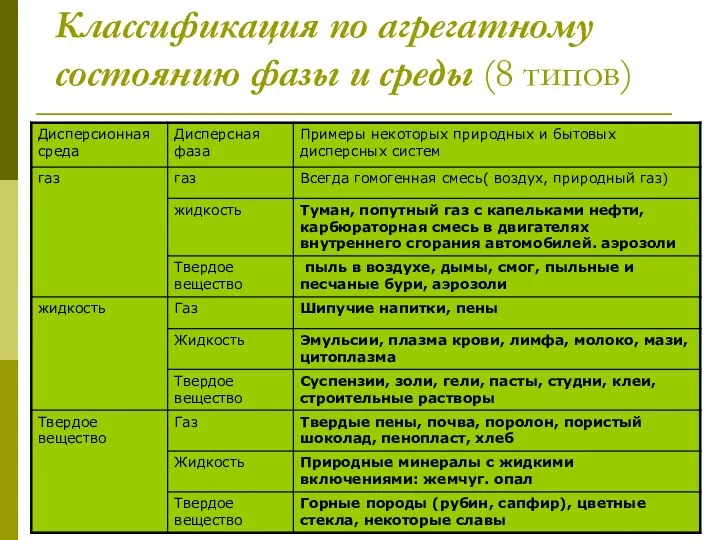
- 7. Классификация по агрегатному состоянию фазы и среды (8 типов)
- 8. Дисперсионные методы получения коллоидных систем механические – дробление, растирание, размол и т. д.; электрический – получение
- 9. Конденсационные методы физические: резкое охлаждение (образование тумана); замена лучшего растворителя на худший (раствор мыла в спирте
- 10. Химические способы проведение таких химических реакций, как окисление: 2H2S + O2 → 2H2O + 2S (золь
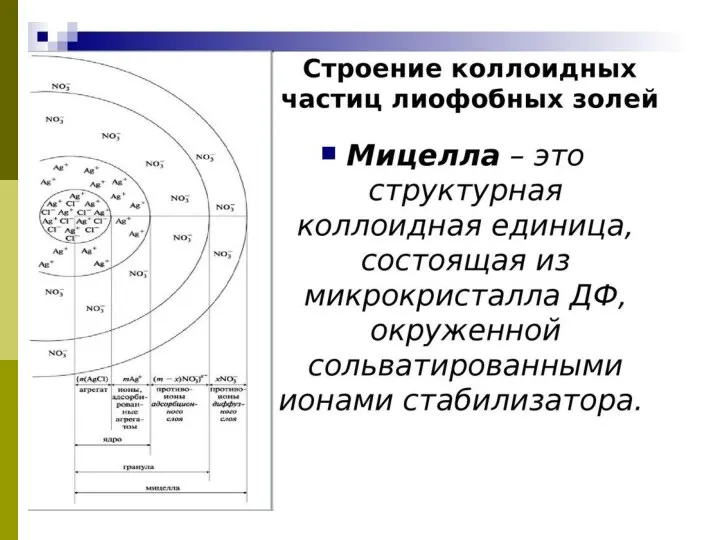
- 11. Теория Думанского и Пескова Коллоидный раствор состоит из мицелл (твердая или дисперсная фаза) и Интермицеллярной жидкости,
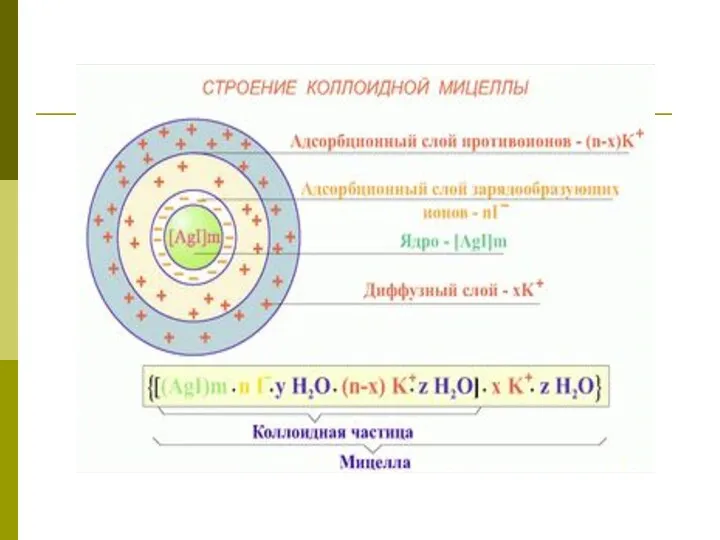
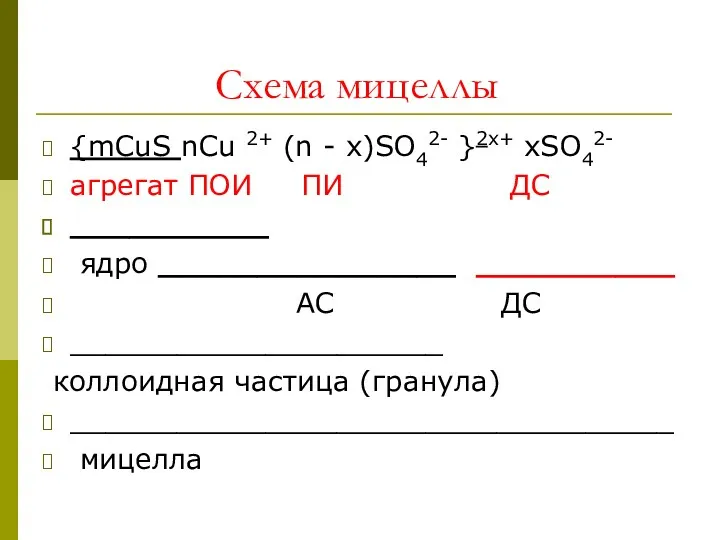
- 14. Схема мицеллы {mCuS nCu 2+ (n - х)SO42- }2х+ хSO42- агрегат ПОИ ПИ ДС __________ ядро
- 15. (mCuS) –это агрегат, на поверхности которого, согласно правилу Фаянса-Пескова: Из дисперсионной среды адсорбируются те ионы стабилизатора
- 16. Затем адсорбируются противоионы (ПИ), в данном случае SO42- в количестве (n – х). Ядро и ПИ
- 17. Устойчивость коллоидных растворов. Агрегативная устойчивость - сохранение размеров частиц. Седиментационная устойчивость – равномерное распределение частиц по
- 18. Правило Шульце-Гарди: коагуляцию коллоидных растворов вызывает не весь электролит, а только тот его ион, который противоположен
- 19. Коллоидные растворы в природе и технике. В природной воде содержится часть примесей в коллоидном состоянии. Поэтому
- 20. Применение Можно разделить коллоидные частицы и ионы через мембрану, проницаемую для молекул и ионов и непроницаемую
- 22. Скачать презентацию













 Углекислый газ СО2
Углекислый газ СО2 Методы хроматографии. Ионообменная хроматография
Методы хроматографии. Ионообменная хроматография Спирти
Спирти Енергетичний стан поверхні. Сорбційні явища. Мезопористі матеріали
Енергетичний стан поверхні. Сорбційні явища. Мезопористі матеріали Основи, їх склад, назви, класифікація
Основи, їх склад, назви, класифікація Зависят ли свойства предельных одноатомных спиртов от их химического строения?
Зависят ли свойства предельных одноатомных спиртов от их химического строения? Фосфор
Фосфор Кислород O2
Кислород O2 Жесткость воды
Жесткость воды Азотная кислота
Азотная кислота Всероссийская олимпиада школьников по химии (региональный этап). Разбор заданий, 9 класс
Всероссийская олимпиада школьников по химии (региональный этап). Разбор заданий, 9 класс Непредельные углеводороды: этилен
Непредельные углеводороды: этилен Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду
Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду Гниение. Брожение
Гниение. Брожение Теория кристаллического поля
Теория кристаллического поля Вещества и их свойства
Вещества и их свойства Азотные удобрения
Азотные удобрения Непредельные углеводороды
Непредельные углеводороды Теория электрической диссоциации
Теория электрической диссоциации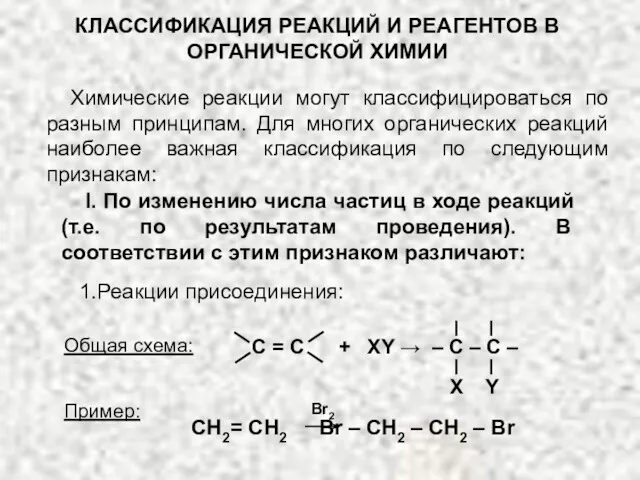 Классификация реакций и реагентов органической химии
Классификация реакций и реагентов органической химии Бор шикізатын қышқылдық ыдырату
Бор шикізатын қышқылдық ыдырату Органолептические и визуальные методы идентификация полимера
Органолептические и визуальные методы идентификация полимера Аминокислоты. Физические свойства
Аминокислоты. Физические свойства Введение в химическую технологию топлив и углеродных материалов
Введение в химическую технологию топлив и углеродных материалов Основания. Неорганические соединения
Основания. Неорганические соединения Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов
Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов Формы минералов и их агрегатов
Формы минералов и их агрегатов Основи. Властивості, застосування гідроксидів Натрію і Калію
Основи. Властивості, застосування гідроксидів Натрію і Калію