Слайд 2

Термодинамика
Наука о взаимных превращениях различных видов энергии.
Термодинамика устанавливает законы этих
превращений, а также направление самопроизвольного, течения различных процессов в данных условиях.
Слайд 3

При химических реакциях происходят глубокие качественные изменения в системе, рвутся связи
в исходных веществах и возникают новые связи в конечных продуктах. Эти изменения сопровождаются поглощением или выделением энергии. В большинстве случаев этой энергией является теплота. Реакции, которые сопровождаются выделением теплоты, называют экзотермическими, а те, которые сопровождаются поглощением теплоты, – эндотермическими.
Слайд 4
При химических реакциях происходят глубокие качественные изменения в системе, рвутся связи
в исходных веществах и возникают новые связи в конечных продуктах.
2Н2(г) + О2 = 2Н2О(ж) + 285,84 кДж
Слайд 5

При любом процессе соблюдается закон сохранения энергии как проявление более общего
закона природы – закона сохранения материи. Теплота Q, поглощенная системой, идет на изменение ее внутренней энергии Δ U и на совершение работы A:
Q = ΔU + A
Слайд 6

Внутренняя энергия системы U – это общий ее запас, включающий энергию
поступательного и вращательного движения молекул, энергию внутримолекулярных колебаний атомов и атомных групп, энергию движения электронов, внутриядерную энергию и т.д. Внутренняя энергия – полная энергия системы без потенциальной энергии, обусловленной положением системы в пространстве, и без кинетической энергии системы как целого.
Слайд 7

Изохорный процесс
При химических реакциях А – это работа против внешнего давления,
т.е. в первом приближении
А = pΔV,
где ΔV – изменение объема системы (V2 – V1).
При изохорном процессе (V-const):
(V2 – V1)=0, тогда А=0; теплота
QV = ΔU + 0,
QV = (U2 – U1) = ΔU
Слайд 8

Изобарный процесс
(p-const) теплота
Qp = ΔU + pΔV,
Qp = (U2 – U1)
+ p(V2 – V1);
Qp = (U2 + pV2) – (U1 + pV1).
Сумма U + pV обозначим через Н, тогда:
Qp = Н2 – Н1 = ΔН.
Слайд 9

Величину Н называют энтальпией. Таким образом, теплота при p=const и T=const
приобретает свойство функции состояния и не зависит от пути, по которому протекает процесс. Отсюда теплота реакции в изобарно-изотермическом процессе Qр равна изменению энтальпии системы ΔН (если единственным видом работы является работа расширения):
Qp = ΔН.
Слайд 10

Энтальпия, как и внутренняя энергия, является функцией состояния; ее изменение (ΔН)
определяется только начальными и конечными состояниями системы и не зависит от пути перехода. Нетрудно видеть, что теплота реакции в изохорно-изотермическом процессе (V=const; T=const), при котором ΔV = 0, равна изменению внутренней энергии системы:
QV = ΔU
Слайд 11
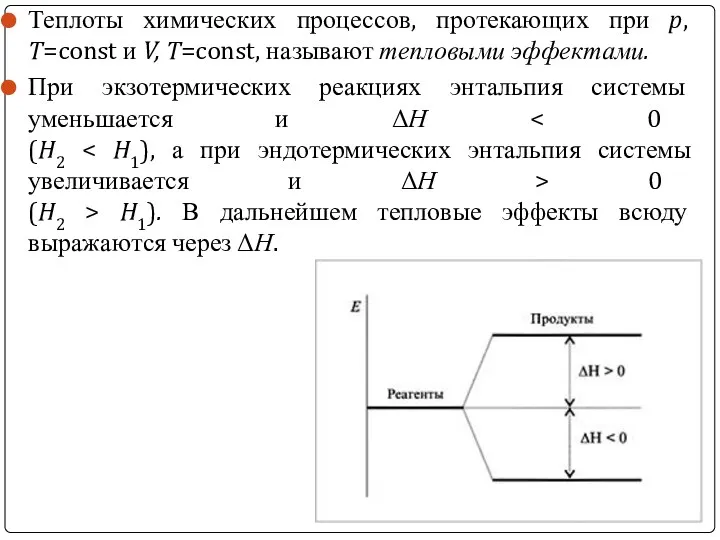
Теплоты химических процессов, протекающих при p, T=const и V, T=const, называют
тепловыми эффектами.
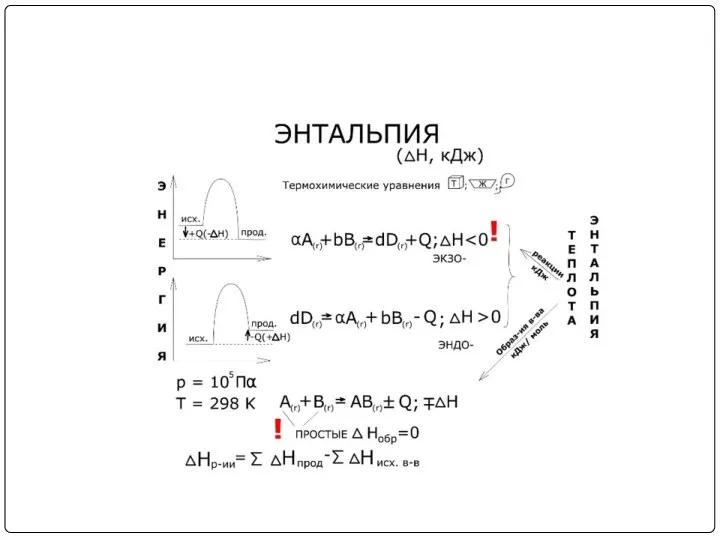
При экзотермических реакциях энтальпия системы уменьшается и ΔН < 0
(H2 < H1), а при эндотермических энтальпия системы увеличивается и ΔН > 0
(H2 > H1). В дальнейшем тепловые эффекты всюду выражаются через ΔН.
Слайд 12
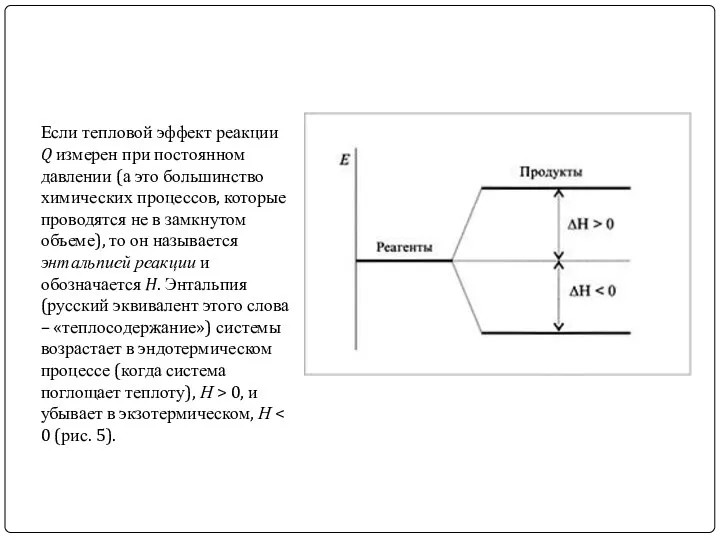
Если тепловой эффект реакции Q измерен при постоянном давлении (а это
большинство химических процессов, которые проводятся не в замкнутом объеме), то он называется энтальпией реакции и обозначается H. Энтальпия (русский эквивалент этого слова – «теплосодержание») системы возрастает в эндотермическом процессе (когда система поглощает теплоту), Н > 0, и убывает в экзотермическом, Н < 0 (рис. 5).
Слайд 13
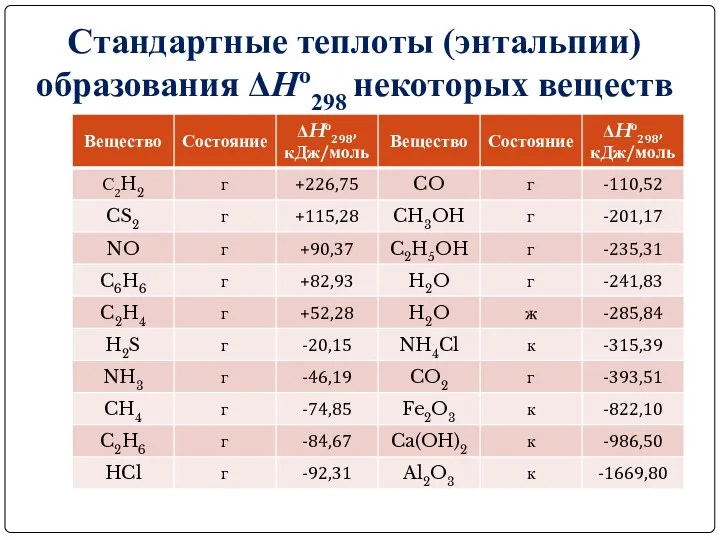
Стандартные теплоты (энтальпии) образования ΔHо298 некоторых веществ
Слайд 14

Часто в термохимических расчетах применяют следствие из закона Гесса: тепловой эффект
реакции (ΔHх.р.) равен сумме теплот образования ΔHобр продуктов реакции за вычетом суммы теплот образования исходных веществ с учетом коэффициентов перед формулами этих веществ в уравнении реакции
Слайд 15
Слайд 16

Энтальпии очень многих реакций найдены экспериментально, часто с использованием калориметров. Однако
это осуществлено далеко не для всех процессов. Во-первых, их слишком много, возможно, практически бесконечное число. Во-вторых, отнюдь не все реакции можно провести в калориметре, например реакцию, происходящую в зеленых растениях:
Слайд 17

Энтальпией образования вещества fH называется энтальпия реакции образования 1 моль этого
вещества из соответствующих простых веществ.
















 Производство ацетальдегида
Производство ацетальдегида Коррозия металлов
Коррозия металлов Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Титриметрический анализ
Титриметрический анализ O-alkylation catalysts
O-alkylation catalysts Титриметрические методы количественного определения лекарственных веществ
Титриметрические методы количественного определения лекарственных веществ Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау
Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау Алкени i Алкіни. Загальна та молекулярні формули, структурна ізомерія, систематична номенклатура
Алкени i Алкіни. Загальна та молекулярні формули, структурна ізомерія, систематична номенклатура Number of molecues with a particular energy
Number of molecues with a particular energy Предельные углеводороды. Алканы
Предельные углеводороды. Алканы Общая характеристика липидов. Строение. Классификация. Функции. Переваривание и всасывание липидов в ЖКТ Роль желчи
Общая характеристика липидов. Строение. Классификация. Функции. Переваривание и всасывание липидов в ЖКТ Роль желчи Химия и современный быт человека
Химия и современный быт человека Понятие об алкинах
Понятие об алкинах Витамины. Ашылу тарихы
Витамины. Ашылу тарихы Токсикология пестицидов
Токсикология пестицидов Органическая химия
Органическая химия Валентные возможности атомов химических элементов
Валентные возможности атомов химических элементов Получение уксусной кислоты и опыты с ней
Получение уксусной кислоты и опыты с ней Теоретическая электрохимия
Теоретическая электрохимия Строение и свойства материалов. Тема 1.1
Строение и свойства материалов. Тема 1.1 Одноатомные спирты
Одноатомные спирты Кремний и его соединения
Кремний и его соединения Титанның химиялық элементі
Титанның химиялық элементі Anionic Polymerization
Anionic Polymerization Хромотография, явления, атомы и молекулы. 8 класс
Хромотография, явления, атомы и молекулы. 8 класс Трансмиссионные масла
Трансмиссионные масла Общая химия
Общая химия Кристаллические решетки
Кристаллические решетки