Содержание
- 3. ЗАКОН АВОГАДРО В равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул.
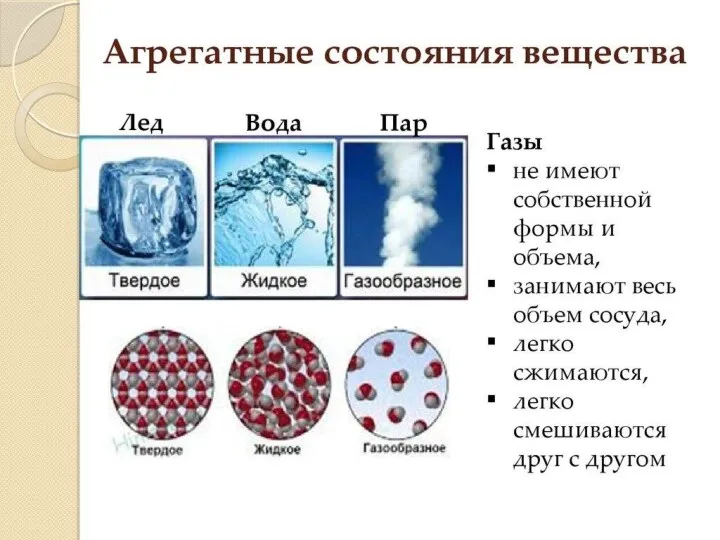
- 4. Газы не имеют собственное формы и объема. Они занимают весь объем сосуда, в котором находятся. Газы
- 5. Важнейшими природными газами являются воздух и природный газ.
- 6. Состав воздуха складывался миллионы лет благодаря фотосинтезу, осуществляемому растениями. В то время как природный газ сформировался
- 7. ОПАСНОСТЬ!!!!!!!!!!!!!!!!$ При смешивании природных газов может произойти катастрофа (кабум), что не редко происходит при несоблюдении правил
- 8. ТЕХНИКА БЕЗОПАСНОСТИ При ощущении малейшего запаха газа необходимо проветрить помещение, не включать электроприборы, избегать любого огня
- 9. ВОДОРОД (H2) – САМЫЙ ЛЕГКИЙ ГАЗ Использование -Производство аммиака. -Получение маргарина. -Водородная резка и сварка металлов.
- 10. АППАРАТ КИППА
- 11. КИСЛОРОД -— ЭЛЕМЕНТ 16-Й ГРУППЫ, ВТОРОГО ПЕРИОДА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА, С АТОМНЫМ
- 12. Состав атмосферы может изменятся в результате антропогенного загрязнения.
- 13. Парниковый эффект — повышение температуры нижних слоёв атмосферы планеты по сравнению с эффективной температурой, то есть
- 14. В лаборатории кислород получают разложением перманганата калия 2 KMnO4 = K2MnO4 + MnO2 + O2 ↑
- 15. УГЛЕКИСЛЫЙ ГАЗ (CO2) Использование -Изготовление шипучих напитков. -Тушение пожаров. -Изготовление (сухого) льда
- 16. В ПРОМЫШЛЕННОСТИ ПОЛУЧАЮТ. Обжиг известняка.
- 17. В лаборатории оксид углерода(IV) получает действием соляной кислоты на мрамор.
- 18. Распознать углекислый газ можно с помощью горящей лучинки, которая гаснет в его атмосфере, или по помутнению
- 19. АММИАК(NH3)-БЕСЦВЕТНЫЙ ГАЗ С ЕДКИМ ЗАПАХОМ, СОЕДИНЕНИЕ АЗОТА С ВОДОРОДОМ. Лабораторный способ получения аммиака.
- 20. Природный газ служит сырьем для получения ценных газообразных органических соединений, например: этилен. Этилен. В промышленности получают
- 21. ПОЛУЧЕНИЕ ЭТИЛЕНА В ЛАБОРАТОРИИ.
- 22. 1-Деполимеризация полиэтилена. 2-Дегидратация этилового спирта.
- 24. Скачать презентацию



















 Оптические свойства и методы исследования дисперсных систем. Лекция 16
Оптические свойства и методы исследования дисперсных систем. Лекция 16 Классификация моторных масел
Классификация моторных масел Водород. Свойства водорода
Водород. Свойства водорода Растворы. Часть 2. Лекция №7
Растворы. Часть 2. Лекция №7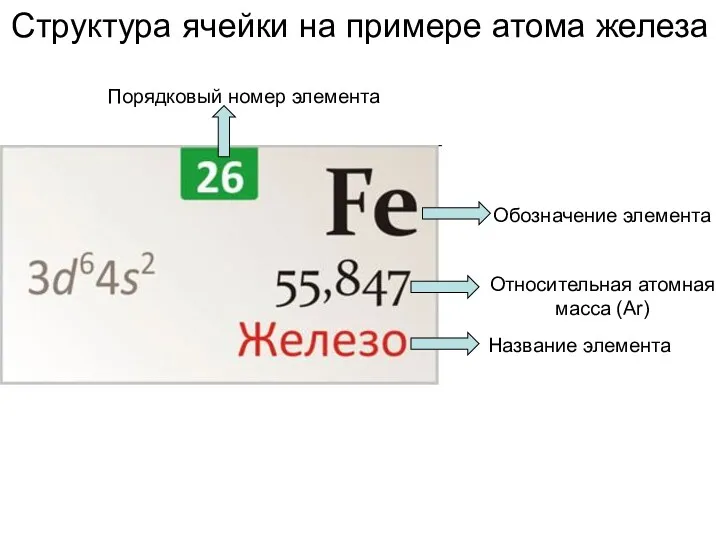 Структура ячейки на примере атома железа
Структура ячейки на примере атома железа Производство азотной кислоты
Производство азотной кислоты Теорія хімічної будови органічних сполук О.М. Бутлерова. Теорія, як вища форма наукових знань
Теорія хімічної будови органічних сполук О.М. Бутлерова. Теорія, як вища форма наукових знань ТЕРМОДИНАМИКА БИОЛОГИЧЕСКИХ СИСТЕМ
ТЕРМОДИНАМИКА БИОЛОГИЧЕСКИХ СИСТЕМ Химия радиоактивных элементов
Химия радиоактивных элементов Milk Composition. Proteins - Молоко
Milk Composition. Proteins - Молоко 20231104_prezentatsiya_teoriya_elektroliticheskoy_dissotsiatsii
20231104_prezentatsiya_teoriya_elektroliticheskoy_dissotsiatsii Основні технологічні процеси очистки води. Знезараження води. Знезараження води хлором
Основні технологічні процеси очистки води. Знезараження води. Знезараження води хлором Тепловой эффект химической реакции
Тепловой эффект химической реакции Классификация, строение и номенклатура органически. Предмет органической химии
Классификация, строение и номенклатура органически. Предмет органической химии Коррозия и методы борьбы с ней
Коррозия и методы борьбы с ней Катализ. Классификация каталитических процессов. Механизм действия катализаторов
Катализ. Классификация каталитических процессов. Механизм действия катализаторов Понятия про синтетические лекарственные средства
Понятия про синтетические лекарственные средства Строение электронных оболочек атомов
Строение электронных оболочек атомов Матеріальний баланс процесу горіння
Матеріальний баланс процесу горіння Липиды. Структурные компоненты липидов
Липиды. Структурные компоненты липидов Биохимия нуклеиновых кислот
Биохимия нуклеиновых кислот Количество вещества. 8 класс
Количество вещества. 8 класс Воздушные вяжущие вещества. Гипсоангидритовые вяжущие вещества. Основы процессов схватывания и твердения. (Лекция 1)
Воздушные вяжущие вещества. Гипсоангидритовые вяжущие вещества. Основы процессов схватывания и твердения. (Лекция 1) Методика преподавания химии
Методика преподавания химии Решение упражнений по теме: Углеводы
Решение упражнений по теме: Углеводы Введение в аналитическую химию. Введение в качественный анализ
Введение в аналитическую химию. Введение в качественный анализ Производство серы из природного газа и продукты на ее основе
Производство серы из природного газа и продукты на ее основе Генетическая связь
Генетическая связь