Содержание
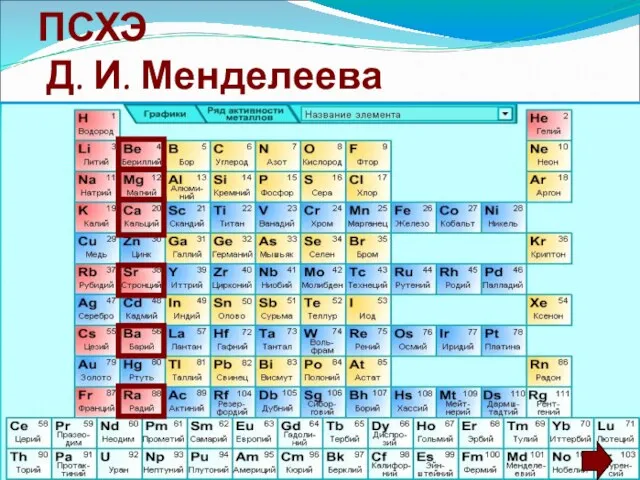
- 2. Положение элементов в ПСХЭ Д. И. Менделеева
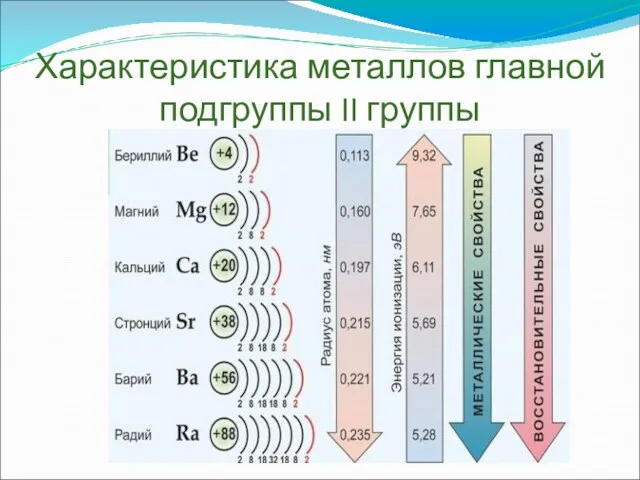
- 3. Характеристика металлов главной подгруппы II группы
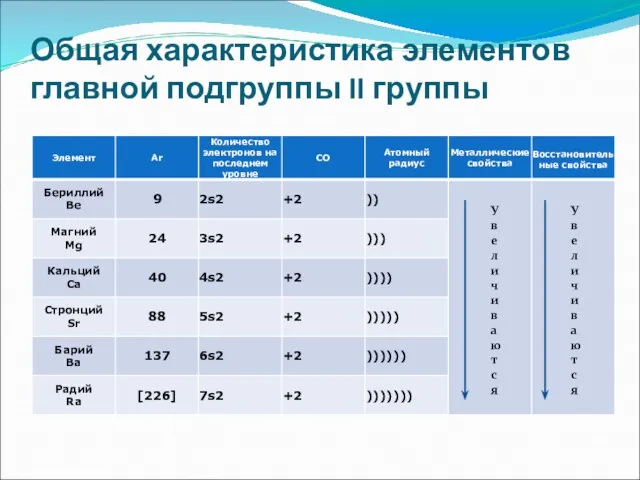
- 4. Общая характеристика элементов главной подгруппы II группы У в е л и ч и в а
- 5. Общая характеристика элементов главной подгруппы II группы Одинаковое строение внешнего электронного слоя Элементы проявляют С.О. +2
- 6. Ве - амфотерный металл, Mg – металл, Сa, Sr,Ba - щёлочноземельные металлы Ra –радиоактивный элемент
- 8. Получение щелочноземельных металлов Термическое восстановление их соединений: Be Cl2 + Mg = Be + MgCl2 MgO
- 9. Электролиз расплавов и рстворов галогенидов CuSO4 ⇄ Cu2+ + SO42- K(-): Cu2+ + 2e → Cu0
- 10. Химические свойства Щелочноземельные элементы - химически активные металлы. Они являются сильными восстановителями. Из металлов этой подгруппы
- 11. Взаимодействие с простыми веществами Все легко взаимодействуют с кислородом и серой: 2Be + O2 = 2BeO
- 12. Химические свойства элементов II группы главной подгруппы
- 13. Взаимодействие с водой Бериллий с водой не реагирует, магний реагирует медленно, остальные металлы реагируют с водой,
- 14. Взаимодействие с кислотами Все взаимодействуют с хлороводородной и разбавленной серной кислотами с выделением водорода: Be +
- 15. Взаимодействие со щелочами Бериллий взаимодействует с водными растворами щелочей с образованием комплексной соли и выделением водорода:
- 16. Кислородные соединения - оксиды BeO – амфотерный оксид MgO CaO SrO Основные оксиды BaO Оксид кальция
- 17. ВеО В природе оксид бериллия встречается в виде минерала бромеллита. Получают оксид бериллия термическим разложение гидроксида
- 18. Химические свойства ВеО Реакционная способность оксида бериллия зависит от способа его получения. Прокаленный при температуре не
- 19. MgO белые кристаллы, нерастворимые в воде, На этом свойстве основано его применение в спортивной гимнастике, нанесенный
- 20. Химические свойства Реагирует с разбавленными кислотами с образованием солей MgO + 2HCl → MgCl2 + H2O
- 21. Взаимодействие оксида кальция с водой ( гашение извести) CaO + H2O → Ca(OH)2 + Q
- 22. Химические свойства гидроксидов Ве(ОН)2 – амфотерный гидроксид Mg(OH)2 – нерастворимое основание Ca(OH)2 Sr(OH)2 Ba(OH)2 Растворимые основания
- 23. Химические свойства Be(OH)2 Взаимодействие с щелочами с образованием соли: Be(OH)2 + 2NaOH ⟶ Na2Be(OH)4 Взаимодействие с
- 24. Взаимодействие гидроксидов с кислотами Ca(OH)2+2HCl=CaCl2+2H2O Mg(OH)2+2HCl=MgCl2+2H2O
- 27. Жесткость воды Карбонатная, или временная Некарбонатная, или постоянная Общая жесткость Общая жесткость воды – это сумма
- 28. Карбонатная, или временная жесткость Обусловлена присутствием гидрокарбонатов кальция и магния. Её можно устранить: 1. Кипячением Ca(HCO3)2
- 29. Некарбонатная, или постоянная жесткость Обусловлена присутствием сульфатов и хлоридов кальция и магния. Её можно устранить действием
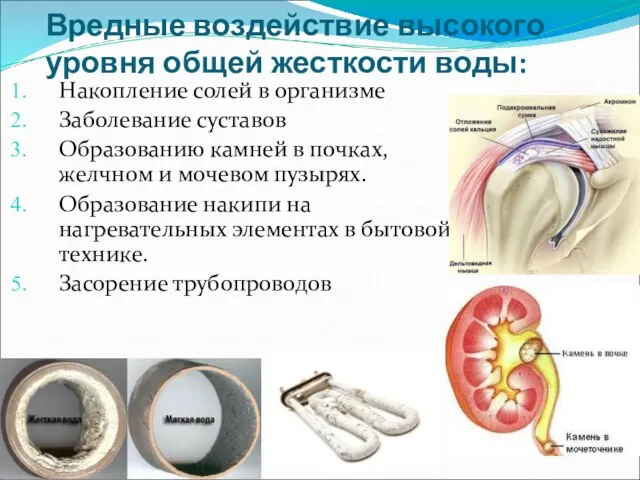
- 30. Вредные воздействие высокого уровня общей жесткости воды: Накопление солей в организме Заболевание суставов Образованию камней в
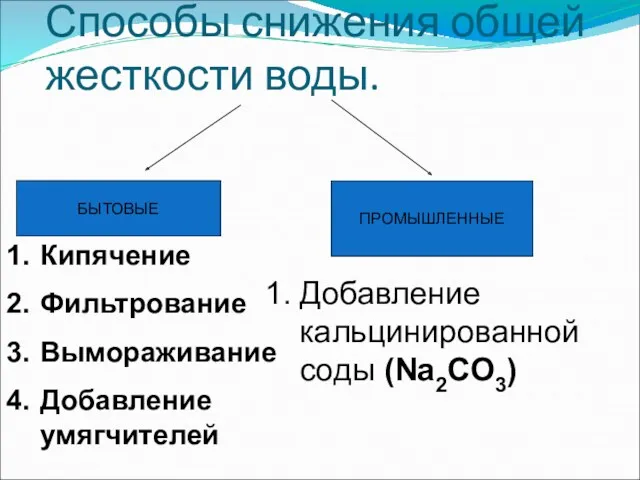
- 31. Способы снижения общей жесткости воды. БЫТОВЫЕ ПРОМЫШЛЕННЫЕ Кипячение Фильтрование Вымораживание Добавление умягчителей Добавление кальцинированной соды (Na2CO3)
- 32. Кипячение Снижение жесткости примерно на 30 - 40%
- 33. Вымораживание Вымораживание снижает общую жесткость на 70-80%
- 34. Фильтрование Фильтрование воды бытовым фильтром «Барьер-6» снижает общую жесткость до 80%.
- 35. Выполнить превращение: Ca→CaH2→Ca(OH)2→ CaCO3→CaO→CaCl2→ Ca3(PO4)2
- 36. Задание №1 Что представляет собой изотонический раствор? Почему его называют изотоническим? Рассчитать, сколько граммов соли необходимо
- 38. Скачать презентацию






























 Активационный анализ
Активационный анализ Рекомендации по использованию пластмасс в быту. Опасные типы пластмасс
Рекомендации по использованию пластмасс в быту. Опасные типы пластмасс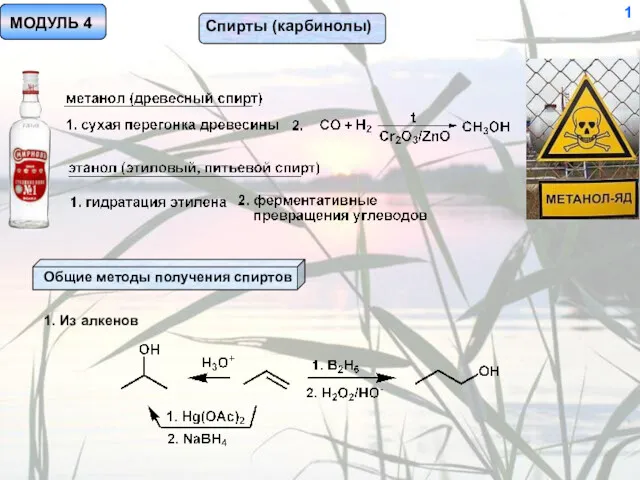 Спирты (карбинолы)
Спирты (карбинолы) Арены - ароматические соединения
Арены - ароматические соединения Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия
Контрольная работа по дисциплине Физическая химия. Раздел: Электрохимия Алкины (ацетиленовые углеводороды)
Алкины (ацетиленовые углеводороды) Введение в неорганическую химию. Классификация неорганических соединений
Введение в неорганическую химию. Классификация неорганических соединений Закономерности изменения свойств элементов в периодах и группах. Химия. 8 класс
Закономерности изменения свойств элементов в периодах и группах. Химия. 8 класс Железо. Характеристика химического элемента железа по его положению в ПСХЭ и строению атома
Железо. Характеристика химического элемента железа по его положению в ПСХЭ и строению атома Липиды (Жиры)
Липиды (Жиры) Химическая промышленность. 9 класс
Химическая промышленность. 9 класс Химическое вещество
Химическое вещество Кислород. Общая характеристика и нахождение в природе. 8 класс
Кислород. Общая характеристика и нахождение в природе. 8 класс Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение
Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение Метаморфические горные породы
Метаморфические горные породы Исследовательская работа на тему: Удивительные свойства воды
Исследовательская работа на тему: Удивительные свойства воды Вода – это жизнь!
Вода – это жизнь! Турнир Наследники Менделеева. Отборочный тур
Турнир Наследники Менделеева. Отборочный тур Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10)
Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10) Заключительный урок в 8 классе Тест по химии.
Заключительный урок в 8 классе Тест по химии. Аминокислоты, их строение, изомерия, свойства, применение
Аминокислоты, их строение, изомерия, свойства, применение Дисперсные системы. Растворы
Дисперсные системы. Растворы Теория диаграмм состояния
Теория диаграмм состояния ПРОСТЫЕ ВЕЩЕСТВА -НЕМЕТАЛЛЫ
ПРОСТЫЕ ВЕЩЕСТВА -НЕМЕТАЛЛЫ Периодический закон и периодическая система химических элементов
Периодический закон и периодическая система химических элементов Тұндыру әдістері
Тұндыру әдістері Углеводы. Сn(H2O)m – общая формула углеводов
Углеводы. Сn(H2O)m – общая формула углеводов Хімічні явища в побуті
Хімічні явища в побуті