Содержание
- 2. 1. Основные понятия и представления Термодинамика изучает только состояния систем, она не прослеживает подробно путь реакции,
- 3. Основные понятия химической кинетики Химическая кинетика – наука, изучающая скорости и механизмы химических процессов, а также
- 4. Химическая кинетика Исследование количественных закономерностей развития биологических процессов во времени на молекулярном уровне Химическая кинетика -
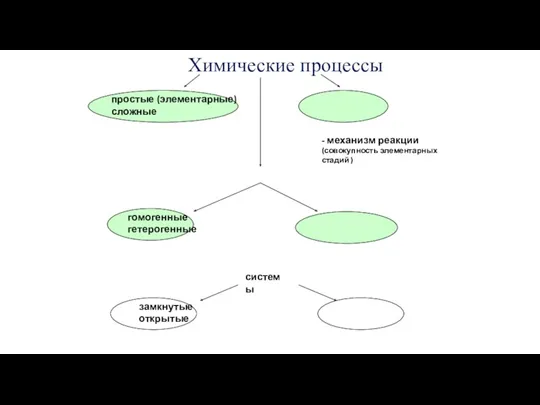
- 5. простые (элементарные) сложные Химические процессы - механизм реакции (совокупность элементарных стадий ) гомогенные гетерогенные замкнутые открытые
- 8. Скорость химической реакции V = const Элементарная реакция: w = число элементарных актов реакции в единице
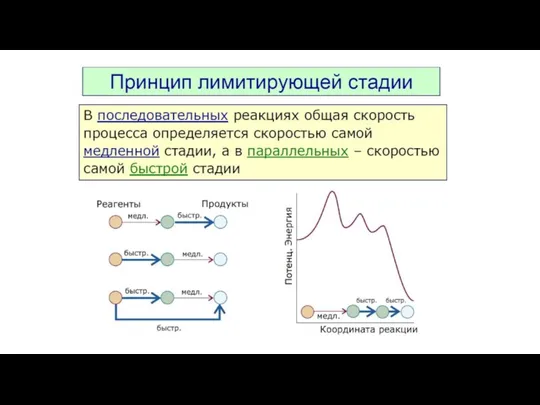
- 10. Под механизмом реакции в кинетике понимают путь реакции, т. е. подробное изменение координат всех частиц в
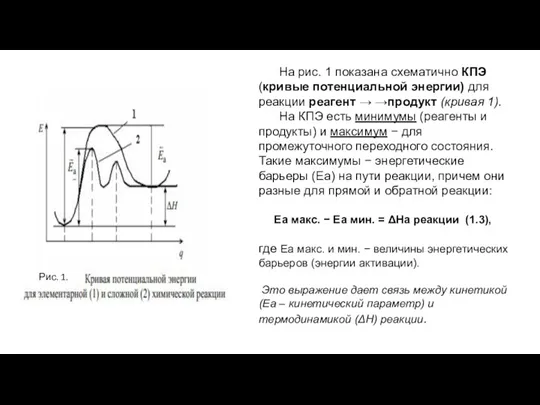
- 11. На рис. 1 показана схематично КПЭ (кривые потенциальной энергии) для реакции реагент → →продукт (кривая 1).
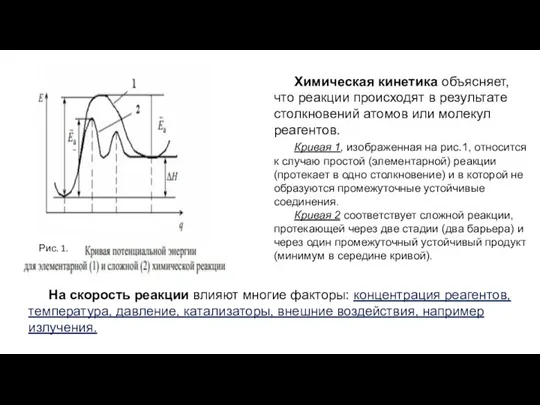
- 12. Химическая кинетика объясняет, что реакции происходят в результате столкновений атомов или молекул реагентов. Кривая 1, изображенная
- 13. 2. Влияние концентрации на скорость химической реакции Т.к. скорость химической реакции зависит от столкновений, а количество
- 14. Зависимость скорости химической реакции от концентрации реагентов Закон действующих масс гласит: при постоянной температуре скорость элементарной
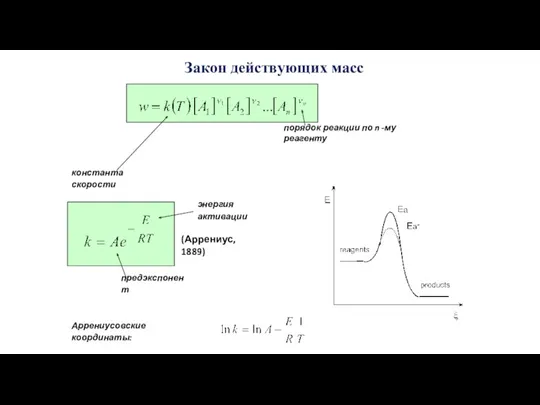
- 16. Закон действующих масс константа скорости порядок реакции по n -му реагенту (Аррениус, 1889) энергия активации предэкспонент
- 19. Особенности гетерогенных реакций Стадии гетерогенных реакций : подвод вещества к реакционной поверхности химическое взаимодействие отвод продукта
- 20. 3. Влияние давления на скорость химической реакции Влияние давления существенно влияет на реакции с участием газообразных
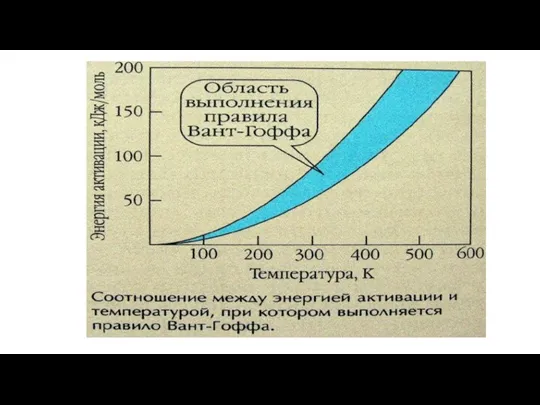
- 21. Правило Вант-Гоффа При повышении температуры на каждые 100 скорость большинства реакций увеличивается в 2-4 раза: и
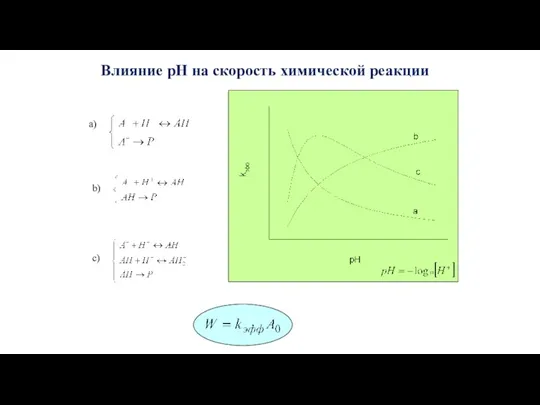
- 23. Влияние pH на скорость химической реакции a) b) c)
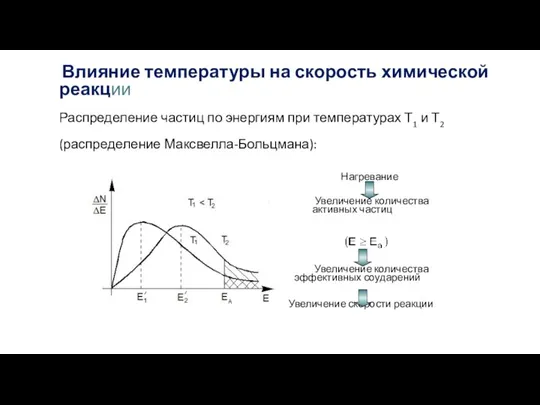
- 24. Влияние температуры на скорость химической реакции Распределение частиц по энергиям при температурах Т1 и Т2 (распределение
- 25. Влияние T на скорость химической реакции - слабая функция от T для химических реакций - резкая
- 26. Ферментативный катализ Схема Михаэлиса-Ментен: фермент субстрат комплекс
- 27. константа Михаэлиса максимальная скорость стационарная скорость Ферментативный катализ
- 28. Зависимость константы скорости от температуры Уравнение Аррениуса Еа ‑ энергия активации, кДж/моль R ‑ универсальная газовая
- 29. Влияние катализаторов на скорость химической реакции Катализаторы - вещества, увеличивающие скорость реакции и остающиеся в конце
- 32. Задачи на определение Скорости химических реакций
- 33. Пример 2.
- 34. Пример 3.
- 35. Пример 4.
- 36. Пример 5.
- 37. Заключение Химическая кинетика изучает скорости и механизмы химических процессов, а также факторы, влияющие на них Скорость
- 39. Скачать презентацию




























 Типичные окислители
Типичные окислители Количество вещества. 8 класс
Количество вещества. 8 класс Химическая связь. Взаимное влияние атомов в молекуле
Химическая связь. Взаимное влияние атомов в молекуле Основания. Классификация оснований
Основания. Классификация оснований Водородный показатель
Водородный показатель Химические свойства металлов. Взаимодействие с простыми веществами
Химические свойства металлов. Взаимодействие с простыми веществами Молярный объем газов. 8 класс
Молярный объем газов. 8 класс Использование технологии уровневой дифференциации на уроках химии
Использование технологии уровневой дифференциации на уроках химии Кристаллические решётки и их виды
Кристаллические решётки и их виды Алкалоиды, производные тропана
Алкалоиды, производные тропана Термохимия. Термохимические уравнения
Термохимия. Термохимические уравнения Общие представления о фазовых состояниях и фазовых переходах полимеров
Общие представления о фазовых состояниях и фазовых переходах полимеров фосфор и его соединения
фосфор и его соединения Эколого-химическая характеристика качества почвы
Эколого-химическая характеристика качества почвы Закон триад. Открытие периодического закона
Закон триад. Открытие периодического закона Жидкое и растворимое стекло
Жидкое и растворимое стекло Основы химической термодинамики и кинетики химических реакций
Основы химической термодинамики и кинетики химических реакций O-alkylation catalysts
O-alkylation catalysts Электролитическая диссоциация
Электролитическая диссоциация Мінеральні добрива та їх класифікація
Мінеральні добрива та їх класифікація Псевдоморфозы. Образование псевдоморфоз
Псевдоморфозы. Образование псевдоморфоз Құрамында белгілі қоспасы бар басқа заттың массасын (көлемін) реакция теңдеуі бойынша есептеу
Құрамында белгілі қоспасы бар басқа заттың массасын (көлемін) реакция теңдеуі бойынша есептеу Топырақ биоремедиациясы
Топырақ биоремедиациясы Равновесие в растворах электролитов
Равновесие в растворах электролитов Галогены. Свойства галогенов
Галогены. Свойства галогенов Ртуть
Ртуть Циклоалканы. 10 класс
Циклоалканы. 10 класс Фенолы. Классификация и номенклатура фенолов
Фенолы. Классификация и номенклатура фенолов