Содержание
- 2. Цели урока Вспомнить понятие о кислотах, как о классе электролитов; Рассмотреть классификацию кислот по различным признакам;
- 3. План урока I. Состав и классификация кислот; II. Ионные уравнения реакций на примере химических свойств кислот;
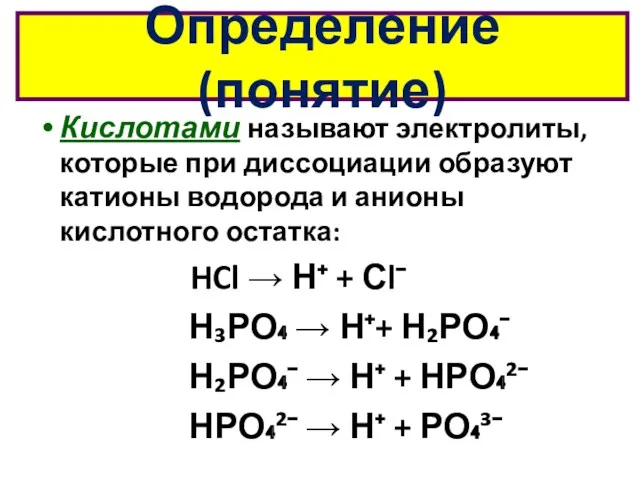
- 4. Определение (понятие) Кислотами называют электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка: HCl
- 5. Задание Выберите формулы кислот: КNО₂ Н₂О₂ Н₂СО₃ NаНSО₄ NаОН НF Са(ОН)₂ Мg(НСО₃)₂ Н₂SО₄ Аl(NО₃)₃ СuОН НМnО4
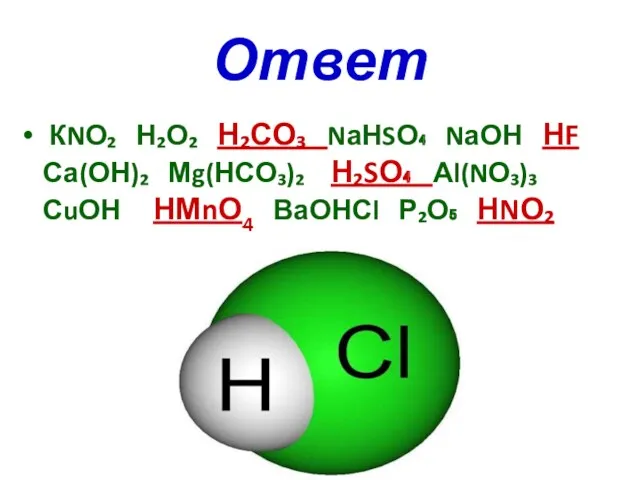
- 6. Ответ КNО₂ Н₂О₂ Н₂СО₃ NаНSО₄ NаОН НF Са(ОН)₂ Мg(НСО₃)₂ Н₂SО₄ Аl(NО₃)₃ СuОН НМnО4 ВаОНСl Р₂О₅ НNО₂
- 7. Физические свойства кислот: Кислоты бывают: твердыми (фосфорная, кремниевая) жидкими ( серная кислота). Такие газы, как хлороводород
- 8. Водные растворы соляной, серной, фосфорной и ряда других кислот не имеют окраски. Водные растворы хромовой кислоты
- 9. Классификация кислот: 1. Наличие кислорода в кислотном остатке Кислородные H3PO4 HNO3 Бескислородные H2S, HCl HBr
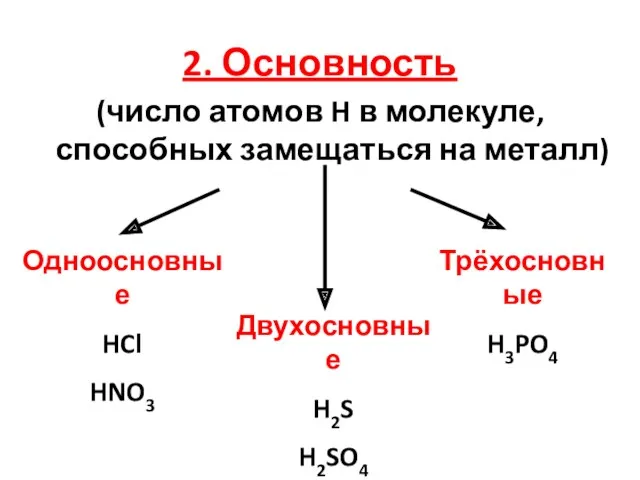
- 10. 2. Основность (число атомов H в молекуле, способных замещаться на металл) Одноосновные HCl HNO3 Двухосновные H2S
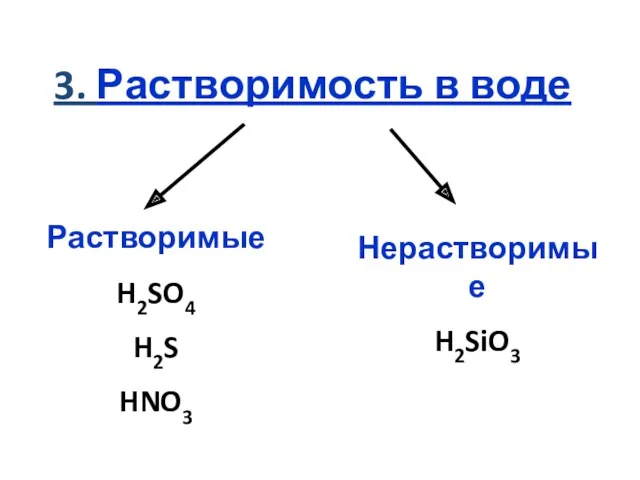
- 11. 3. Растворимость в воде Растворимые H2SO4 H2S HNO3 Нерастворимые H2SiO3
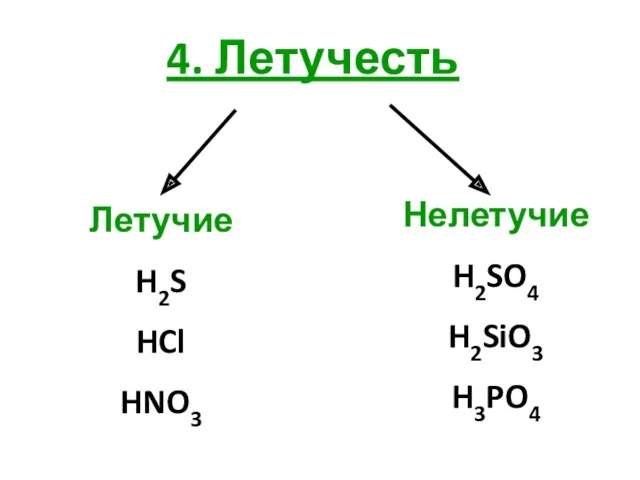
- 12. 4. Летучесть Летучие H2S HCl HNO3 Нелетучие H2SO4 H2SiO3 H3PO4
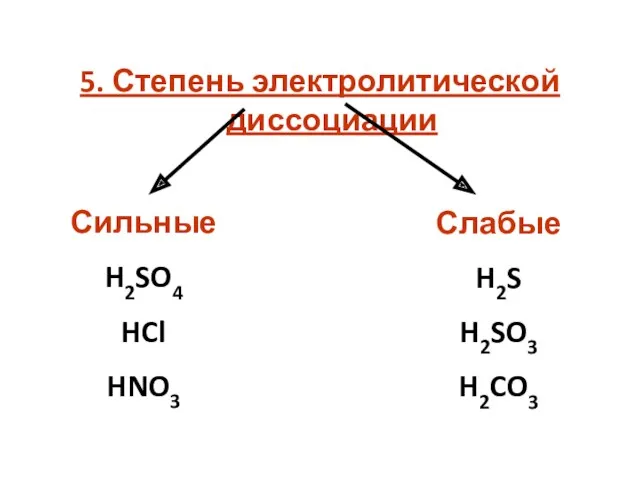
- 13. 5. Степень электролитической диссоциации Сильные H2SO4 HCl HNO3 Слабые H2S H2SO3 H2CO3
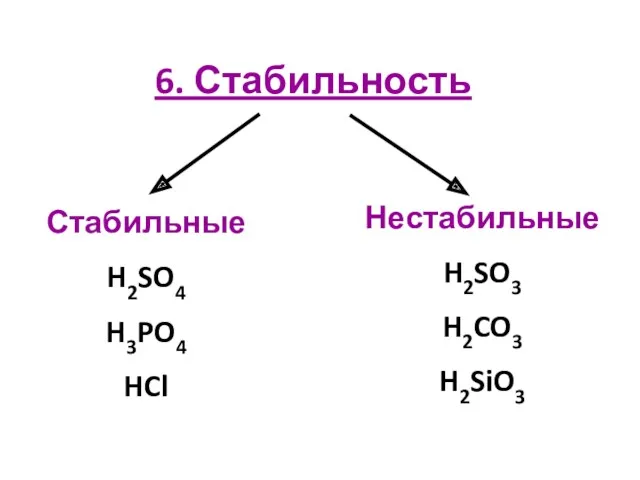
- 14. 6. Стабильность Стабильные H2SO4 H3PO4 HCl Нестабильные H2SO3 H2CO3 H2SiO3
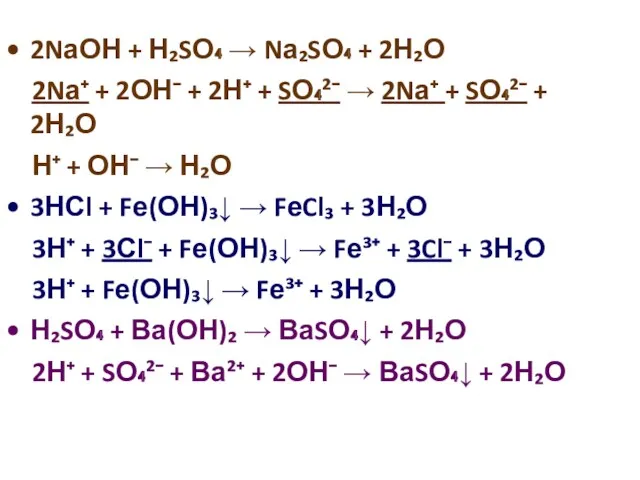
- 15. Химические свойства кислот 1)Реакция нейтрализации: кислота + основание → соль + вода (реакция обмена)
- 16. 2NаОН + Н₂SО₄ → Nа₂SО₄ + 2Н₂О 2Nа⁺ + 2ОН⁻ + 2Н⁺ + SО₄²⁻ → 2Nа⁺
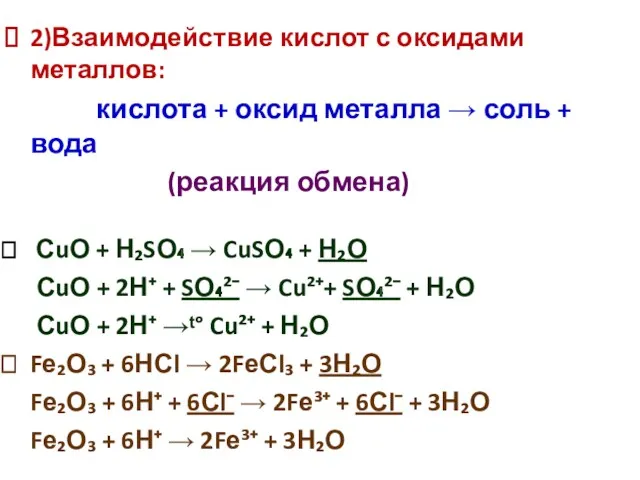
- 17. 2)Взаимодействие кислот с оксидами металлов: кислота + оксид металла → соль + вода (реакция обмена) СuО
- 18. 3)Взаимодействие кислот с металлами: кислота + металл → соль + водород (реакция замещения) Условия протекания реакций:
- 19. 3) Нерастворимые кислоты (кремневая) не вступают в реакции с металлами: Н₂SiО₃ + Мg → 4)Концентрированный и
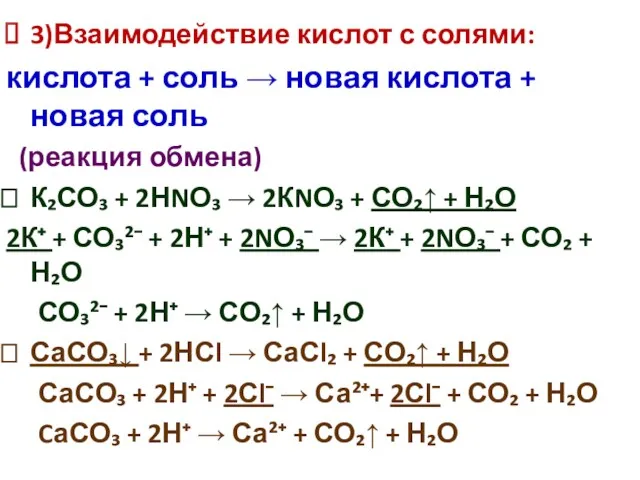
- 20. 3)Взаимодействие кислот с солями: кислота + соль → новая кислота + новая соль (реакция обмена) К₂СО₃
- 21. Качественная реакция на SО₄²⁻ (сульфат-ион) ВаСl₂ + Н₂SО₄ → ВаSО₄↓ + 2НСl Ва²⁺ + 2Сl⁻ +
- 22. Качественная реакция на Сl⁻ (хлорид-ион) АgNО₃ + НСl → АgCl↓ + НNО₃ Аg⁺ + NО₃⁻ +
- 23. Итоги 1. Классификация кислот; 2. Типичные химические свойства кислот; 3. Условия протекания типичных реакций кислот;
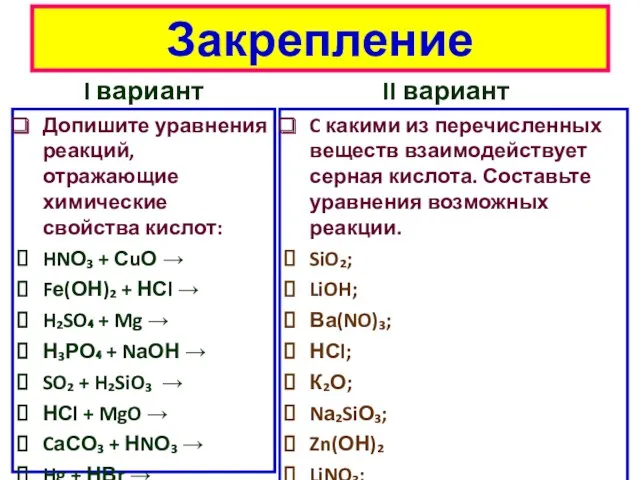
- 24. I вариант Допишите уравнения реакций, отражающие химические свойства кислот: HNО₃ + СuО → Fе(ОН)₂ + НСl
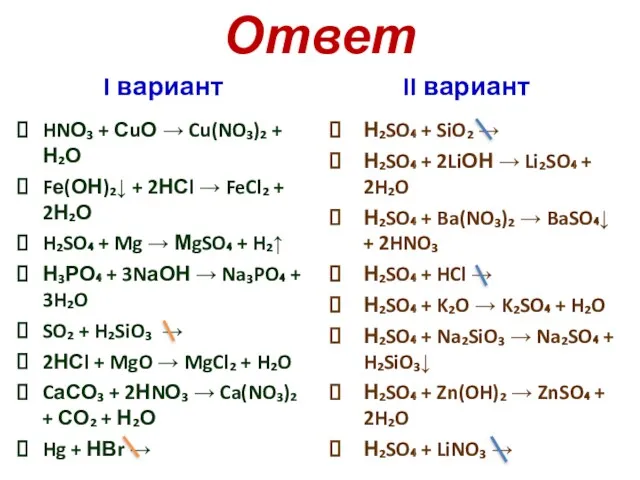
- 25. Ответ I вариант HNО₃ + СuО → Cu(NO₃)₂ + Н₂О Fе(ОН)₂↓ + 2НСl → FeCl₂ +
- 26. Дополнительное задание Запишите молекулярные и ионные уравнения практически осуществимых реакций, протекающих между: магнием и соляной кислотой;
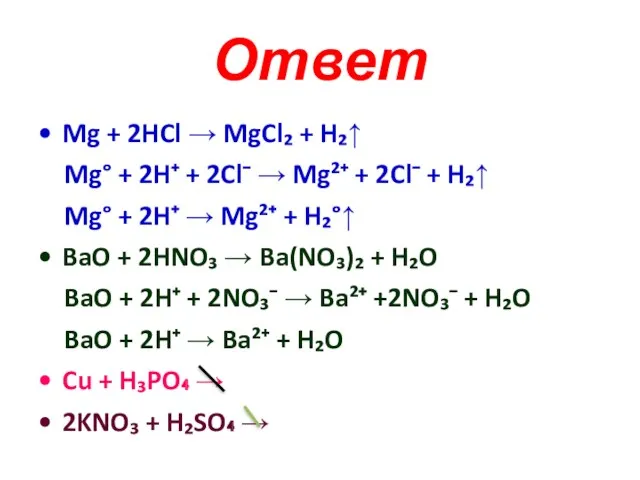
- 27. Ответ Mg + 2HCl → MgCl₂ + H₂↑ Mg° + 2H⁺ + 2Cl⁻ → Mg²⁺ +
- 29. Скачать презентацию











 Хімічні властивості металів
Хімічні властивості металів Карбоновые кислоты. Тест
Карбоновые кислоты. Тест Материаловедение. Основные задачи материаловедения
Материаловедение. Основные задачи материаловедения Электролитическая диссоциация. Вещества в растворах
Электролитическая диссоциация. Вещества в растворах Общая электронная теория восстановления и окисления металлов
Общая электронная теория восстановления и окисления металлов Фосфор. Урок в 9 классе
Фосфор. Урок в 9 классе Химические свойства кислот
Химические свойства кислот Кристаллические решетки
Кристаллические решетки Пробоотбор других ООС. Лекция 3
Пробоотбор других ООС. Лекция 3 Дисперсные системы в атмосфере
Дисперсные системы в атмосфере Хром. Физические и химические свойства
Хром. Физические и химические свойства Титан және оның қорытпалары. Титанның физика-химиялық қасиеттері
Титан және оның қорытпалары. Титанның физика-химиялық қасиеттері Химический факультет
Химический факультет Химия как компонент системы естественнонаучного образования
Химия как компонент системы естественнонаучного образования Cromatografia ionică
Cromatografia ionică Основні класи неорганічних сполук
Основні класи неорганічних сполук Алюминий и сплавы на его основе
Алюминий и сплавы на его основе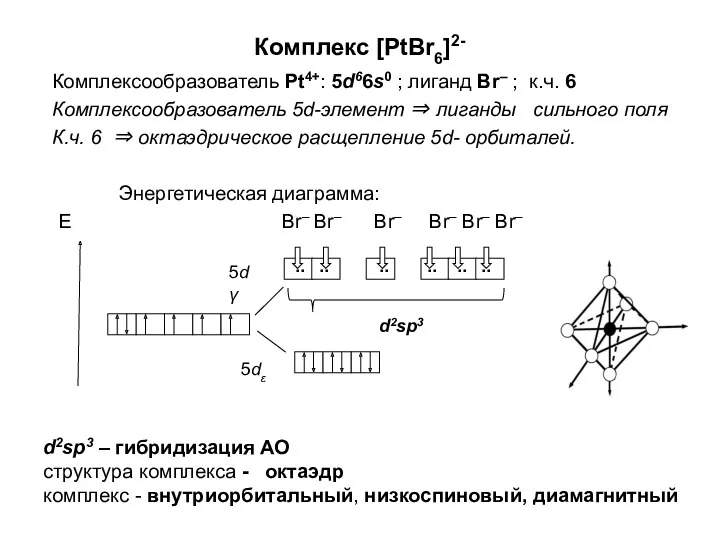 Комплексообразователь. (Лекция 5)
Комплексообразователь. (Лекция 5) Как и где используется соляная кислота
Как и где используется соляная кислота Электрохимические процессы
Электрохимические процессы Кислород. Атом кислорода
Кислород. Атом кислорода Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Классификация и общая характеристика механизмов образования свободных радикалов и активных форм кислорода
Классификация и общая характеристика механизмов образования свободных радикалов и активных форм кислорода Гранулометрический состав горных пород
Гранулометрический состав горных пород Дезодоранты. Антиперспиранты
Дезодоранты. Антиперспиранты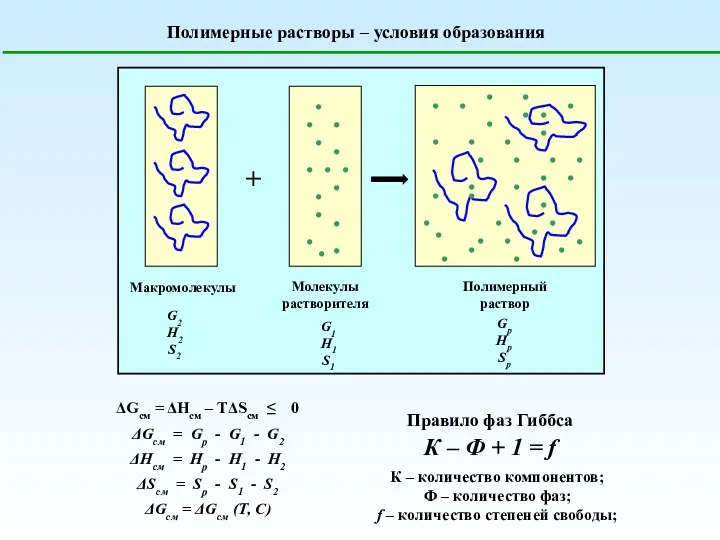 Полимерные растворы. Условия образования
Полимерные растворы. Условия образования Химиялық тепе-теңдік
Химиялық тепе-теңдік Неметаллы. Общая характеристика неметаллов
Неметаллы. Общая характеристика неметаллов