Содержание
- 2. Классы неорганических соединений Оксиды Кислоты Основания Соли
- 3. оксиды Бинарные соединения, состоящие из двух элементов, одним из которых является кислород
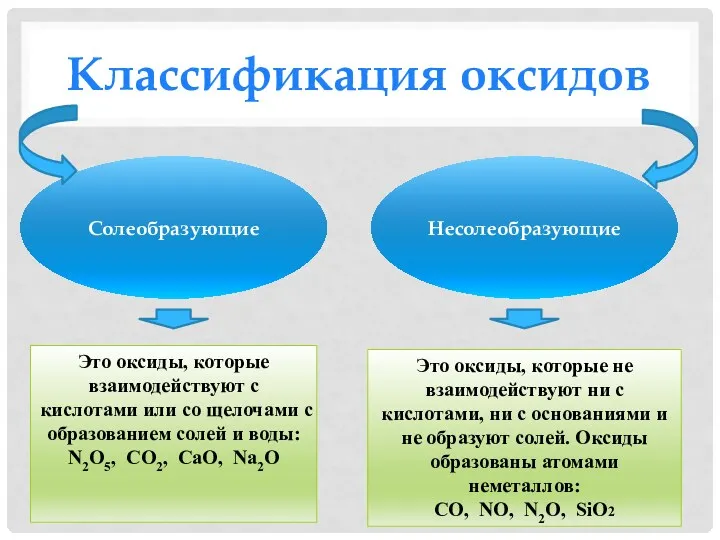
- 4. Классификация оксидов Солеобразующие Несолеобразующие Это оксиды, которые не взаимодействуют ни с кислотами, ни с основаниями и
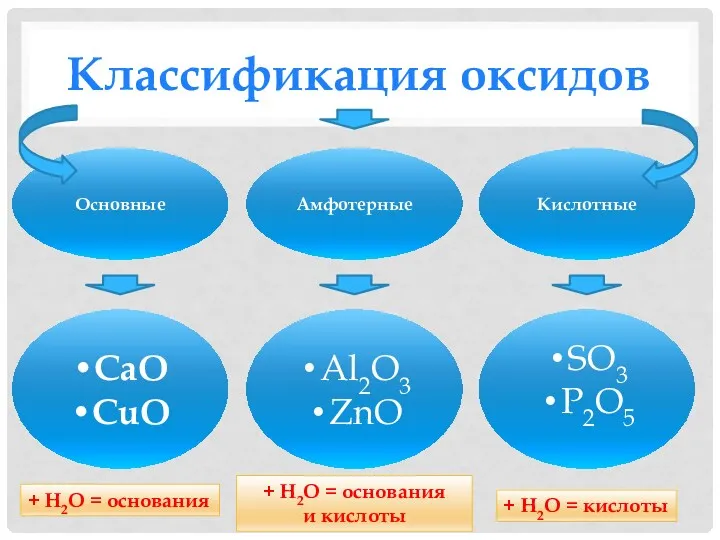
- 5. Классификация оксидов Основные Амфотерные Кислотные CaO CuO Al2O3 ZnO SO3 P2O5 + Н2О = основания +
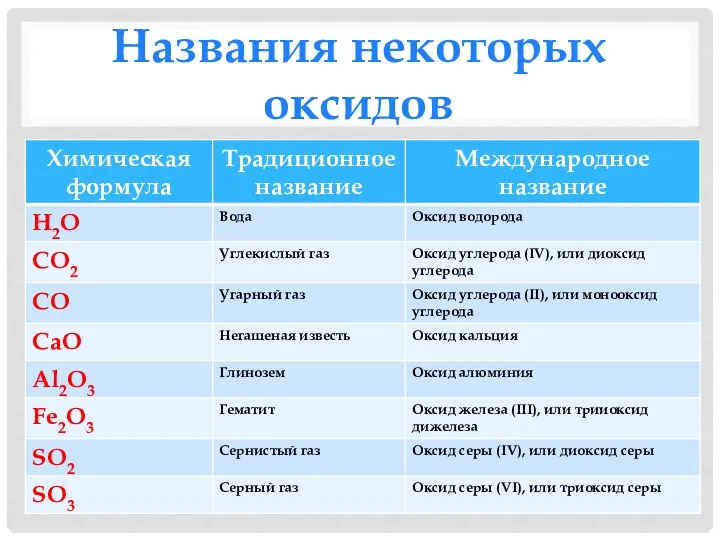
- 6. Названия некоторых оксидов
- 7. Структурные формулы оксидов SO2 S О О Al2O3 Al Al О О О К2O О К
- 8. Получение оксидов 1. Взаимодействие простых веществ с кислородом: С + O2 = CO2 Cu + O2
- 9. Получение оксидов 2. Горение сложных веществ: CH4 + O2 = CO2 + H2O 2 2 Метан
- 10. Получение оксидов 3. Окисление оксидов: FeO + O2 = Fe2O3 CO + O2 = CO2 2
- 11. Получение оксидов 4. Разложение нерастворимых оснований при нагревании: 2 Mg(OH)2 = MgO + H2O Fe(OH)3 =
- 12. Получение оксидов 5. Разложение солей: CaCO3 = CaO + CO2 CaSO4 = CaO + SO3
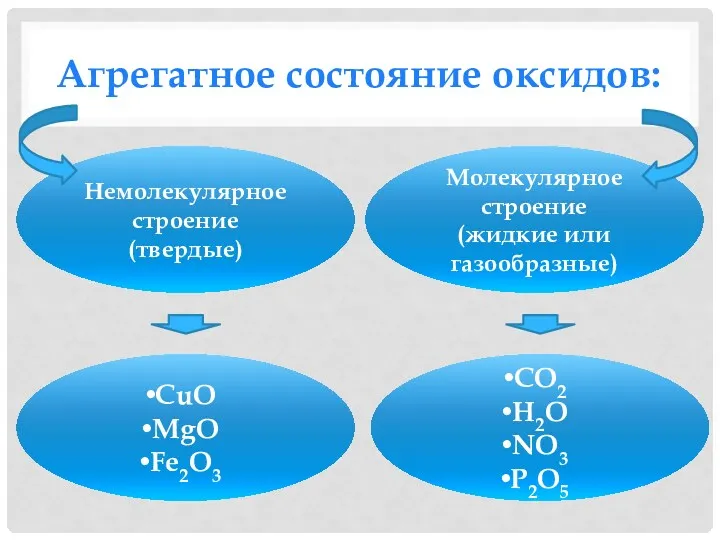
- 13. Агрегатное состояние оксидов: Немолекулярное строение (твердые) Молекулярное строение (жидкие или газообразные) CuO MgO Fe2O3 CO2 H2O
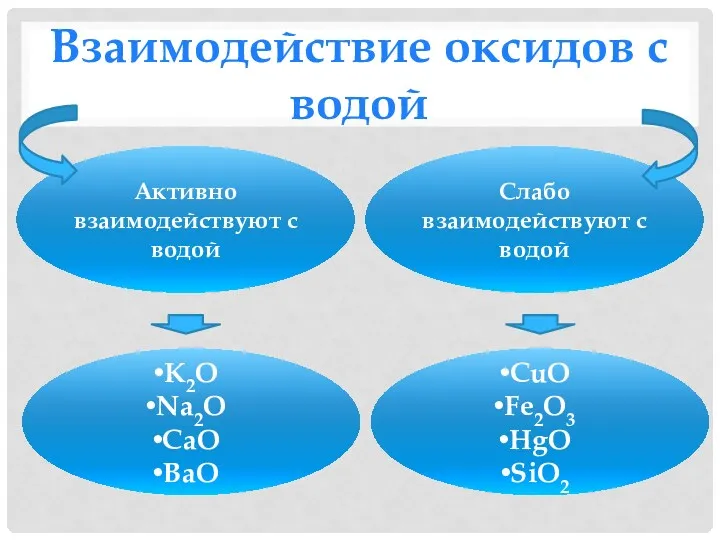
- 14. Взаимодействие оксидов с водой Активно взаимодействуют с водой Слабо взаимодействуют с водой K2O Na2O CaO BaO
- 15. Химические свойства основных оксидов 1. Взаимодействие основных оксидов с водой и образованием щелочи: Na2O + H2O
- 16. Химические свойства основных оксидов 2. Взаимодействие основных оксидов с сильными кислотами с образованием соли и воды:
- 17. Химические свойства основных оксидов 3. Взаимодействие основных и кислотных оксидов между собой с образованием соли: CaO
- 18. Химические свойства кислотных оксидов 1. Взаимодействие с водой с образование кислот: SO3 + H2O = H2SO4
- 19. Химические свойства кислотных оксидов 2. Взаимодействие кислотных оксидов со щелочами с образованием соли и воды: NaOH
- 20. Химические свойства кислотных оксидов 3. Взаимодействие кислотных оксидов с основными оксидами с образованием соли: SiO2 +
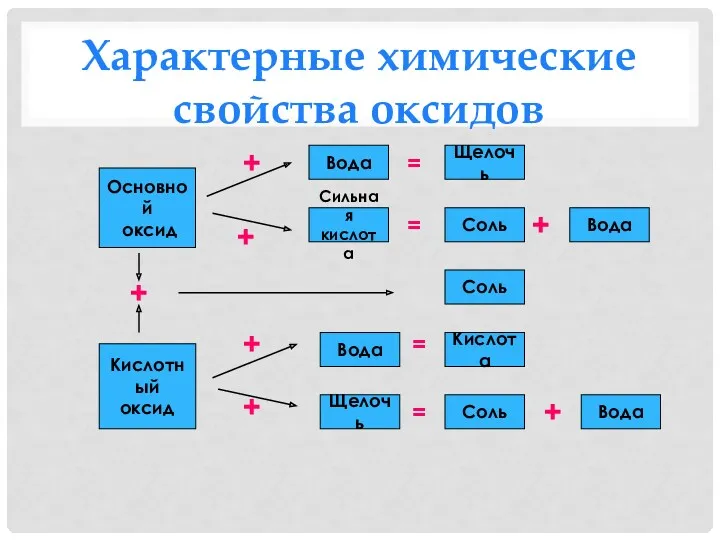
- 21. Характерные химические свойства оксидов Основной оксид Кислотный оксид Щелочь Вода Сильная кислота Вода Вода Вода Соль
- 22. Химические свойства амфотерных оксидов Основные свойства ZnO + H2SO4 = ZnSO4 + H2O Кислотные свойства ZnO
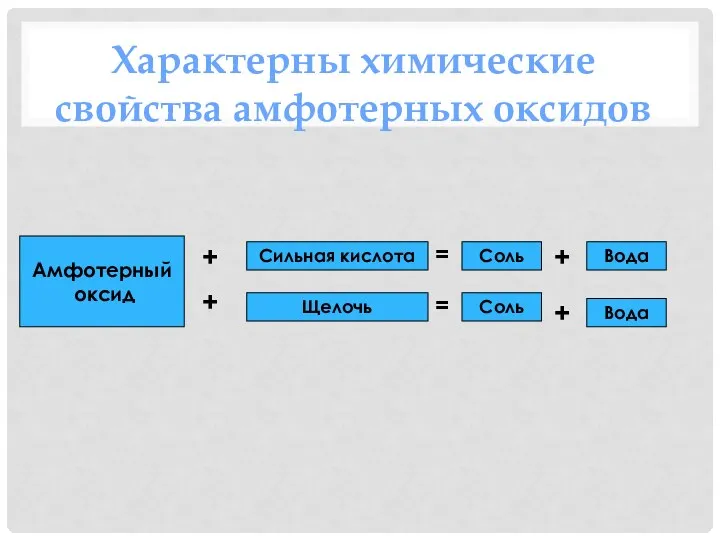
- 23. Амфотерный оксид Сильная кислота Щелочь Соль Соль Вода Вода + + + + = = Характерны
- 25. Скачать презентацию














 Липиды
Липиды Період як особлива синтаксична конструкція
Період як особлива синтаксична конструкція Глицерин. Свойства и применение
Глицерин. Свойства и применение Крекинг нефти
Крекинг нефти Аварийно-химически-опасные вещества (АХОВ). Описание. Методы оказания первой помощи
Аварийно-химически-опасные вещества (АХОВ). Описание. Методы оказания первой помощи Химическая связь
Химическая связь Приготовление растворов солей с определенной массовой долей растворенного вещества
Приготовление растворов солей с определенной массовой долей растворенного вещества Вода – это жизнь!
Вода – это жизнь! The production of stable isotopes
The production of stable isotopes Молибден. Нахождение в природе
Молибден. Нахождение в природе Предмет біоорганічної хімії. Класифікація, номенклатура, електронні уявлення, будова, реакційна здатність органічних сполук
Предмет біоорганічної хімії. Класифікація, номенклатура, електронні уявлення, будова, реакційна здатність органічних сполук Түймедақ гүлімен құрғақ теріге арналған ылғалдандырушы крем дайындау
Түймедақ гүлімен құрғақ теріге арналған ылғалдандырушы крем дайындау Аммиак
Аммиак Что нас объединяет?
Что нас объединяет? Таблицы. Определение характера оксидов
Таблицы. Определение характера оксидов Основи
Основи Методы оценки плотности и вязкости нефтей и нефтепродуктов
Методы оценки плотности и вязкости нефтей и нефтепродуктов Ионное произведение воды. Водородный показатель
Ионное произведение воды. Водородный показатель Ионы и ионная химическая связь
Ионы и ионная химическая связь Металлы главных подгрупп
Металлы главных подгрупп Производство извести
Производство извести Металлы. Свойства металлов
Металлы. Свойства металлов Химия. D-элементтер
Химия. D-элементтер Методы определения вязкости жидкости
Методы определения вязкости жидкости Химический состав клетки
Химический состав клетки Основні класи неорганічних сполук
Основні класи неорганічних сполук Алюминий (лат. Aluminium)
Алюминий (лат. Aluminium) Непредельные углеводороды. Алкины
Непредельные углеводороды. Алкины