Содержание
- 2. Элементный состав клетки Макроэлементы (99% массы клетки): (кислород, углерод, азот, водород) - 98% массы клетки; калий,
- 3. Химический состав клетки Органические соединения: ВМС (биополимеры) НМС Неорганические соединения: простые соединения (атомарные, молекулярные); сложные соединения;
- 4. Сложные неорганические соединения клетки, ионы Сложные (оксиды, соли, кислоты, основания) соединения. Важнейшие оксиды: Н2О, СО2, NO.
- 5. Функции ионов в клетке Входят в состав белков (ферментов, гормонов, пигментов). Обеспечивают буферные свойства. Являются регуляторами
- 6. Вода. Физико-химические свойства. Прозрачная жидкость без вкуса и запаха; Чистая вода не проводит электрический ток (молекулы
- 7. Функции воды универсальный растворитель (растворение и гидратирование веществ); участник химических реакций (гидролиз, гидратация, фотолиз воды); обеспечение
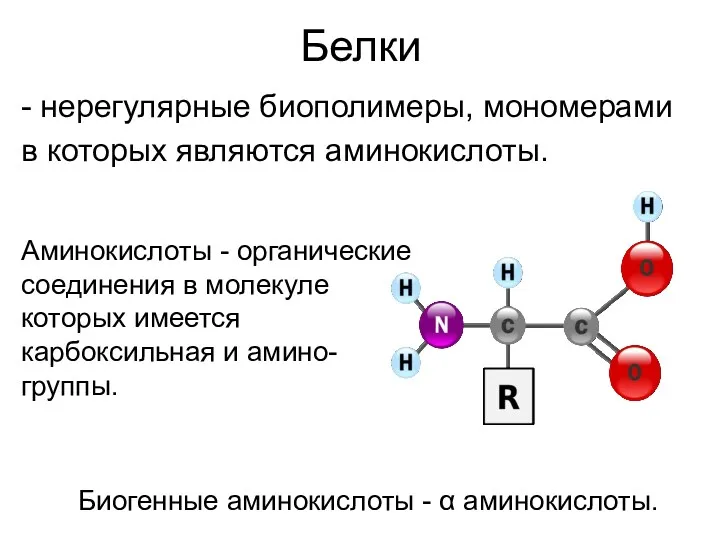
- 8. Белки - нерегулярные биополимеры, мономерами в которых являются аминокислоты. Аминокислоты - органические соединения в молекуле которых
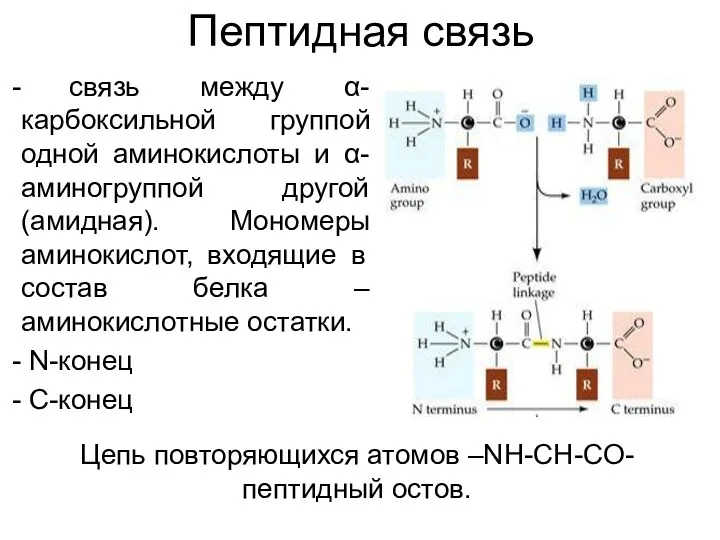
- 9. Пептидная связь связь между α-карбоксильной группой одной аминокислоты и α-аминогруппой другой (амидная). Мономеры аминокислот, входящие в
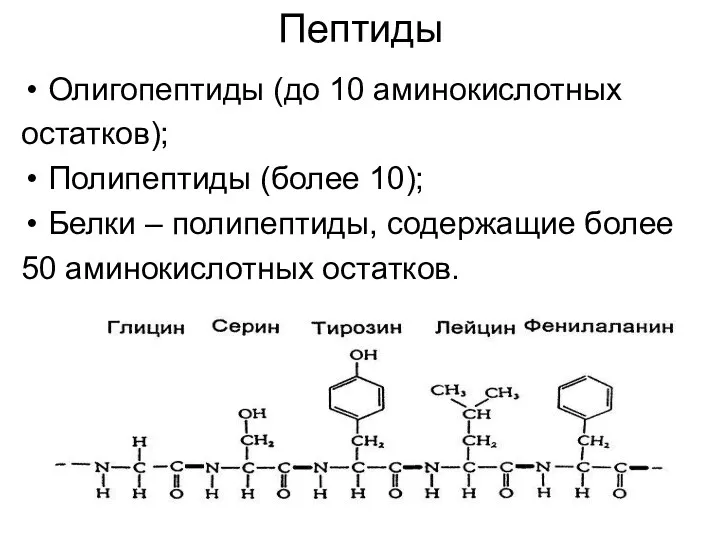
- 10. Пептиды Олигопептиды (до 10 аминокислотных остатков); Полипептиды (более 10); Белки – полипептиды, содержащие более 50 аминокислотных
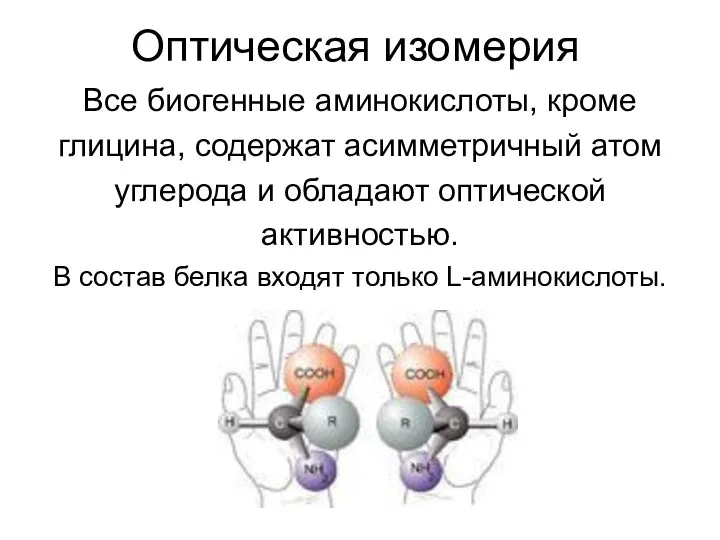
- 11. Оптическая изомерия Все биогенные аминокислоты, кроме глицина, содержат асимметричный атом углерода и обладают оптической активностью. В
- 12. Роль D-аминокислот Оптические изомеры аминокислот претерпевают медленную самопроизвольную неферментативную рацемизацию. Например, в белках дентина L-аспартат переходит
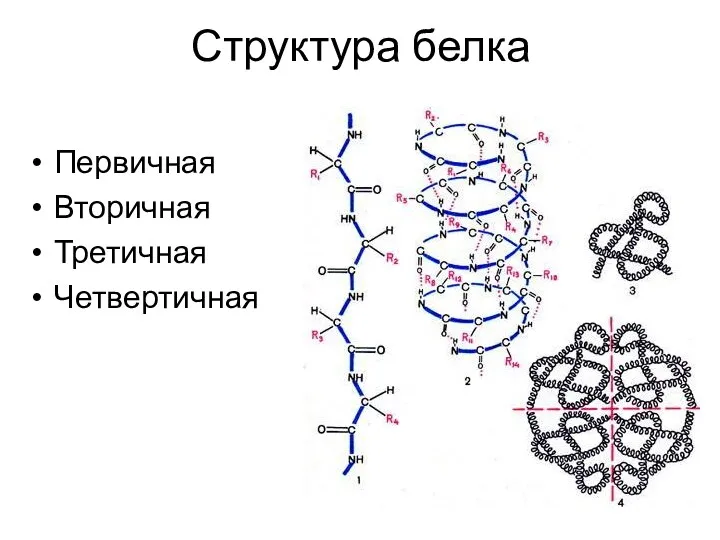
- 13. Структура белка Первичная Вторичная Третичная Четвертичная
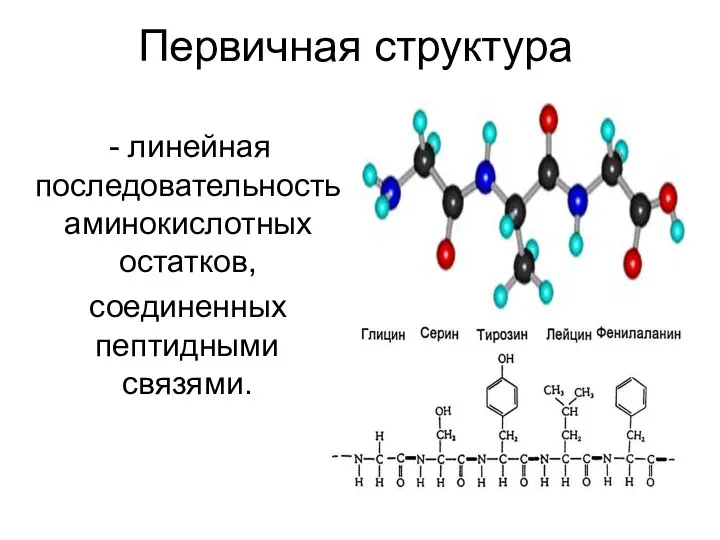
- 14. Первичная структура линейная последовательность аминокислотных остатков, соединенных пептидными связями.
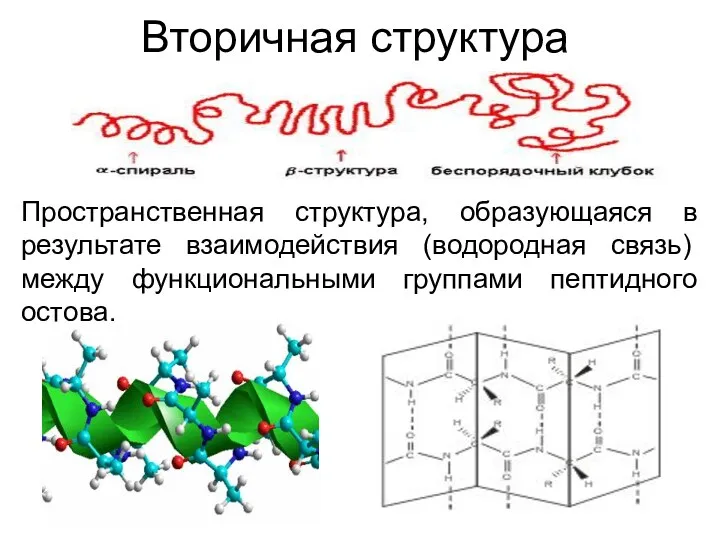
- 15. Вторичная структура Пространственная структура, образующаяся в результате взаимодействия (водородная связь) между функциональными группами пептидного остова.
- 16. Третичная структура - пространственная структура белковой молекулы, образующаяся за счет взаимодействия радикалов аминокислотных остатков. Водородные связи.
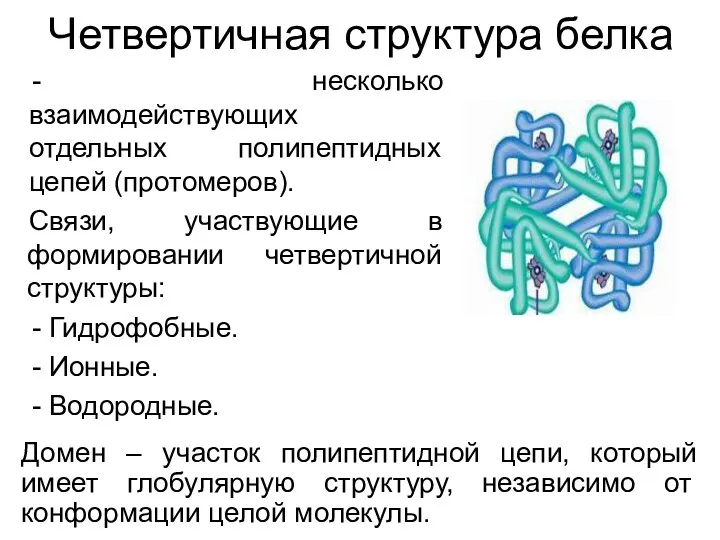
- 17. Четвертичная структура белка несколько взаимодействующих отдельных полипептидных цепей (протомеров). Связи, участвующие в формировании четвертичной структуры: Гидрофобные.
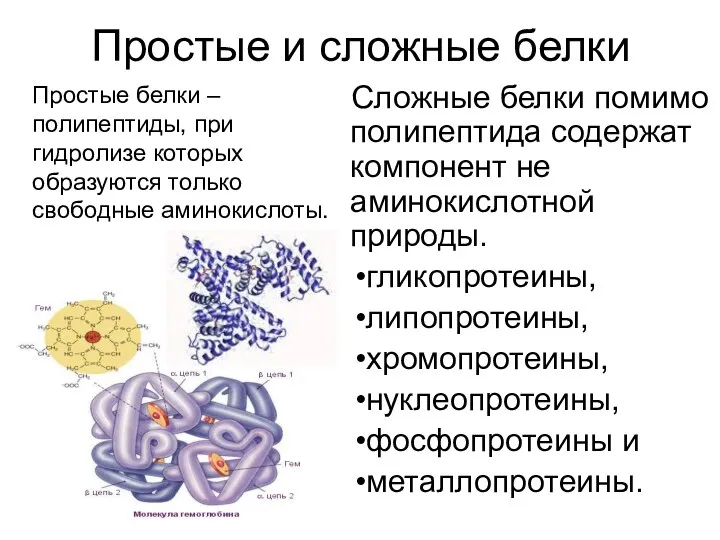
- 18. Простые и сложные белки Сложные белки помимо полипептида содержат компонент не аминокислотной природы. гликопротеины, липопротеины, хромопротеины,
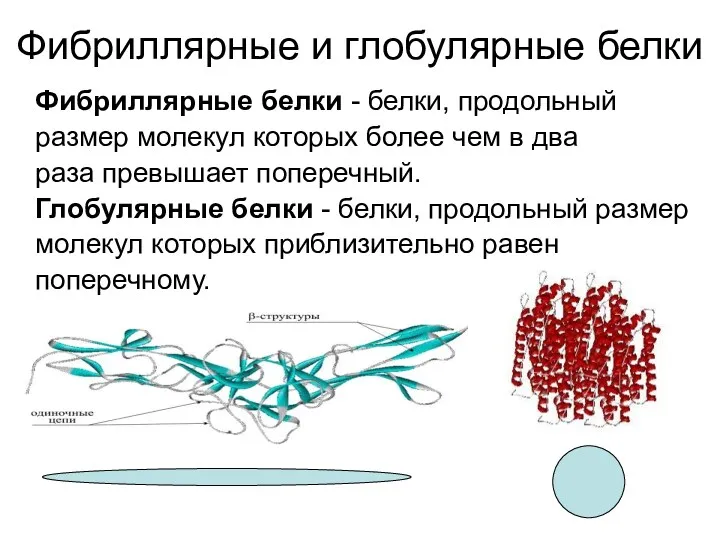
- 19. Фибриллярные и глобулярные белки Фибриллярные белки - белки, продольный размер молекул которых более чем в два
- 21. Углеводы (карбогидраты) полигидроксилсодержащие, гетерофункциональные производные карбонильных соединений. Моносахариды Олигосахариды (2-10 углеводных остатка) Полисахариды Функции углеводов: Структурная.
- 22. Моносахариды По природе карбонильной группы: Альдозы Кетозы По количеству атомов углерода: Триозы (глицериновый альдегид) Тетрозы (эритроза)
- 23. Таутомерия - равновесная динамическая изомерия, при котором два или более изомера легко переходят друг в друга.
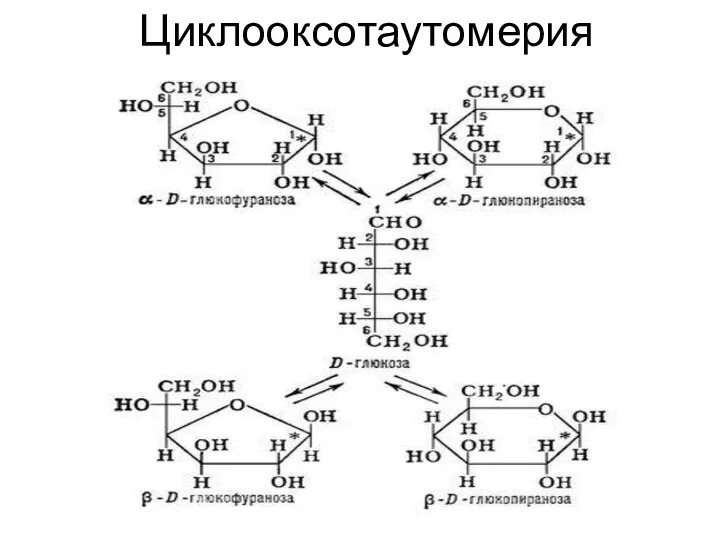
- 24. Циклооксотаутомерия
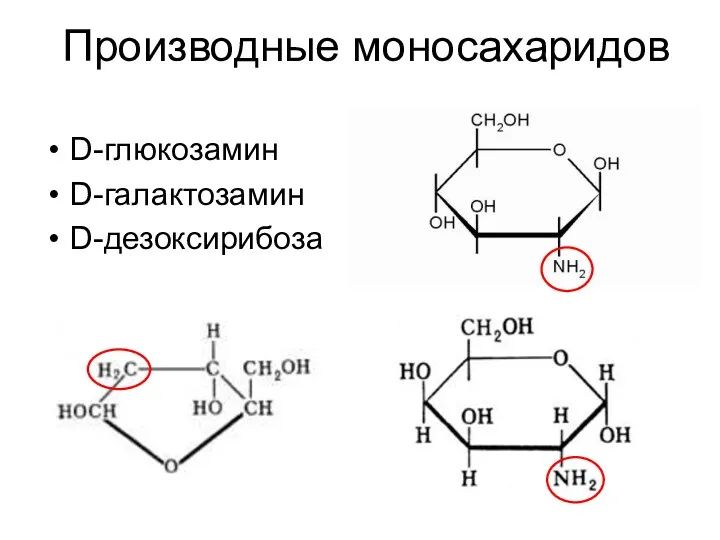
- 25. Производные моносахаридов D-глюкозамин D-галактозамин D-дезоксирибоза
- 26. Сиаловые кислоты N- и О-ацильные производные нейраминовой кислоты. Входят в состав гликопротеинов и гликолипидов.
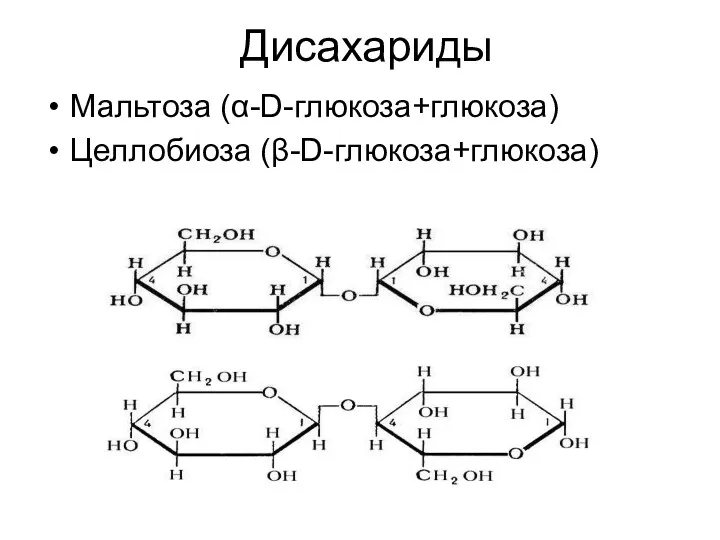
- 27. Дисахариды Мальтоза (α-D-глюкоза+глюкоза) Целлобиоза (β-D-глюкоза+глюкоза)
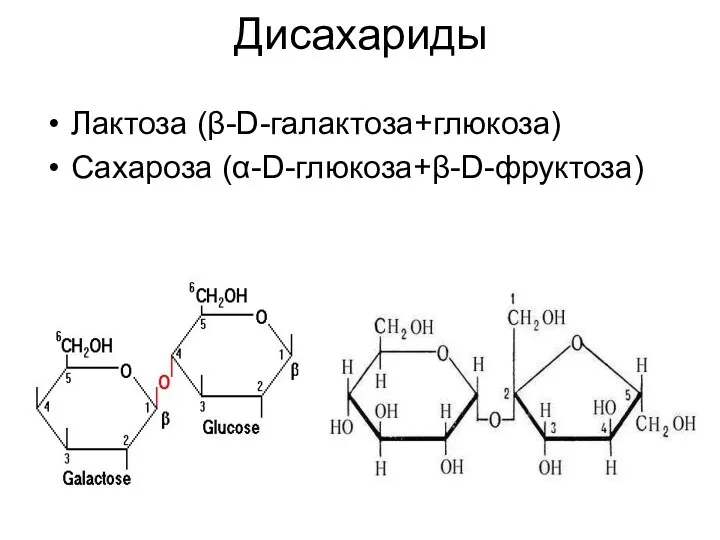
- 28. Дисахариды Лактоза (β-D-галактоза+глюкоза) Сахароза (α-D-глюкоза+β-D-фруктоза)
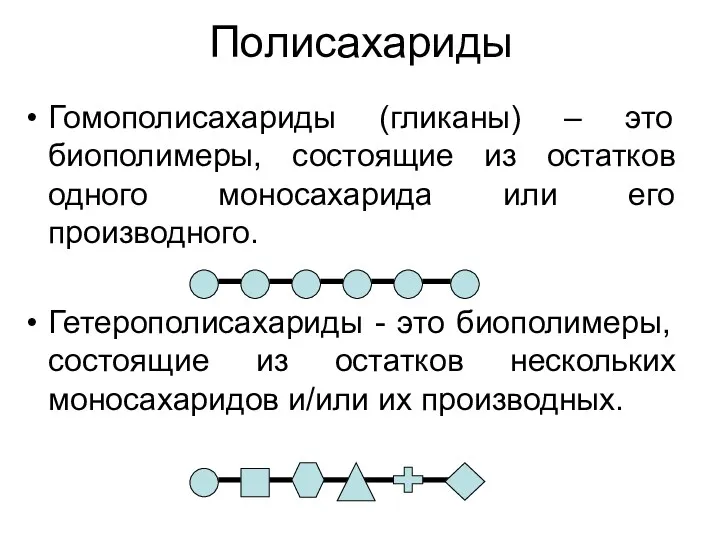
- 29. Полисахариды Гомополисахариды (гликаны) – это биополимеры, состоящие из остатков одного моносахарида или его производного. Гетерополисахариды -
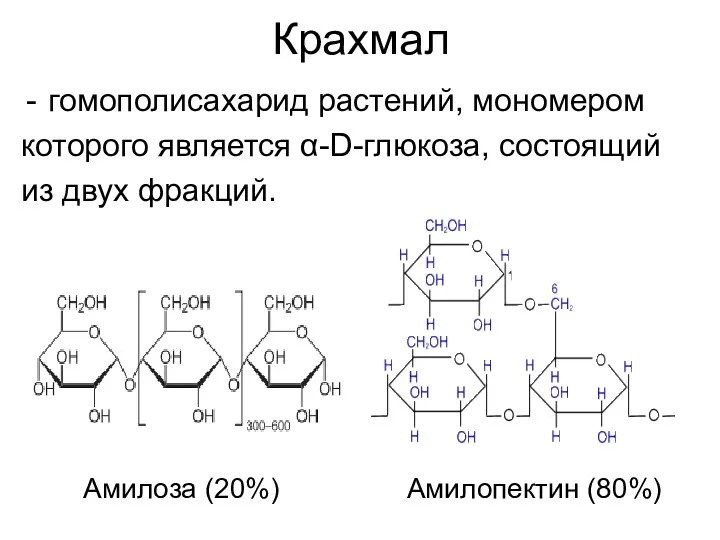
- 30. Крахмал гомополисахарид растений, мономером которого является α-D-глюкоза, состоящий из двух фракций. Амилоза (20%) Амилопектин (80%)
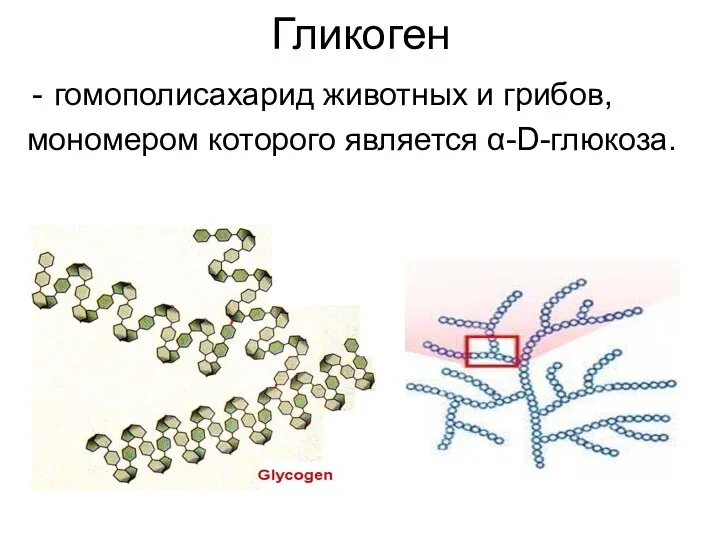
- 31. Гликоген гомополисахарид животных и грибов, мономером которого является α-D-глюкоза.
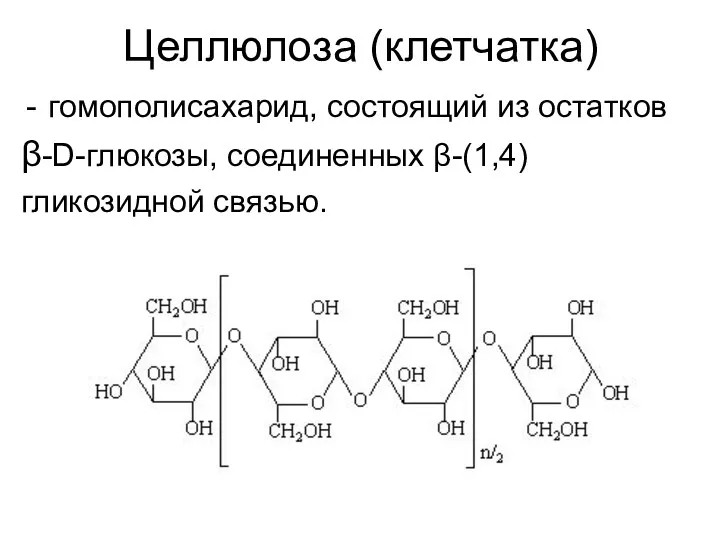
- 32. Целлюлоза (клетчатка) гомополисахарид, состоящий из остатков β-D-глюкозы, соединенных β-(1,4) гликозидной связью.
- 33. Прочие гомополисахариды Декстран - гомополисахарид бактерий, состоящий из остатков α-D-глюкозы, соединенных α-(1,4)-гликозидной связью. Инулин - гомополисахарид,
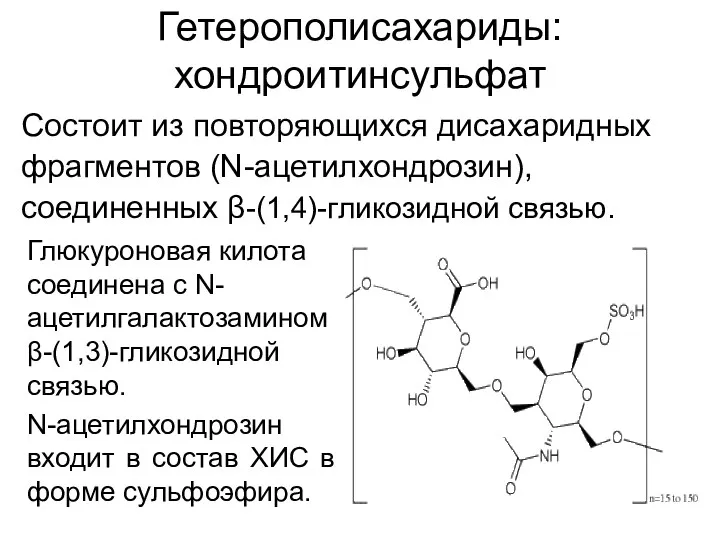
- 34. Гетерополисахариды: хондроитинсульфат Состоит из повторяющихся дисахаридных фрагментов (N-ацетилхондрозин), соединенных β-(1,4)-гликозидной связью. Глюкуроновая килота соединена с N-ацетилгалактозамином
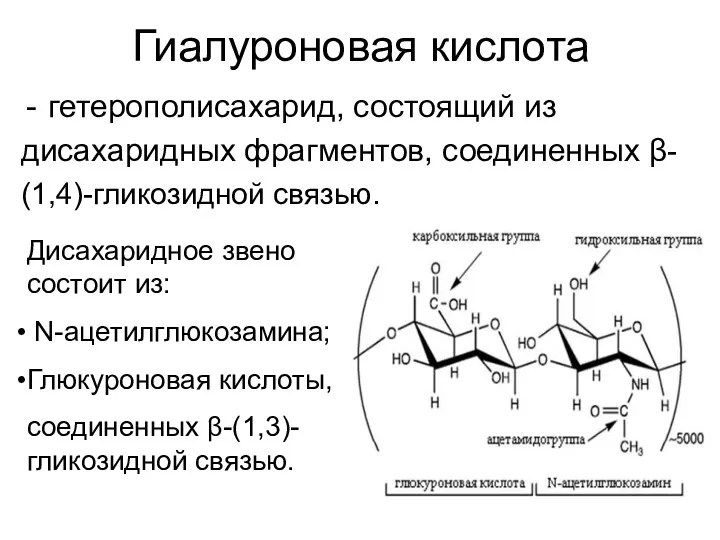
- 35. Гиалуроновая кислота гетерополисахарид, состоящий из дисахаридных фрагментов, соединенных β- (1,4)-гликозидной связью. Дисахаридное звено состоит из: N-ацетилглюкозамина;
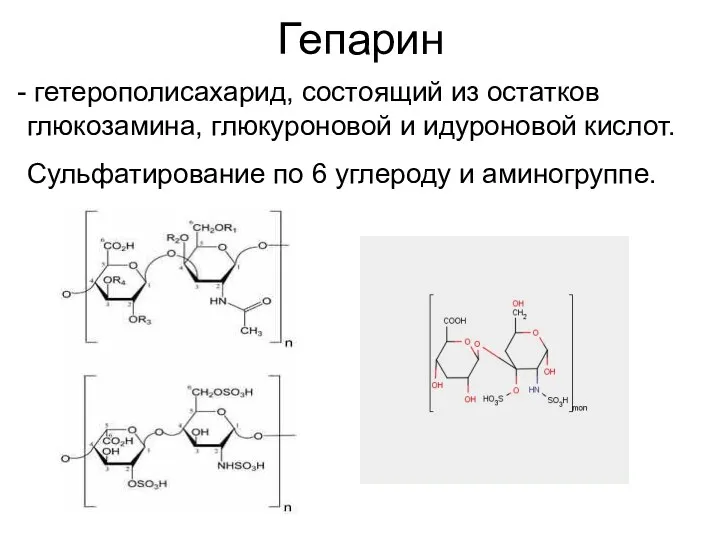
- 36. Гепарин гетерополисахарид, состоящий из остатков глюкозамина, глюкуроновой и идуроновой кислот. Сульфатирование по 6 углероду и аминогруппе.
- 37. Нуклеиновые кислоты высокомолекулярные органические соединения, биополимеры (полинуклеотиды), образованные мономерами – нуклеотидами.
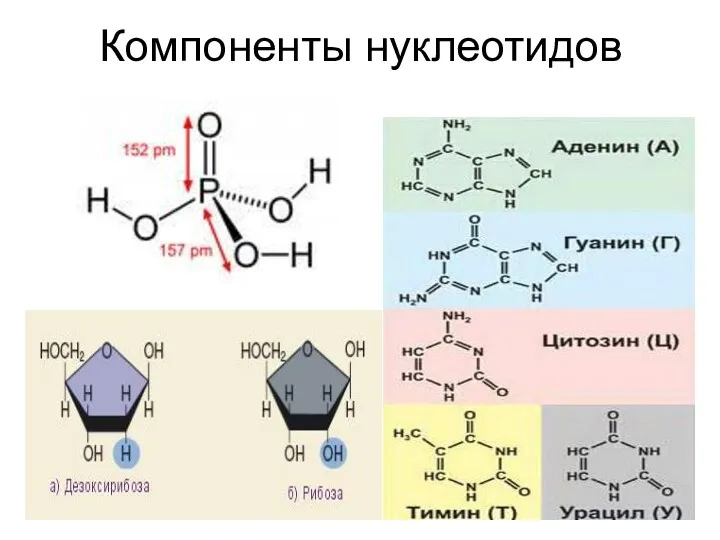
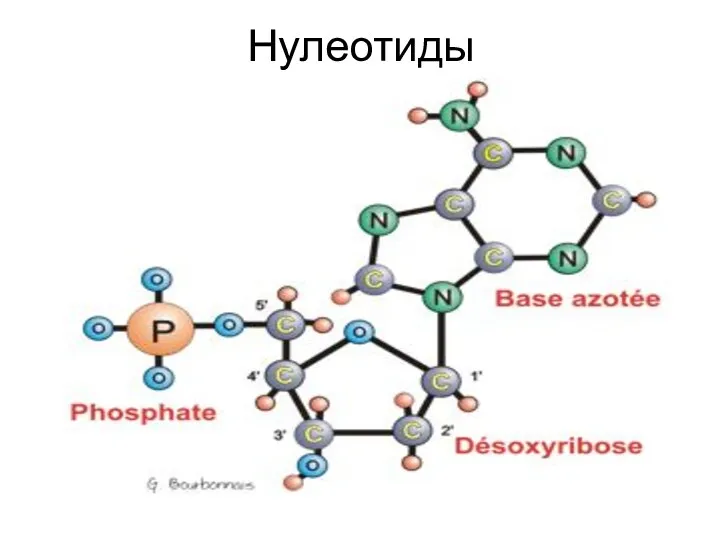
- 38. Компоненты нуклеотидов
- 39. Нулеотиды
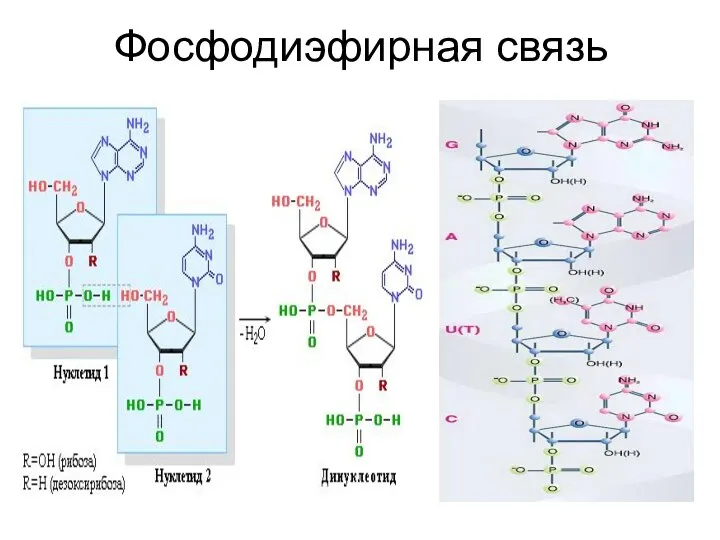
- 40. Фосфодиэфирная связь
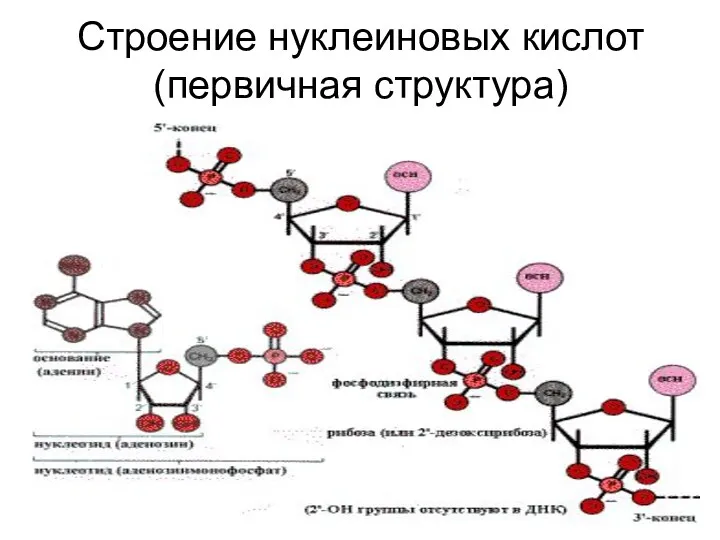
- 41. Строение нуклеиновых кислот (первичная структура)
- 42. Правила Чаргаффа А=Т, Ц=Г Пуриновые АО = Пиримидиновые АО Правила Чаргаффа послужили предпосылкой для разработки Ф.
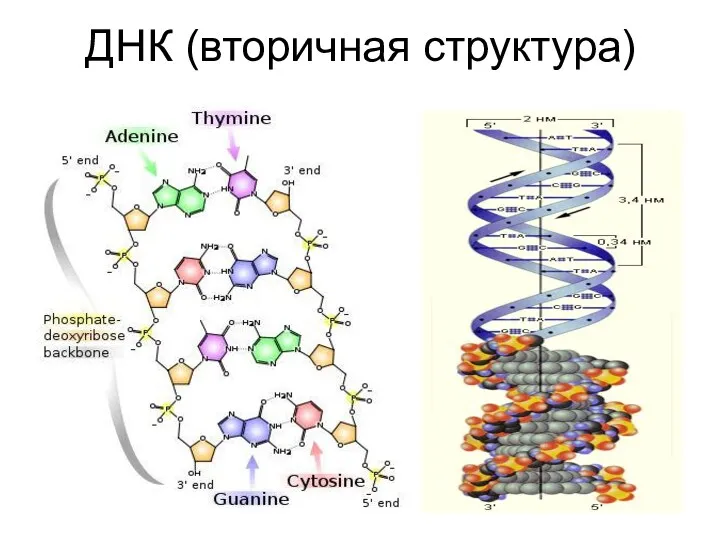
- 43. ДНК - нуклеиновая кислота, полимер дезоксирибонуклеотидов, в состав которых входят остаток ортофосфорной кислоты, дезоксирибозу и азотистые
- 44. ДНК (вторичная структура)
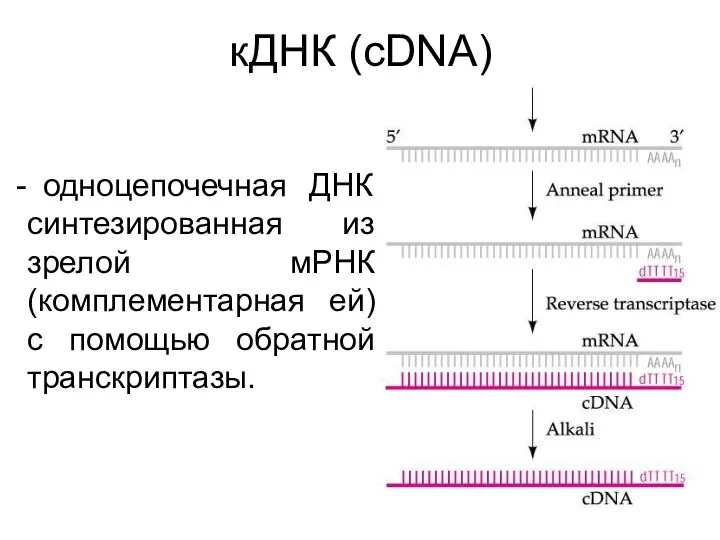
- 45. кДНК (cDNA) одноцепочечная ДНК синтезированная из зрелой мРНК (комплементарная ей) с помощью обратной транскриптазы.
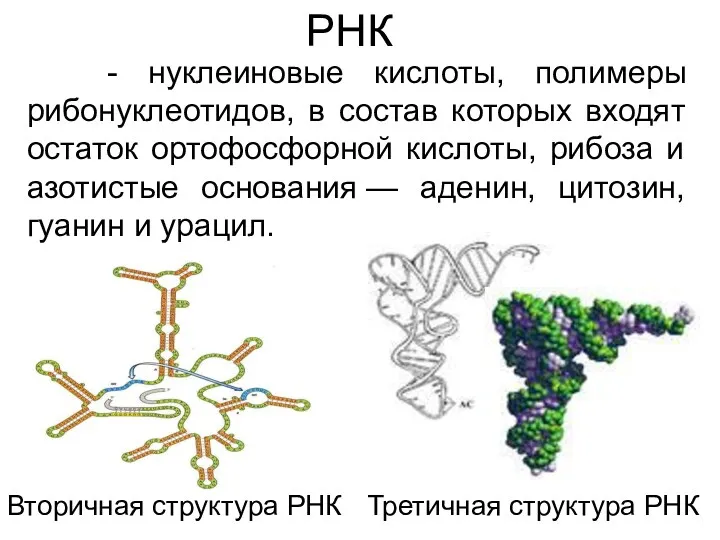
- 46. РНК - нуклеиновые кислоты, полимеры рибонуклеотидов, в состав которых входят остаток ортофосфорной кислоты, рибоза и азотистые
- 47. ДНК-подобная РНК (гяРНК,hnRNA) полирибонуклеотид, являющийся полной копией транскрибируемого участка ДНК и являющийся предшественником мРНК. Содержатся в
- 48. Матричная РНК (мРНК) На 5‘-конце – 7-метилгуанозин-5‘-фосфат. 5‘UTR-нетранслирующий регион Инициирующий кодон – AUG CDS-кодирующая последовательность Терминирующий
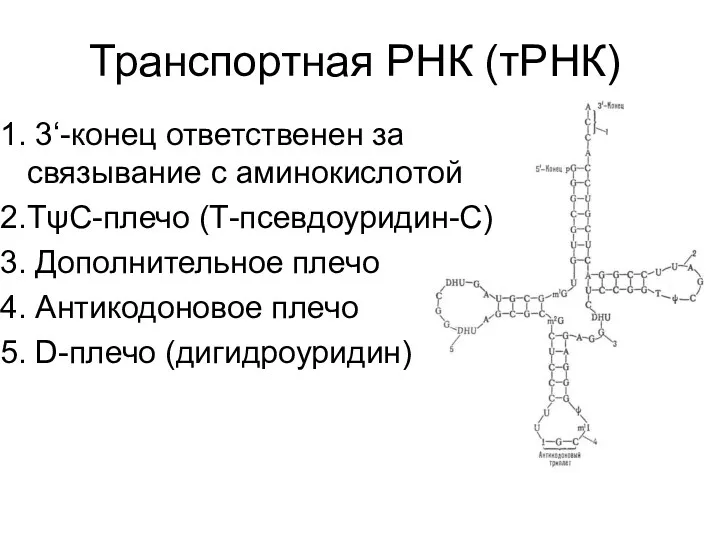
- 49. Транспортная РНК (тРНК) 3‘-конец ответственен за связывание с аминокислотой ТψС-плечо (Т-псевдоуридин-С) Дополнительное плечо Антикодоновое плечо D-плечо
- 50. Рибосомальная РНК (рРНК) 5 S кодируется отдельным геном 5,8 S 28 S считываются с одного гена
- 51. Малые РНК (sRNA) Описаны только у эукариот. Содержат до 300 нуклеотидов До 106 на клетку. тмРНК
- 52. Малые РНК (sRNA) Описаны только у эукариот. Содержат до 300 нуклеотидов До 106 на клетку Функции:
- 53. Липиды - разнородная группа органических веществ, нерастворимые в воде, но хорошо растворимые в неполярных растворителях. Омыляемые
- 54. Жирные кислоты Гидрофобные участки мембранных липидов представлены остатками высших карбоновых кислот. В составе жирных кислот выделяют
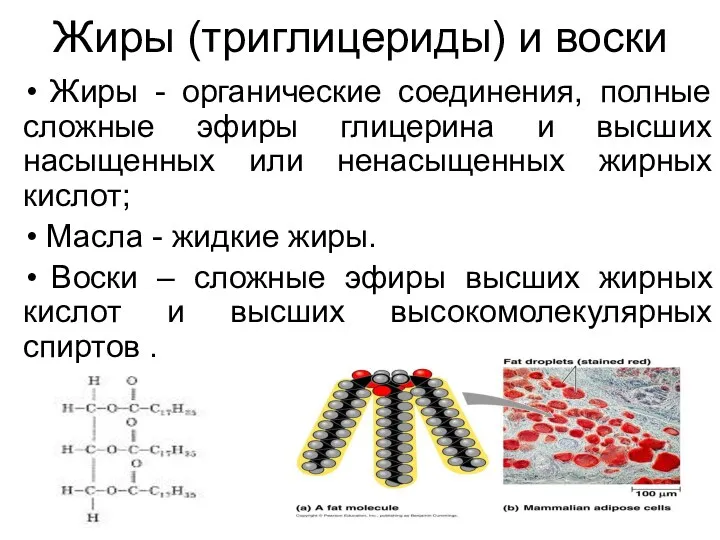
- 55. Жиры (триглицериды) и воски Жиры - органические соединения, полные сложные эфиры глицерина и высших насыщенных или
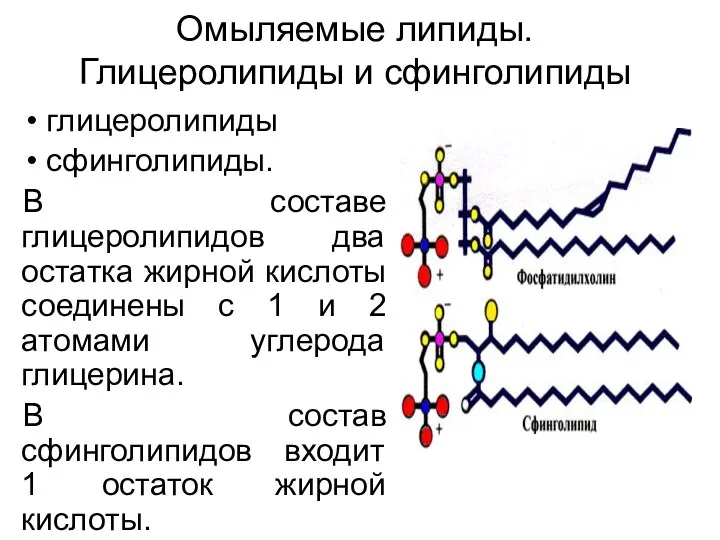
- 56. Омыляемые липиды. Глицеролипиды и сфинголипиды глицеролипиды сфинголипиды. В составе глицеролипидов два остатка жирной кислоты соединены с
- 57. Фосфолипиды и гликолипиды К свободной 3 ОН-группе глицерина и ОН-группе сфингозина, может присоединиться остаток фосфорной кислоты
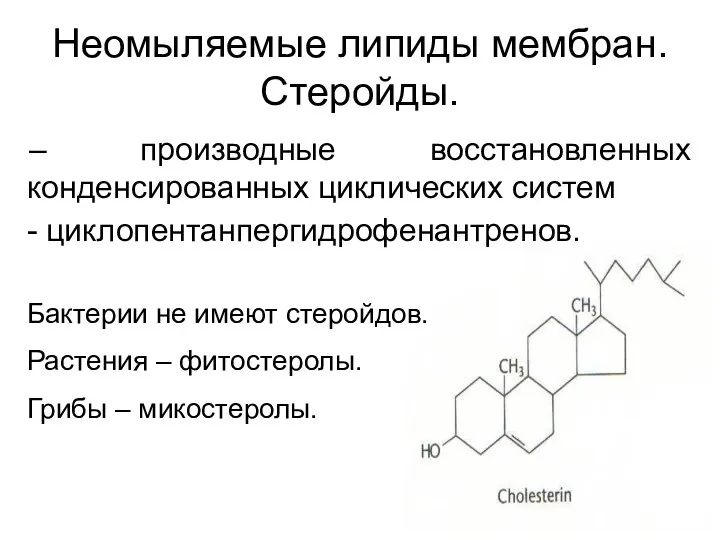
- 58. Неомыляемые липиды мембран. Стеройды. – производные восстановленных конденсированных циклических систем - циклопентанпергидрофенантренов. Бактерии не имеют стеройдов.
- 59. Функции липидов Структурная Барьерная Энергетическая Терморегуляция Запасание воды Синтез витаминов Синтез гормонов Синтез желчных кислот
- 61. Скачать презентацию























 Полимеры. Основные понятия
Полимеры. Основные понятия Химия и современный быт человека
Химия и современный быт человека Аммиак. 9 класс
Аммиак. 9 класс Алканы: метан, пропан, этан, бутан
Алканы: метан, пропан, этан, бутан Значение периодического закона
Значение периодического закона Періодична система хімічних елементів
Періодична система хімічних елементів Дәріс тақырыбы: Кіріспе. Аналитикалық химия пәні. Сапалық талдау әдістері
Дәріс тақырыбы: Кіріспе. Аналитикалық химия пәні. Сапалық талдау әдістері Каменный уголь. Физические и химические свойства
Каменный уголь. Физические и химические свойства Изомерия. (11 класс)
Изомерия. (11 класс) драгоценные и поделочные
драгоценные и поделочные Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Почему мыло пенится
Почему мыло пенится Физическая химия. Химическая термодинамика
Физическая химия. Химическая термодинамика Состав краски
Состав краски Титриметриялық анализ. Жіктелуі. Қышқылдықнегіздік титрлеу. Алкалиметрия және ацидометрия. Реакцияларға қойылатын талаптар
Титриметриялық анализ. Жіктелуі. Қышқылдықнегіздік титрлеу. Алкалиметрия және ацидометрия. Реакцияларға қойылатын талаптар Классификация полимеров
Классификация полимеров Вода
Вода Оксид серы (VI). Серная кислота
Оксид серы (VI). Серная кислота Изделия из металлов
Изделия из металлов Этот многоликий цинк
Этот многоликий цинк Решение задач по теме: «Электролиз»
Решение задач по теме: «Электролиз» Общие проблемы определения низких концентраций
Общие проблемы определения низких концентраций Свойства простых веществ в свете ОВР
Свойства простых веществ в свете ОВР Различные теории кислот и оснований
Различные теории кислот и оснований Азотсодержащие соединения
Азотсодержащие соединения Железо. Fe (лат. Феррум)
Железо. Fe (лат. Феррум) Кремний және оның қосылыстары
Кремний және оның қосылыстары Озон. Значение Озона
Озон. Значение Озона