Содержание
- 2. Вода Воде была дана волшебная власть стать соком жизни на Земле. Леонардо да Винчи
- 3. Содержание Тест Вода в природе Применение воды Круговорот воды Физические свойства воды Химические свойства воды
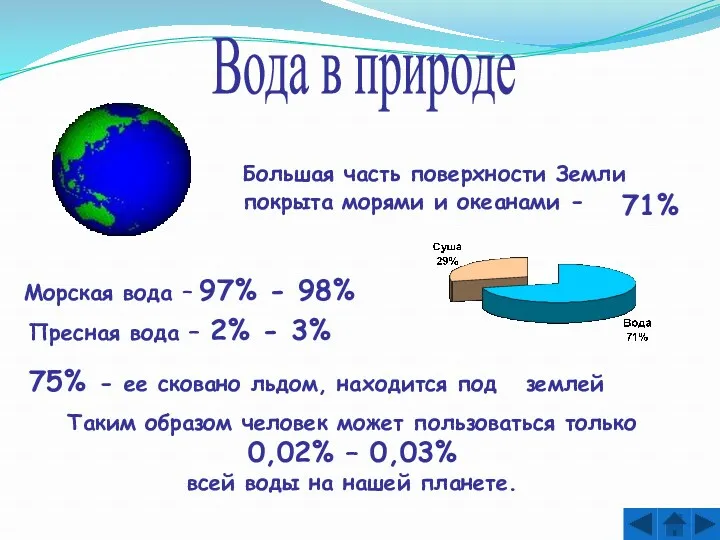
- 4. Вода в природе Большая часть поверхности Земли покрыта морями и океанами - 71% Морская вода –
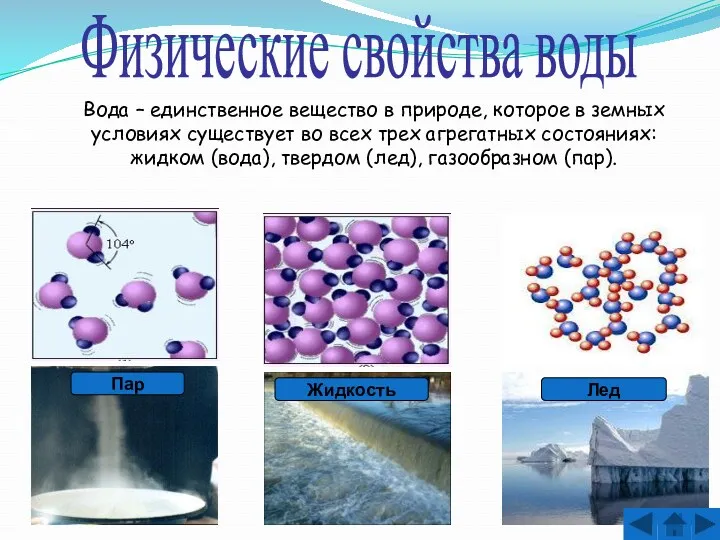
- 5. Физические свойства воды Вода – единственное вещество в природе, которое в земных условиях существует во всех
- 6. Вода в организме человека Кровь человека на 90% состоит из воды Мышцы на 75% Кости на
- 7. Вода в организме человека Обезвоживание организма на 12 – 15 % приводит к нарушению обмена веществ,
- 8. Аномалии воды Лёд плавает на поверхности водоёма, ρ(льда) = 0,92 г/см3, max ρ(воды) при +4°С =
- 9. Химические свойства
- 10. Взаимодействие с металлами При взаимодействии воды с активными металлами образуется щелочь и водород: 2Na + 2H2О=
- 11. Взаимодействие с неметаллами Вода взаимодействует с некоторыми неметаллами; получающиеся продукты взаимодействия очень разнообразны: C + H2О
- 12. Взаимодействие с основными оксидами Взаимодействие с кислотными оксидами Некоторые оксиды металлов могут вступать в реакции соединения
- 13. Круговорот воды в природе Вода постоянно испаряется с поверхности наземных водоемов, листьев растений Так возникает водяной
- 14. Применение воды Вода В жизни растений и животных В быту человека Для получения оснований Для получения
- 15. Вода необходима всем живым организмам: растениям, животным и человеку. Без воды нет жизни. Вода – одно
- 16. Берегите воду
- 17. « Вода – у тебя нет ни цвета, ни вкуса, ни запаха, тебя невозможно описать, тобою
- 18. Вода в природе
- 19. Тест по теме «Вода» Вопрос 1 Вопрос 2 Вопрос 3 Вопрос 4 Вопрос 5 Вопрос 6
- 21. Скачать презентацию












 Геохимия, как наука
Геохимия, как наука Изомерия и ее виды
Изомерия и ее виды Химия атмосферы. Химические процессы в тропосфере
Химия атмосферы. Химические процессы в тропосфере Химическое равновесие. Принцип Ле Шателье
Химическое равновесие. Принцип Ле Шателье Аппаратчик химводоочистки. Билеты для экзамена с ответами (1-16)
Аппаратчик химводоочистки. Билеты для экзамена с ответами (1-16) Простые вещества — металлы и неметаллы
Простые вещества — металлы и неметаллы Обмен липидов
Обмен липидов Минерал родонит. Месторождения
Минерал родонит. Месторождения Органические вещества. Валентность. Теория химического строения
Органические вещества. Валентность. Теория химического строения Атом. Будова атома
Атом. Будова атома Ионные уравнения реакции
Ионные уравнения реакции Строение атома
Строение атома Основные классы неорганических веществ. Соединения химических элементов
Основные классы неорганических веществ. Соединения химических элементов Минералды тыңайтқыштар өндірісі
Минералды тыңайтқыштар өндірісі Комплексные соединения
Комплексные соединения 20230306_gidroliz
20230306_gidroliz Современные химические технологии
Современные химические технологии Материаловедение. Химия функциональных материалов
Материаловедение. Химия функциональных материалов Водород
Водород Углеводы (сахариды)
Углеводы (сахариды) Основные сырьевые материалы для производства портландцемента
Основные сырьевые материалы для производства портландцемента Rate of reactions. (Chapter 2)
Rate of reactions. (Chapter 2) Комплесные соединения
Комплесные соединения Oxidation – Reduction Reaction
Oxidation – Reduction Reaction Органічні розчинники
Органічні розчинники Азот и его соединения. Повторение
Азот и его соединения. Повторение Лекция 8. Электрохимия
Лекция 8. Электрохимия Элементы IV группы главной подгруппы. Углерод
Элементы IV группы главной подгруппы. Углерод