Содержание
- 2. Органические Получены из продуктов жизнедеятельности растительных и животных Организмов (сахар, жиры, масла, красители и др.), а
- 3. Раздел химии, который изучает органические вещества, стали называть «органической химией» Так как в состав каждого органического
- 4. Органические вещества имеют ряд особенностей: Их гораздо больше, чем неорганических веществ; Орг. вещества имеют более сложное
- 5. Валентность Понятие валентности в органической химии более полезно, чем термин «степень окисления», характерный для неорганической химии.
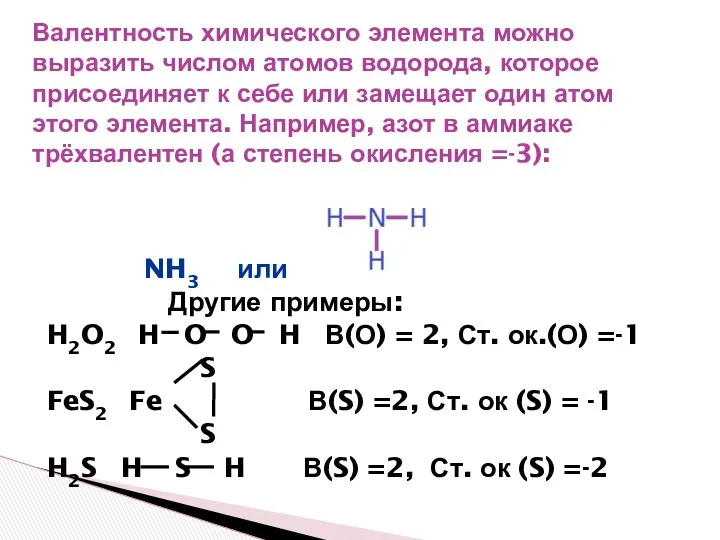
- 6. Валентность химического элемента можно выразить числом атомов водорода, которое присоединяет к себе или замещает один атом
- 7. В отличии от степени окисления, валентность не имеет знака и не может быть равна нулю. Часто
- 8. 3.Теория химического строения Для органической химии основополагающей стала теория химического строения (ТХС) органических веществ А.М. Бутлерова,
- 9. Основные положения ТХС: Запомни! Углерод в органических соединениях всегда четырёхвалентен. 1) Атомы в молекулах органических веществ
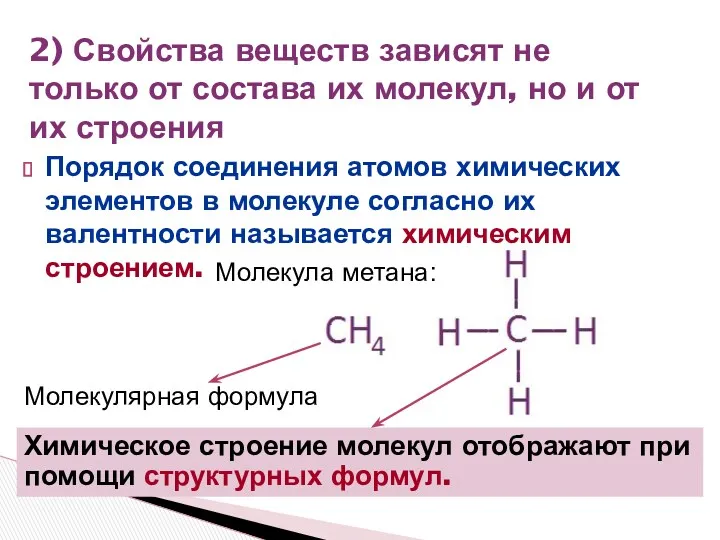
- 10. Порядок соединения атомов химических элементов в молекуле согласно их валентности называется химическим строением. 2) Свойства веществ
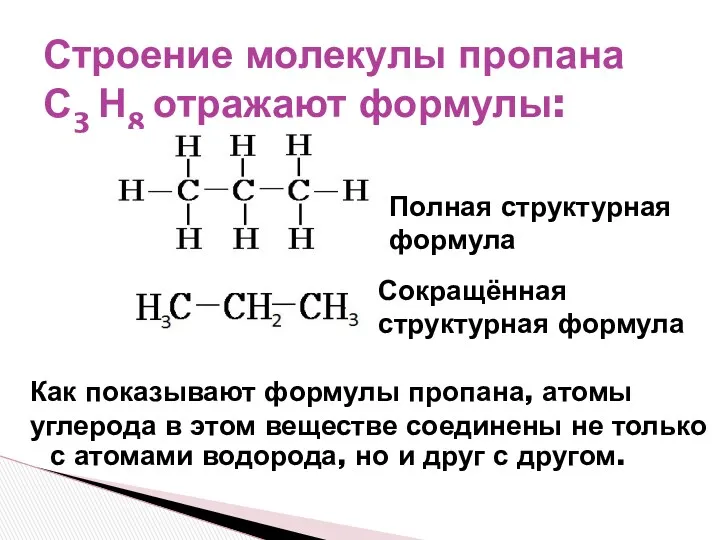
- 11. Строение молекулы пропана С3 Н8 отражают формулы: Как показывают формулы пропана, атомы углерода в этом веществе
- 12. Итак, по теории А.М.Бутлерова Каждое вещество имеет определённое химическое строение; От этого строения зависят и свойства
- 14. Скачать презентацию








 Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды)
Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды) Промежуточные фазы в металлических сплавах
Промежуточные фазы в металлических сплавах Альдегіди. Номенклатура альдегідів
Альдегіди. Номенклатура альдегідів Азот: кислородные соединения. Особенности химии фосфора и элементов его подгруппы
Азот: кислородные соединения. Особенности химии фосфора и элементов его подгруппы Ионные уравнения реакций
Ионные уравнения реакций Получение и применение радиоактивных изотопов
Получение и применение радиоактивных изотопов Карбоновые кислоты и их функциональные производные. Хроматографические методы исследования
Карбоновые кислоты и их функциональные производные. Хроматографические методы исследования Степень окисления ОВР
Степень окисления ОВР Вещества и материалы. Классификация веществ. Реакции нейтрализации
Вещества и материалы. Классификация веществ. Реакции нейтрализации Свойства химических элементов и закономерность их изменения
Свойства химических элементов и закономерность их изменения Побочная подгруппа 1 и 2. Медь
Побочная подгруппа 1 и 2. Медь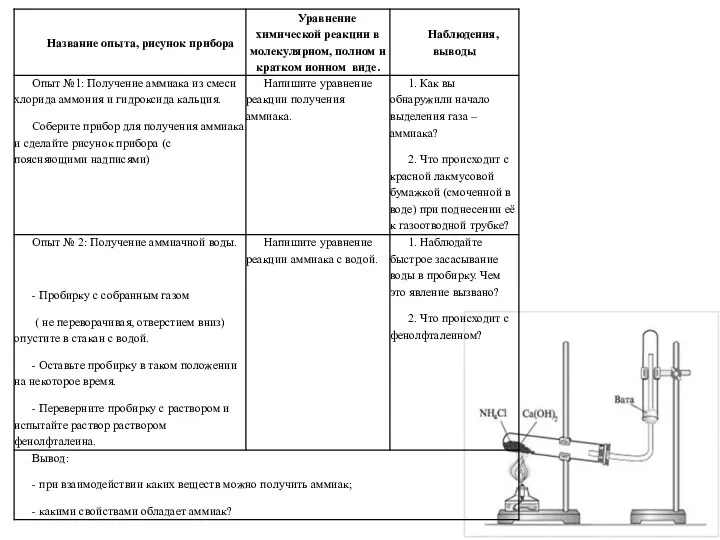 Получение аммиака и изучение его свойств
Получение аммиака и изучение его свойств Полифенолды қосылыстар. Флавоноидтар
Полифенолды қосылыстар. Флавоноидтар Кислород как элемент
Кислород как элемент Соли аммония
Соли аммония Материаловедение и методы диагностики микро- и наноструктурных материалов
Материаловедение и методы диагностики микро- и наноструктурных материалов Растворы ВМС и их свойства
Растворы ВМС и их свойства Химические свойства основных оксидов
Химические свойства основных оксидов Горение топлива
Горение топлива Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Химическая картина мира
Химическая картина мира Карбоновые кислоты
Карбоновые кислоты Комбинированные задачи. 11 класс
Комбинированные задачи. 11 класс Kарбонові кислоти. Гетерофункціональні похідні карбонових кислот
Kарбонові кислоти. Гетерофункціональні похідні карбонових кислот Координационные соединения
Координационные соединения Формы нахождения минералов в природе
Формы нахождения минералов в природе Основы химмотологии моторных топлив. Тема 3
Основы химмотологии моторных топлив. Тема 3 Азотная кислота. Соли азотной кислоты. Получение и применение азотной кислоты. Урок 43
Азотная кислота. Соли азотной кислоты. Получение и применение азотной кислоты. Урок 43