Слайд 2

ШПАРГАЛКА
1. Кислая среда определяется при помощи лакмуса(малиновый цвет). Диссоциация кислот происходит
с образованием ионов водорода
HNO3 = H+ +NO3-
2.Щелочи диссоциируют с образованием гидроксид-ионов, они и окрашивают лакмус в синий цвет
KOH = K+ +OH-
3.В нейтральной среде количество ионов водорода и гидрокид-ионов будет одинаковым и поэтому окраска не изменится.
H+ = OH-
Слайд 3

ТЕОРИЯ
Процесс гидролиза – обратимый взаимодействие соли и воды с образованием слабого
электролита. Из 10 миллионов молекул воды на ионы распадается только одна. Ионы соли взаимодействуют с молекулами воды. Для определения среды пользуются водородным показателем – рН. Если рН=7 среда нейтральная, рН больше 7(щелочная), меньше кислотная.
Слайд 4

1.СОЛЬ, ОБРАЗОВАННАЯ СИЛЬНЫМ ОСНОВАНИЕМ И СЛАБОЙ КИСЛОТОЙ
K2CO3 + HOH = HCO3
2- +K+ +OH-
pH, больше 7, среда щелочная, гидролиз по аниону
Слайд 5

СОЛЬ ОБРАЗОВАНА СИЛЬНЫМ ОСНОВАНИЕМ И СИЛЬНОЙ КИСЛОТОЙ
NaCl +HOH =Na+ + Cl-
+ HOH
соль не подвергается гидролизу, среда нейтральная
Слайд 6

СОЛЬ ОБРАЗОВАНА СЛАБЫМ ОСНОВАНИЕМ И СИЛЬНОЙ КИСЛОТОЙ
ZnSO4 + HOH = ZnOH-
+H+ + SO4 2-
гидролиз идет по катиону, среда кислая, рН меньше 7
Слайд 7

СОЛЬ ОБРАЗОВАНА СЛАБЫМ ОСНОВАНИЕМ И СЛАБОЙ КИСЛОТОЙ
MgSO4 + HOH = Mg(OH)2
+ HOH +SO3
Гидролиз идет по катиону и аниону, рН=7, среда нейтральная
Слайд 8

ВЫВОД
Гидролиз это взаимодействие молекул соли и воды.
Слайд 9

ПРАКТИКУМ
ЗАПОЛНИТЕ ТАБЛИЦУ
.Практикум
Заполните таблицу








 Приёмы обращения с лабораторным оборудованием
Приёмы обращения с лабораторным оборудованием Химия биогенных элементов p -блока
Химия биогенных элементов p -блока Периодический закон и периодическая система химических элементов
Периодический закон и периодическая система химических элементов Основные классы неорганических веществ. Соединения химических элементов
Основные классы неорганических веществ. Соединения химических элементов Выделение транс-анетола из эфирных масел
Выделение транс-анетола из эфирных масел Изучение свойств горных пород, минералов и полезных ископаемых
Изучение свойств горных пород, минералов и полезных ископаемых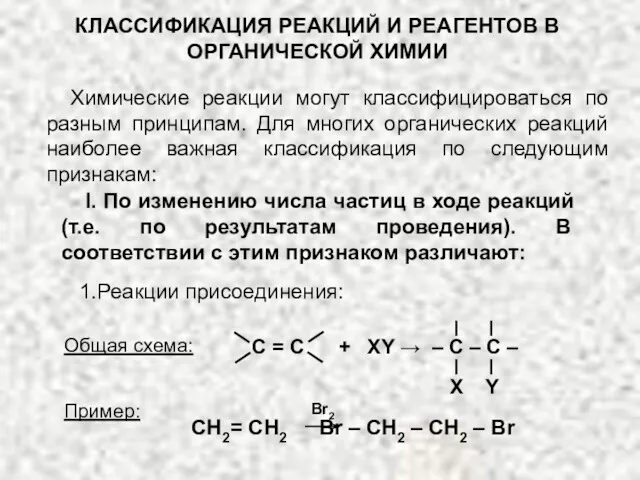 Классификация реакций и реагентов органической химии
Классификация реакций и реагентов органической химии Химическая промышленность
Химическая промышленность Азотсодержащие гетероциклические соединения
Азотсодержащие гетероциклические соединения Химические свойства металлов
Химические свойства металлов Хімічний склад і використання мінералів
Хімічний склад і використання мінералів Химиялық тепе-теңдік және оның ығысуына әсер етуші жағдайлар. Ле Шателье-Браун принциптері
Химиялық тепе-теңдік және оның ығысуына әсер етуші жағдайлар. Ле Шателье-Браун принциптері Окислительно-восстановительные реакции. Лекция 8
Окислительно-восстановительные реакции. Лекция 8 Получение порошков автоклавным осаждением
Получение порошков автоклавным осаждением Обратимость химических реакций. Химическое равновесие и способы его смещения
Обратимость химических реакций. Химическое равновесие и способы его смещения Строение атома
Строение атома Электролиз. Электролизеры
Электролиз. Электролизеры Применение уксусной кислоты
Применение уксусной кислоты Фосфор. Гипофосфатемия и гиперфосфатемия
Фосфор. Гипофосфатемия и гиперфосфатемия Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Розрахунки за хімічними рівняннями
Розрахунки за хімічними рівняннями Установка по переработке углеводородов
Установка по переработке углеводородов Комплексные соединения
Комплексные соединения Физико-химические методы анализа. Лекция 3
Физико-химические методы анализа. Лекция 3 Сера. Аллотропные модификации
Сера. Аллотропные модификации Гидролиз органических и неорганических соединений
Гидролиз органических и неорганических соединений Качественное определение химических элементов в почве
Качественное определение химических элементов в почве Аммиак
Аммиак