Сначала называют комплексный анион.
Число лигандов в анионе обозначается греческими числительными:
2–ди, 3–три, 4–тетра, 5–пента, 6–гекса и т.д.,
далее следуют названия лигандов, к которым прибавляют соединительную гласную «о»: Cl– – хлоро-, CN– – циано-, OH– – гидроксо- и т.п.
Если у комплексообразователя переменная степень окисления, то в скобках римскими цифрами указывают его степень окисления, а его название с суффиксом -ат: Zn – цинкат, Fe – феррат(III), Au – аурат(III).
2. Последним называют катион внешней сферы в родительном падеже.
Номенклатура
названия комплексных соединений
![СТРОЕНИЕ на примере тетрагидроксоалюмината натрия(Na[Al(OH)4]) Al OH OH HO HO](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/604/slide-1.jpg)
![СТРОЕНИЕ на примере сульфата тетраамминмеди(2) ([Cu(NH3)4]SO4) Cu NH3 NH3 NH3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/604/slide-2.jpg)

 Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Утворення асимілятів та їхнє перетворення
Утворення асимілятів та їхнє перетворення Алгоритм определения вида связи по формуле вещества
Алгоритм определения вида связи по формуле вещества Полипропилен
Полипропилен Буферные растворы. Граф структуры. Теория электрической диссоциации. Химическое равновесие
Буферные растворы. Граф структуры. Теория электрической диссоциации. Химическое равновесие Алкены. Непредельные углеводороды ряда этилена
Алкены. Непредельные углеводороды ряда этилена 20230306_gidroliz
20230306_gidroliz Хімічні властивості солей
Хімічні властивості солей Строение атома. 10 ен
Строение атома. 10 ен Чистые вещества. Смеси. Способы разделения смесей (7 класс)
Чистые вещества. Смеси. Способы разделения смесей (7 класс) Способы выражения состава раствора. Задача 7
Способы выражения состава раствора. Задача 7 Алкены. Гомологический ряд и изомерия
Алкены. Гомологический ряд и изомерия Углеводы, липиды
Углеводы, липиды Способы производства железоуглеродистых сплавов
Способы производства железоуглеродистых сплавов Подгруппа азота
Подгруппа азота Проект Кабинет химии будущего
Проект Кабинет химии будущего Органическая химия. Лекция - Оксокислоты
Органическая химия. Лекция - Оксокислоты Практическая работа №1. Приготовление раствора с определенной массовой долей соли
Практическая работа №1. Приготовление раствора с определенной массовой долей соли Титан және титан қорытпалары. Деформацияланған және кұйма титан қорытпалары
Титан және титан қорытпалары. Деформацияланған және кұйма титан қорытпалары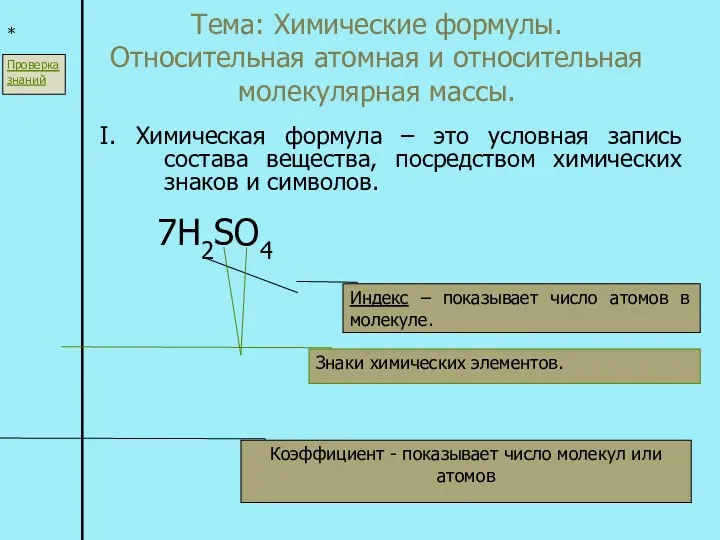 Химические формулы. Относительная атомная и относительная молекулярная массы
Химические формулы. Относительная атомная и относительная молекулярная массы Алкены. Номенклатура. Строение молекулы
Алкены. Номенклатура. Строение молекулы Химия в строительстве
Химия в строительстве Валентность химических элементов
Валентность химических элементов Химическая наука и промышленность в годы ВОВ
Химическая наука и промышленность в годы ВОВ Фосфор и его соединения. 9 класс
Фосфор и его соединения. 9 класс Синтез и химические модификации индиго
Синтез и химические модификации индиго Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ
Об изучении окислительно-восстановительных реакций в школьном курсе химии. Степени окисления атомов и формулы веществ Тема 7-Карбоновые кислоты
Тема 7-Карбоновые кислоты