Содержание
- 2. Подгруппа меди (медь, серебро, золото) Подгруппа цинка (цинк, кадмий, ртуть) Переходные металлы (хром, марганец, молибден, вольфрам
- 3. Особенностью является наличие заполненного предвнешнего d-подуровня, достигаемое за счёт перескока электрона с внешнего s-подуровня. Причина такого
- 4. при 400–500°С : 2Cu + O2 = 2CuO; при 1000°С : 4Cu + O2 = 2Cu2O
- 5. Растворяется в разбавленной азотной кислоте: 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O Реагирует с
- 6. Соли Cu2+ обычно окрашены в голубой или зеленоватый цвет. Образование нерастворимого гидроксида меди (II) голубого цвета:
- 7. При обычных условиях реагирует с серой, образуя сульфид серебра (I): 2Ag + S = Ag2S, при
- 8. Образование белого творожистого осадка Ag+ + Cl- = AgCl↓, растворимого в гидрате аммиака AgCl + 2NH4OH
- 9. Цинк [Ar] 3d10 4s2 хрупкий переходный металл голубовато-белого цвета (тускнеет на воздухе, покрываясь тонким слоем оксида
- 10. На воздухе покрывается оксидной пленкой, при сильном нагреве горит голубоватым пламенем 2Zn + O2 = 2ZnO
- 11. Типичный переходный элемент. Zn + 2H2SO4 = ZnSO4 + SO2 + 2H2O; Zn + 4HNO3 =
- 12. Образование нерастворимого основания Zn2+ + 2OH- = Zn(OH)2↓ + 2OH- = [Zn(OH)4]2- осадок белого цвета, растворимый
- 13. Эл. Конфигурация [Ar] 3d5 4s1 В свободном виде — голубовато-белый металл с кубической решеткой, один из
- 14. Оксид хрома (2) - СrО – твердое ярко – красное вещество, типичный основной оксид (ему соответствует
- 15. Наиболее устойчивая с.о. хрома. Оксид хрома (3) - Сr2О3 нерастворим в воде, тугоплавкий, по твёрдости близок
- 16. Оксид хрома (6) - СrО3 – темно – красное кристаллическое вещество, хорошо растворимо в воде, типичный
- 17. В кислой среде раствора хроматы переходят в дихроматы: 2К2СrО4 + Н2SО4 = К2Сr2О7 + К2SО4 +
- 18. Окислительные свойства Cr 6+ Дихроматы – сильные окислители. Под действием восстановителей в кислой среде переходят в
- 19. Электронная конфигурация [Ar] 3d5 4s2 Простое вещество марганец — металл серебристо-белого цвета. Наряду с железом и
- 20. Степени окисления и соединения Алюминотермическим методом, восстанавливая оксид Mn2O3, образующийся при прокаливании пиролюзита: Получение марганца
- 21. Соли Mn 2+ MnCl2 MnSO4
- 22. Соединения Mn 4+
- 23. Соединения Мn 7+
- 25. Скачать презентацию







![Цинк [Ar] 3d10 4s2 хрупкий переходный металл голубовато-белого цвета (тускнеет](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/295500/slide-8.jpg)



![Эл. Конфигурация [Ar] 3d5 4s1 В свободном виде — голубовато-белый](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/295500/slide-12.jpg)





![Электронная конфигурация [Ar] 3d5 4s2 Простое вещество марганец — металл](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/295500/slide-18.jpg)




 Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс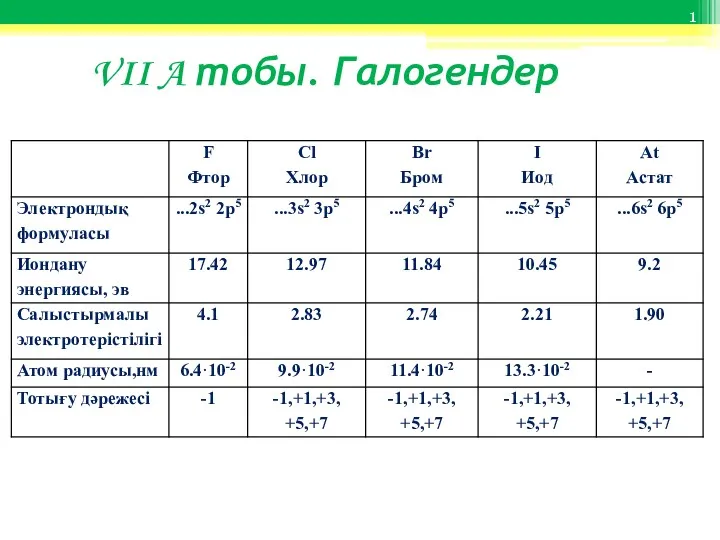 VII A тобы. Галогендер
VII A тобы. Галогендер Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ
Рекомендации по оформлению развёрнутых ответов на задания ЕГЭ МОЛЯРНЫЙ ОБЪЕМ Химия 8 класс
МОЛЯРНЫЙ ОБЪЕМ Химия 8 класс Химия өнеркәсібіндегі энергетикалық ресурстар
Химия өнеркәсібіндегі энергетикалық ресурстар Химическая связь. Валентность элементов в ковалентных соединениях. Степень окисления элементов
Химическая связь. Валентность элементов в ковалентных соединениях. Степень окисления элементов Процесс оксихлорирования
Процесс оксихлорирования Растворы. Классификация, способы выражения концентрации, свойства растворов
Растворы. Классификация, способы выражения концентрации, свойства растворов Гидроочистка нефти и газа
Гидроочистка нефти и газа Основные типы химический реакций
Основные типы химический реакций Теория электролитической диссоциации
Теория электролитической диссоциации Межмолекулярные силы (силы Ван дер Ваальса)
Межмолекулярные силы (силы Ван дер Ваальса) Простые эфиры
Простые эфиры Аллотропные модификации углерода. Алмазы
Аллотропные модификации углерода. Алмазы Введение. Методы и средства обучения химии
Введение. Методы и средства обучения химии Нанохимия
Нанохимия Карбонові кислоти. Хімія. 9 клас
Карбонові кислоти. Хімія. 9 клас Гетероциклические соединения. Пятичленные гетероциклы
Гетероциклические соединения. Пятичленные гетероциклы Кислородные соединения азота
Кислородные соединения азота Взаємодія кисню із складними речовинами
Взаємодія кисню із складними речовинами Химические элементы и организм человека
Химические элементы и организм человека Основные классы неорганических соединений. Тема 2
Основные классы неорганических соединений. Тема 2 Физико-химические свойства белков. Количественные (колориметрические) методы определения концентрации белка
Физико-химические свойства белков. Количественные (колориметрические) методы определения концентрации белка Аналитические методы
Аналитические методы Средства бытовой химиии
Средства бытовой химиии Химический элемент. Электронное строение атома
Химический элемент. Электронное строение атома Кристалічна ґрадка. Встановити взаємозв’язок між будовою речовин та їх фізичними властивостями
Кристалічна ґрадка. Встановити взаємозв’язок між будовою речовин та їх фізичними властивостями Ароматические углеводороды
Ароматические углеводороды