Содержание
- 2. Сложные вещества Оксиды Кислоты Основания Соли Основные Кислотные Амфотерные Бескислородные Кислородсодержащие Щелочи Нерастворимые в воде Средние
- 3. Вещества, образованные атомами двух элементов, одним из которых является кислород Оксиды
- 4. Вещества, молекулы которых состоят из одного или нескольких атомов водорода, способных замещаться на атомы металлов, и
- 5. Вещества, образованные атомами металлов и гидроксогруппами. Основания
- 6. Вещества, образованные атомами металлов и кислотными остатками. Соли
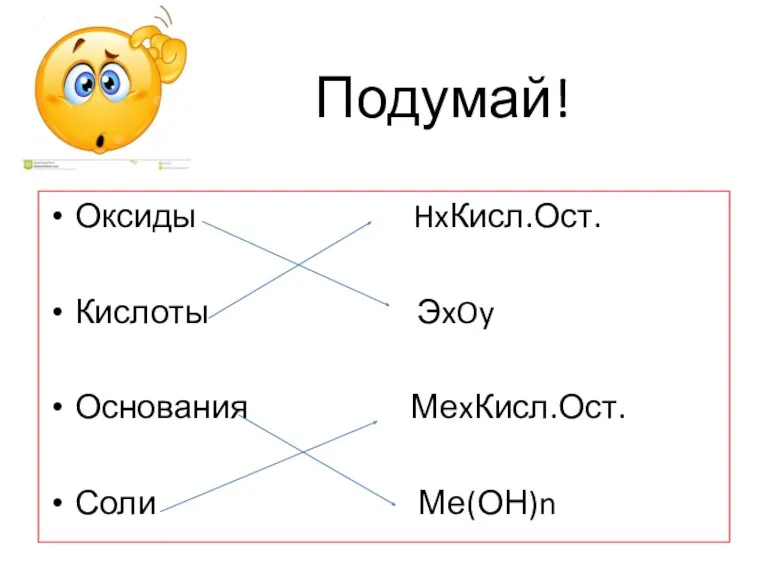
- 7. Подумай! Оксиды HxКисл.Ост. Кислоты ЭxOy Основания МеxКисл.Ост. Соли Ме(ОН)n
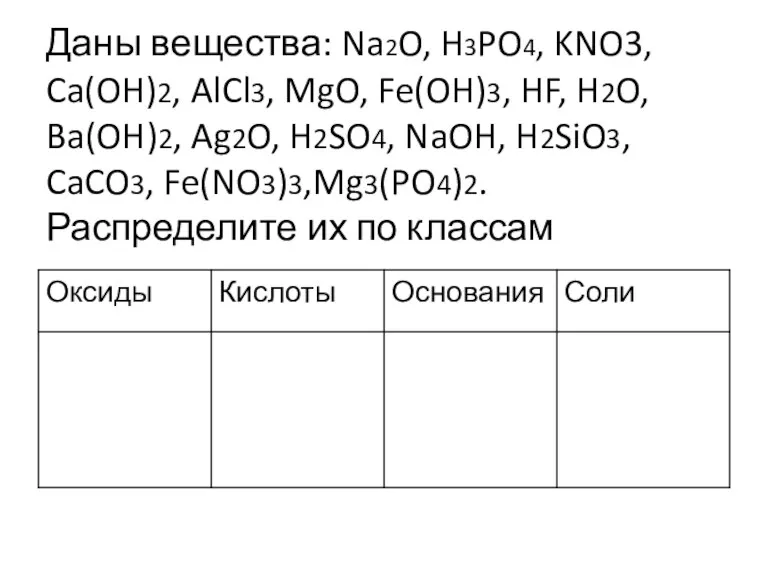
- 8. Даны вещества: Na2O, H3PO4, KNO3, Ca(OH)2, AlCl3, MgO, Fe(OH)3, HF, H2O, Ba(OH)2, Ag2O, H2SO4, NaOH, H2SiO3,
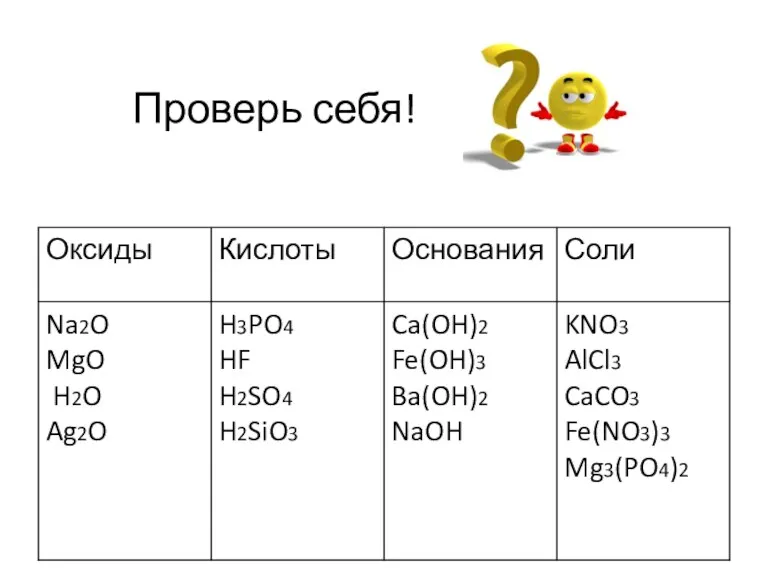
- 9. Проверь себя!
- 10. Химические свойства неорганических веществ
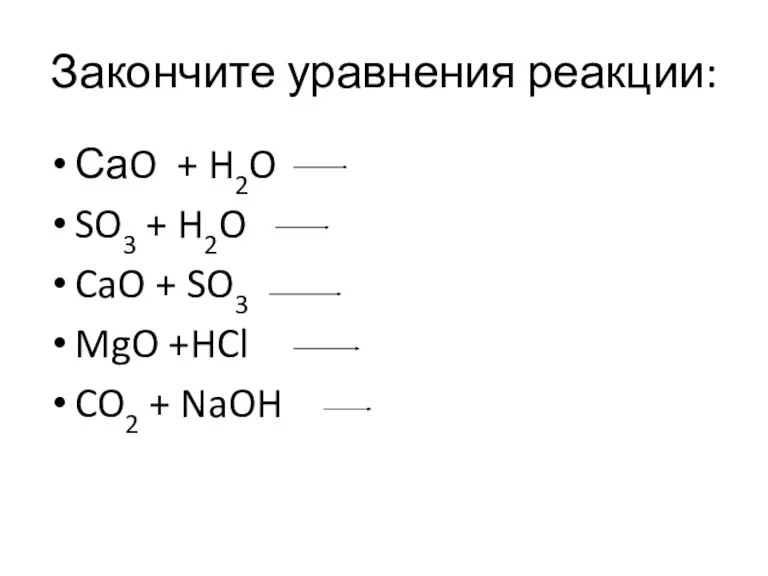
- 11. Закончите уравнения реакции: СаO + H2O SO3 + H2O CaO + SO3 MgO +HCl CO2 +
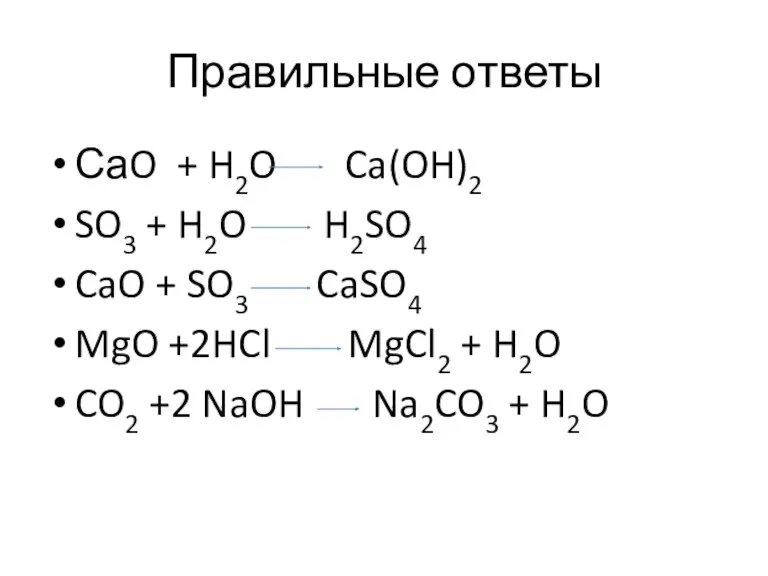
- 12. Правильные ответы СаO + H2O Ca(OH)2 SO3 + H2O H2SO4 CaO + SO3 CaSO4 MgO +2HCl
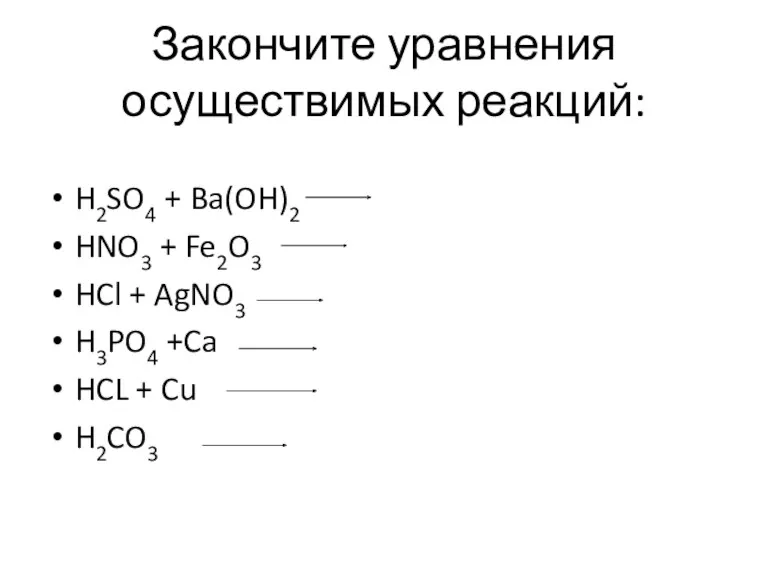
- 13. Закончите уравнения осуществимых реакций: H2SO4 + Ba(OH)2 HNO3 + Fe2O3 HCl + AgNO3 H3PO4 +Ca HCL
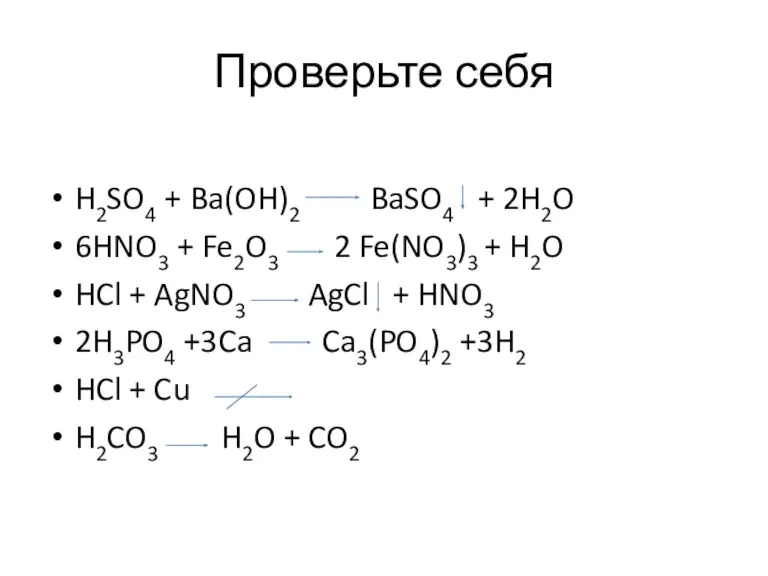
- 14. Проверьте себя H2SO4 + Ba(OH)2 BaSO4 + 2H2O 6HNO3 + Fe2O3 2 Fe(NO3)3 + H2O HCl
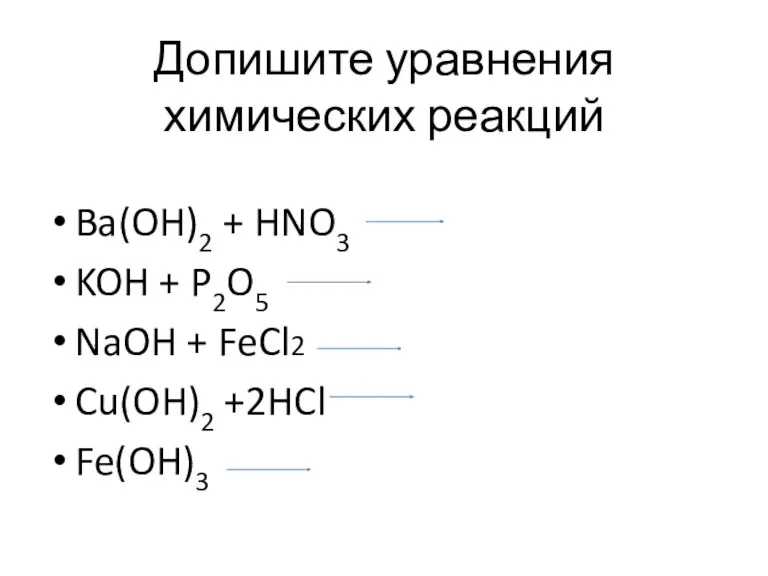
- 15. Допишите уравнения химических реакций Ba(OH)2 + HNO3 KOH + P2O5 NaOH + FeCl2 Cu(OH)2 +2HCl Fe(OH)3
- 16. Химические свойства оснований Ba(OH)2 + 2HNO3 Ba(NO)2 + 2H2O 6KOH + P2O5 2 K3PO4 + 3H2O
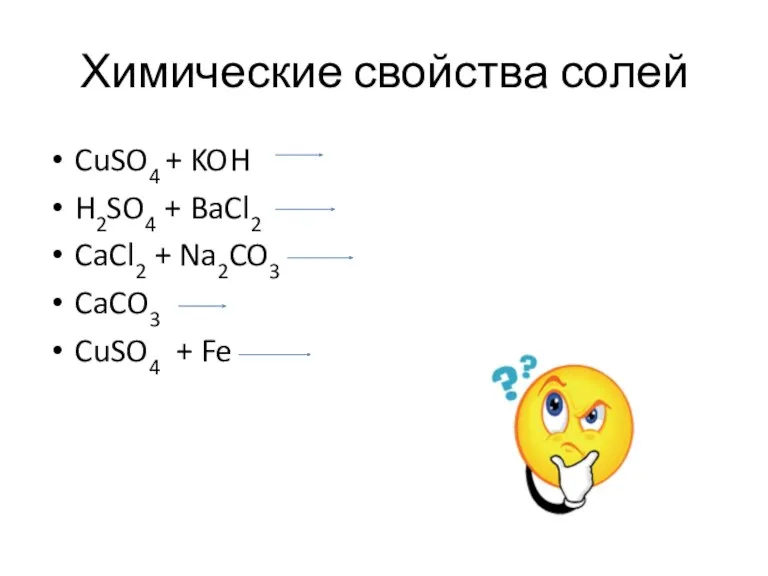
- 17. Химические свойства солей CuSO4 + KOH H2SO4 + BaCl2 CaCl2 + Na2CO3 CaCO3 CuSO4 + Fe
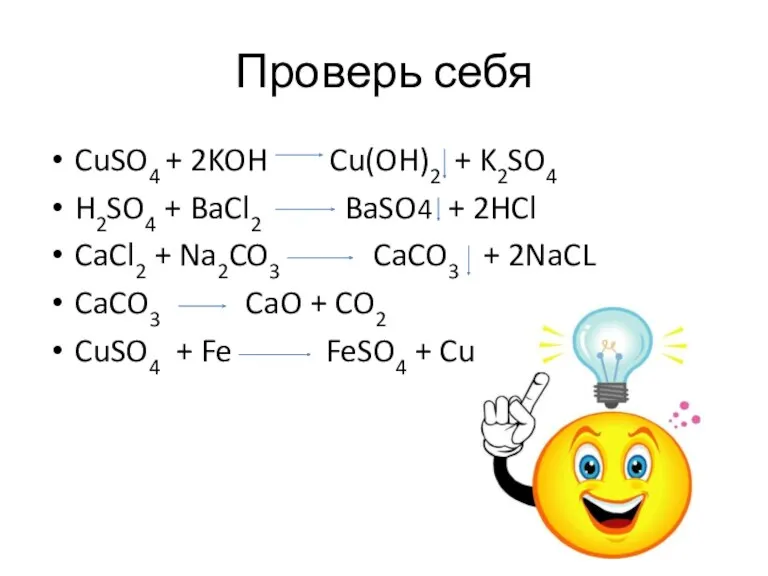
- 18. Проверь себя CuSO4 + 2KOH Cu(OH)2 + K2SO4 H2SO4 + BaCl2 BaSO4 + 2HCl CaCl2 +
- 19. ТЕСТ 1) Из предложенного перечня выберите основной оксид а) K2O б) SO3 в) CO2 2) В
- 20. ОТВЕТЫ ТЕСТА 1) А 2) А 3) В 4) Б 5) А 6) Б Критерии оценки:
- 21. Источники информации 1.Кузнецова Н.Е.Химия 8класс.Изд.центр. «Вентана-Граф».2007г. 2.Кузнецова Н.Е.Задачник по химии 8 класс 8класс.Изд.центр. «Вентана-Граф».2007г.
- 23. Скачать презентацию










 Фракционирование клеточных экстрактов
Фракционирование клеточных экстрактов Історія відкриття періодичної системи хімічних елементів
Історія відкриття періодичної системи хімічних елементів Роль хімічних знань у пізнанні природи
Роль хімічних знань у пізнанні природи Изотопы химических элементов
Изотопы химических элементов Элементы второй группы главной подгруппы
Элементы второй группы главной подгруппы Кристаллическое строение и свойства металлов
Кристаллическое строение и свойства металлов Термический анализ
Термический анализ Водородная связь
Водородная связь Общие свойства металлов
Общие свойства металлов Оценка опасности взрыва горючих газов
Оценка опасности взрыва горючих газов Удивительные свойства воды
Удивительные свойства воды Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Способи очищення води в побуті
Способи очищення води в побуті Классификация неорганических веществ. Оксиды и основания
Классификация неорганических веществ. Оксиды и основания Экспедиция Изучай мир. Содержание углекислого газа в воздухе
Экспедиция Изучай мир. Содержание углекислого газа в воздухе Полимеры. Пластмассы. Волокна
Полимеры. Пластмассы. Волокна Эмульсиялардың тұрақтылығына полиэтиленгликоль-баз композицияларының әсері
Эмульсиялардың тұрақтылығына полиэтиленгликоль-баз композицияларының әсері Классификация полимеров
Классификация полимеров Основы химической кинетики
Основы химической кинетики Строение атома кремния
Строение атома кремния Основания. 8 класс
Основания. 8 класс Тотығу-тотықсыздану титрлеу әдісі
Тотығу-тотықсыздану титрлеу әдісі Химические свойства алкенов
Химические свойства алкенов Химия окружающей среды
Химия окружающей среды Получение наночастиц в сверхкритическом флюиде
Получение наночастиц в сверхкритическом флюиде Аморфные материалы
Аморфные материалы Історичні відомості про способи класифікації хімічних елементів. Поняття про лужні метали, галогени, інертні гази
Історичні відомості про способи класифікації хімічних елементів. Поняття про лужні метали, галогени, інертні гази Химия и проблемы экологии. Кислотные дожди
Химия и проблемы экологии. Кислотные дожди