Слайд 2

ИЗОТОПЫ
Изотопы – это разновидности атомов одного химического элемента, которые отличаются числом
нейтронов в ядре, то есть массой ядра
Слайд 3

ХИМИЧЕСКИЙ ЭЛЕМЕНТ представляет собой совокупность его изотопов
Слайд 4
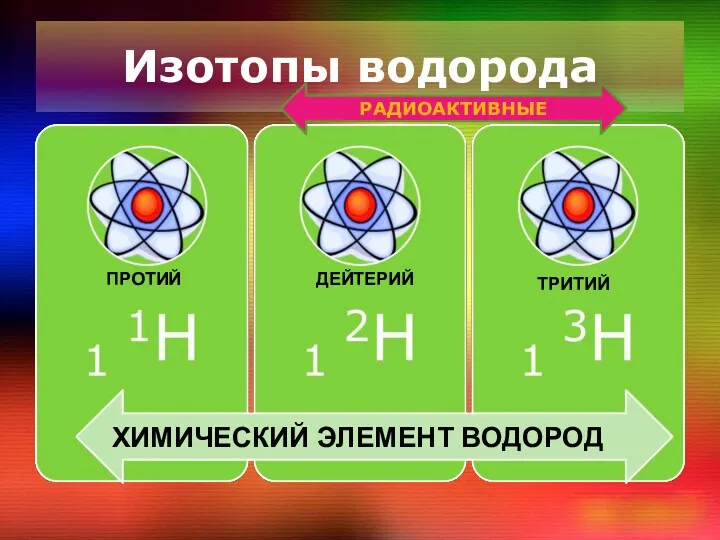
Изотопы водорода
ХИМИЧЕСКИЙ ЭЛЕМЕНТ ВОДОРОД
ПРОТИЙ
ДЕЙТЕРИЙ
ТРИТИЙ
РАДИОАКТИВНЫЕ
Слайд 5

ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ, КОТОРЫЕ СОСТОЯТ ТОЛЬКО ИЗ РАДИОАКТИВНЫХ ИЗОТОПОВ, НАЗЫВАЮТСЯ РАДИОАКТИВНЫМИ
(порядковые номера
более 83)
Слайд 6

Почему относительная атомная масса выражается не целым числом?
ОТНОСИТЕЛЬНАЯ АТОМНАЯ МАССА
ХИМИЧЕСКОГО ЭЛЕМЕНТА РАССЧИТЫВАЕТСЯ С УЧЕТОМ РАСПРОСТРАНЕННОСТИ ЕГО ИЗОТОПОВ В ПРИРОДЕ
Слайд 7

Например,
Хлор в природе встречается в виде изотопов 35Cl (75%) и 37Cl
(25%)
Вычислите относительную атомную массу хлора:
Ar = 35∙0,75 + 37∙0,25 = 35,5






 Средние породы. Типичный андезитовый вулкан
Средние породы. Типичный андезитовый вулкан Учение об агрегатных состояниях вещества. Жидкое состояние. Твердое состояние. Плазма
Учение об агрегатных состояниях вещества. Жидкое состояние. Твердое состояние. Плазма Общие представления о фазовых состояниях и фазовых переходах полимеров
Общие представления о фазовых состояниях и фазовых переходах полимеров Кремний и его соединения. Нахождение в природе
Кремний и его соединения. Нахождение в природе Неметаллы: общая характеристика
Неметаллы: общая характеристика Гидролиз солей
Гидролиз солей Алкандар,жалпы формуласы, гомологтық қатары, изомерлері, атаулары
Алкандар,жалпы формуласы, гомологтық қатары, изомерлері, атаулары Полимеры, бумага
Полимеры, бумага Залежність фізичних властивостей речовин від типу кристалічних ґраток
Залежність фізичних властивостей речовин від типу кристалічних ґраток Минеральные удобрения
Минеральные удобрения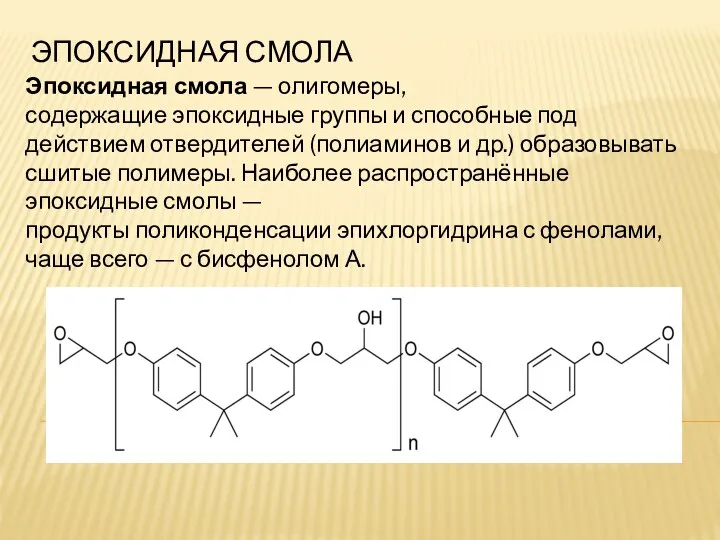 Эпоксидная смола
Эпоксидная смола Предмет органической химии. Органические вещества
Предмет органической химии. Органические вещества Химия в повседневной жизни человека
Химия в повседневной жизни человека Введение в органическую химию
Введение в органическую химию Ерітіндіден заттарды бөлу әдістері
Ерітіндіден заттарды бөлу әдістері Коллигативные свойства растворов
Коллигативные свойства растворов Коррозия металла. Способы защиты от коррозии
Коррозия металла. Способы защиты от коррозии Техника безопасности и правила работы в лаборатории. 10 класс
Техника безопасности и правила работы в лаборатории. 10 класс Вещества и их превращения Роль химии в нашей жизни
Вещества и их превращения Роль химии в нашей жизни Выделение транс-анетола из эфирных масел
Выделение транс-анетола из эфирных масел Качественные реакции на органические вещества
Качественные реакции на органические вещества Распределение электронов в атомах. 8 класс
Распределение электронов в атомах. 8 класс Посуда, ее виды и использование
Посуда, ее виды и использование Титриметрические методы количественного определения лекарственных веществ
Титриметрические методы количественного определения лекарственных веществ Кинетика химических реакций. Химическое равновесие
Кинетика химических реакций. Химическое равновесие Неорганические полимеры
Неорганические полимеры Основные классы неорганических соединений
Основные классы неорганических соединений Гидроксикислоты (оксикислоты)
Гидроксикислоты (оксикислоты)