Основные понятия аналитической химии. Положения теории растворов электролитов и закона действующих масс презентация
Содержание
- 2. План 1. Структура аналитической химии, ее место в системе наук, связанных с практикой. 2. Понятие об
- 3. Литература 1. Основы аналитической химии. В 2-х кн. Учеб. пособие для ВУЗов/ Ю. А. Золотов [и
- 4. Вопрос 1 Структура аналитической химии, ее место в системе наук, связанных с практикой Аналитическая химия –
- 5. Аналитическая служба - система, которая обеспечивает конкретный анализ определённых объектов с использованием методов, рекомендуемых аналитической химией
- 6. Проба – специально отобранная для качественного и количественного анализа часть объекта (образца) Аналиты - определяемые компоненты,
- 7. 1.макроанализ 2.полумикроанализ 3.микроанализ 4.субмикроанализ 5.ультрамикроанализ >0,1 г/10-103 мл 0,01-0,1 г/10-1-10 мл 10-4- 10-3 г/
- 9. Вопрос 2 Понятие об аналитическом сигнале. Аналитические признаки веществ и аналитические реакции. Типы аналитических реакций и
- 10. Единичное определение - однократное выполнение всех последовательных операций, предусмотренных методикой анализа Результат единичного определения - значение
- 11. Методы количественного анализа в зависимости от способа расчёта содержания вещества по величине аналитического сигнала: 1. абсолютные
- 12. Неопределённость и погрешности измерений Погрешность – это разность между данным результатом и истинным значением измеряемой величины
- 14. Основные характеристики методики анализа Воспроизводимость (прецизионность) - степень близости друг к другу независимых результатов измерений при
- 15. Аналитические реакции - химические реакции, результат которых несет определенную аналитическую информацию Классификация аналитических реакции по наблюдаемым
- 16. Вопрос 3 Использование законов термодинамики и кинетики для описания реальных гомогенных и гетерогенных систем Большинство химических
- 17. Активность (a) - такая концентрация вещества в растворе, при использовании которой свойства данного раствора могут быть
- 18. Для характеристики активности электролитов используют следующие коэффициенты активности: - среднеионный коэффициент активности, характеризует поведение электролита в
- 19. Если I Универсального уравнения, с помощью которого можно было бы рассчитать коэффициент активности любого электролита при
- 20. Данное уравнение было получено голландским физиком П. Дебаем и его учеником Э. Хюккелем исходя из следующих
- 21. Для расчёта коэффициентов активности при ионных силах порядка 0,01 - 0,1 используют расширенное уравнение Дебая-Хюккеля: где
- 22. При более высоких значениях ионной силы (до 1) количественную оценку коэффициента активности можно проводить по уравнению
- 23. Константы равновесия, используемые в аналитической химии - концентрационная условная константа равновесия отличается от реальной тем, что
- 24. Равновесная концентрация (обозначают - [ ]) - концентрация определенной формы вещества, участвующего в равновесии Общая концентрация
- 25. Связь между различными видами констант равновесия
- 26. Некоторые из равновесий, используемых в аналитической химии протекают ступенчато. Константы равновесия, характеризующие каждую ступень, называются ступенчатыми.
- 27. Часто вместо значений констант равновесия используют их десятичные логарифмы (если константа очень большая) или отрицательные десятичные
- 29. Скачать презентацию
 Электрохимия. Понятие о двойном электрическом слое (ДЭС)
Электрохимия. Понятие о двойном электрическом слое (ДЭС) Электрохимический ряд напряжений металлов
Электрохимический ряд напряжений металлов Характеристика металу Ферум
Характеристика металу Ферум Виведення формул органічних сполук за масовими частками елементів
Виведення формул органічних сполук за масовими частками елементів Жиры. Сложные эфиры глицерина и высших карбоновых кислот
Жиры. Сложные эфиры глицерина и высших карбоновых кислот Қалдық мөлшерлер
Қалдық мөлшерлер Основные классы неорганических соединений
Основные классы неорганических соединений Самородные элементы
Самородные элементы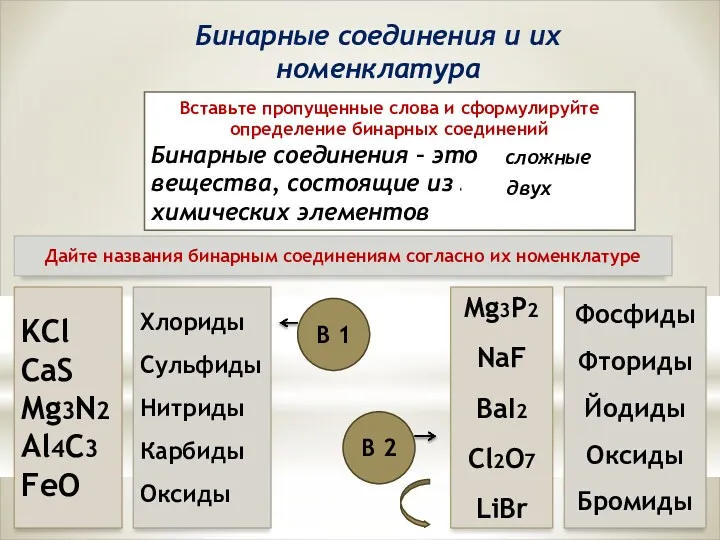 Бинарные соединения и их номенклатура
Бинарные соединения и их номенклатура Биохимические аспекты биотрансформации лекарственных веществ
Биохимические аспекты биотрансформации лекарственных веществ Каучук. История открытия
Каучук. История открытия Нуклеиновые кислоты. Нуклеотиды
Нуклеиновые кислоты. Нуклеотиды Комплексные соединения
Комплексные соединения Генетическая связь между основными классами неорганических соединений
Генетическая связь между основными классами неорганических соединений Горечи. Лекция 3
Горечи. Лекция 3 Технология производства хлорбензола
Технология производства хлорбензола Элементы кристаллохимии
Элементы кристаллохимии Амины. Номенклатура аминов
Амины. Номенклатура аминов Химические свойства кислот в свете теории электролитической диссоциации
Химические свойства кислот в свете теории электролитической диссоциации Азот, фосфор и их соединения
Азот, фосфор и их соединения Необратимые электродные процессы. Часть 2
Необратимые электродные процессы. Часть 2 Поделочные камни
Поделочные камни Химическое равновесие. Смещение химического равновесия
Химическое равновесие. Смещение химического равновесия Адсорбция на пористых адсорбентах. Пористость. Методы получения пористых материалов. Лекция 7
Адсорбция на пористых адсорбентах. Пористость. Методы получения пористых материалов. Лекция 7 Строение и свойства циклоалканов
Строение и свойства циклоалканов Фосфор и его соединения
Фосфор и его соединения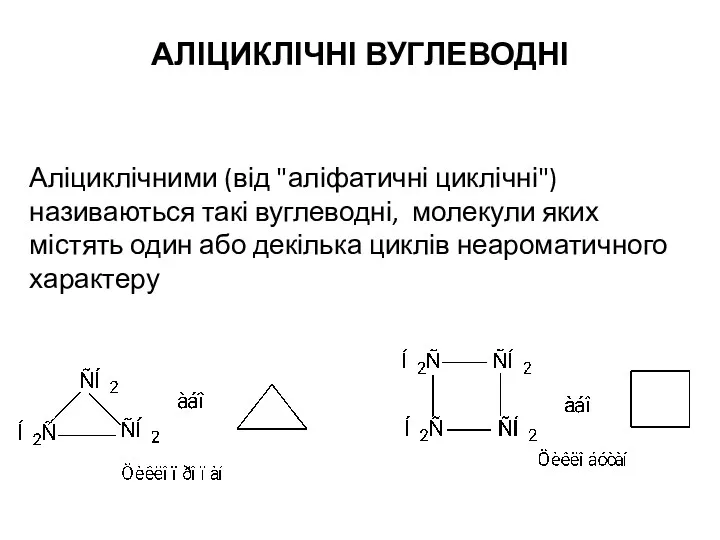 Аліциклічні вуглеводні
Аліциклічні вуглеводні Фунгициды. Достоинства и недостати
Фунгициды. Достоинства и недостати