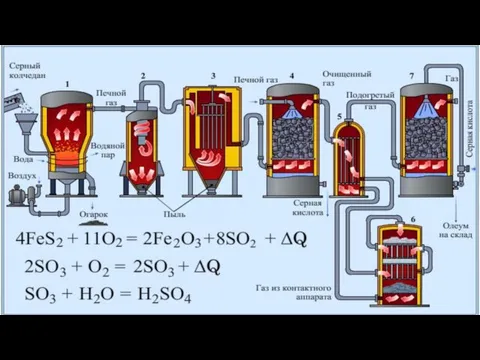
НАУЧНЫЕ СПОСОБЫ ПРОИЗВОДСТВА
I ЭТАП
1. КРУПНЫЕ КУСКИ ПИРИТА ДРОБЯТ, МЕЛКИЕ СПЕКАЮТ.
2.ОБОГАЩАЮТ ВОЗДУХ
КИСЛОРОДОМ, ГОРЕНИЕ В
«КИПЯЩЕМ СЛОЕ».
3. ПРИНЦИП ПРОТИВОТОКА.
3. ТЕПЛООБМЕН, Т.К. ТЕМПЕРАТУРА ВЫШЕ 8000C.
4. ТОЛСТЫЕ СТЕНЫ ПЕЧИ ОБШИТЫ СТАЛЬЮ.
5.МЕХАНИЗАЦИЯ, АВТОМАТИЗАЦИЯ.
II ЭТАП
1. ОЧИСТКА ОТ ПЫЛИ:
“ЦИКЛОН” – ОТ КРУПНЫХ ЧАСТИЦ ПЫЛИ, «ЭЛЕКТРОФИЛЬТР» – ОТ МЕЛКИХ ЧАСТИЦ ПЫЛИ.
3. ОСУШАЮТ ГАЗ В СУШИЛЬНОЙ БАШНЕ .
4. НАГРЕТЬ ДО T=4000 В ТЕПЛООБМЕННИКЕ, ПОНИЖАЮТ ТЕМПЕРАТУРУ ОТ 6000С ДО 4000С.
5. КАТАЛИЗАТОР V2O5 НА КЕРАМИКЕ.
6.ПРОТИВОТОЧНОЕ ДВИЖЕНИЕ.
7.ТЕПЛООБМЕН.
III ЭТАП
1. УВЕЛИЧИВАЮТ ПЛОЩАДЬ СОПРИКОСНОВЕНИЯ (КЕРАМИЧЕСКИЕ КОЛЬЦА РАШИГА).
2.ОТВОДЯТ ПРОДУКТЫ РЕАКЦИИ.
3.ОРОШАЮТ 98% СЕРНОЙ КИСЛОТОЙ, ОБРАЗУЕТСЯ ОЛЕУМ(РАСТВОР SO3 В H2SO4)









 Природный и синтетический каучуки. Резина
Природный и синтетический каучуки. Резина Спектроскопія ямр на ядрах 13с
Спектроскопія ямр на ядрах 13с Способи очищення води в побуті
Способи очищення води в побуті Нитраты в овощах и фруктах
Нитраты в овощах и фруктах Углепластики
Углепластики Темір және оның маңызды қосылыстары
Темір және оның маңызды қосылыстары Решение задач на нахождение молекулярной формулы органических веществ
Решение задач на нахождение молекулярной формулы органических веществ Карбонові кислоти
Карбонові кислоти Аміни
Аміни Радиохимия
Радиохимия Термодинамика химических процессов
Термодинамика химических процессов Титан
Титан Взаємодія кисню зі складними та простими речовинами. Урок 31. 7 клас
Взаємодія кисню зі складними та простими речовинами. Урок 31. 7 клас 20231116_tipy_himicheskih_reaktsiy
20231116_tipy_himicheskih_reaktsiy Свойства воды
Свойства воды Дослідження оптичних властивостей нематичних рідких кристалів допованих Оксидом церію IV (СеО2)
Дослідження оптичних властивостей нематичних рідких кристалів допованих Оксидом церію IV (СеО2) Полибутадиен
Полибутадиен Периодический закон и периодическая система Д.И. Менделеева
Периодический закон и периодическая система Д.И. Менделеева Йони. Йонний зв’язок, його утворення
Йони. Йонний зв’язок, його утворення Химия - Кормилица. 10 класс
Химия - Кормилица. 10 класс Корунд. Разновидности корунда
Корунд. Разновидности корунда Стратегия органического синтеза
Стратегия органического синтеза Хімічні формули речовин. Урок №14
Хімічні формули речовин. Урок №14 Изомерия. (11 класс)
Изомерия. (11 класс) Химический состав клетки. Неорганические вещества клетки
Химический состав клетки. Неорганические вещества клетки Охрана труда в кабинете (лаборатории) химии образовательного учреждения
Охрана труда в кабинете (лаборатории) химии образовательного учреждения Основы электрохимии. Электрохимические процессы
Основы электрохимии. Электрохимические процессы Важнейшие классы бинарных соединений
Важнейшие классы бинарных соединений