Содержание
- 2. Атоми хімічних елементів сполучаються між собою, утворюючи всю різноманітність речовин, або хімічних сполук. Усі речовини вважаються
- 3. Речовини поділяють на прості й складні.
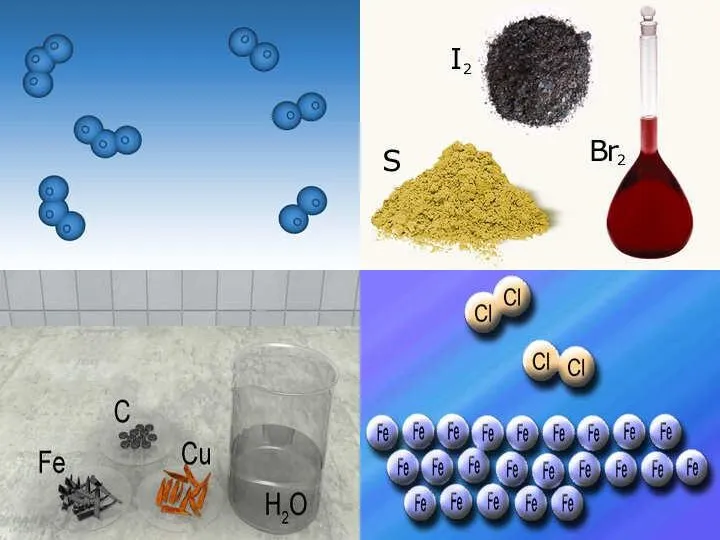
- 5. Хімічна сполука, утворена атомами одного хімічного елемента, називається простою речовиною. азот N2, натрій Na, залізо Fе,
- 7. Маленька цифра, що стоїть справа внизу від символу відповідного елемента, показує, скільки атомів входить до складу
- 8. Для простих речовин атомної будови число атомів у формулі не зазначається. Хімічна формула таких речовин за
- 10. Усі метали мають немолекулярну будову, тому виявляють багато спільних властивостей. Метали добре проводять електричний струм і
- 11. Властивості неметалів Неметали можуть мати як молекулярну, так і немолекулярну структури. Вони погано проводять теплоту й
- 12. Назви простих речовин і відповідних хімічних елементів здебільшого збігаються. Наприклад, проста речовина, утворена хімічним елементом Хлором,
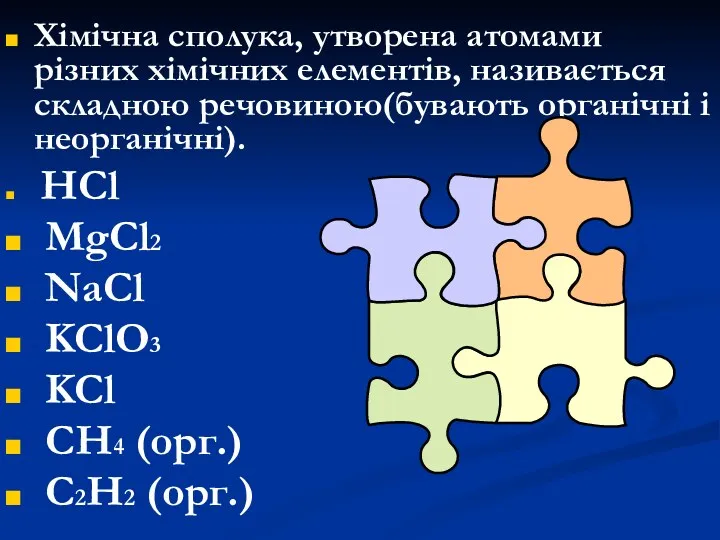
- 13. Хімічна сполука, утворена атомами різних хімічних елементів, називається складною речовиною(бувають органічні і неорганічні). HCl MgCl2 NaCl
- 14. Прикладами складних речовин можуть бути вода Н2О річковий пісок SiO2 цинк оксид ZnO вуглекислий газ СО2
- 15. Складні речовини, так само як і прості, бувають молекулярної і немолекулярної будови До речовин молекулярної будови
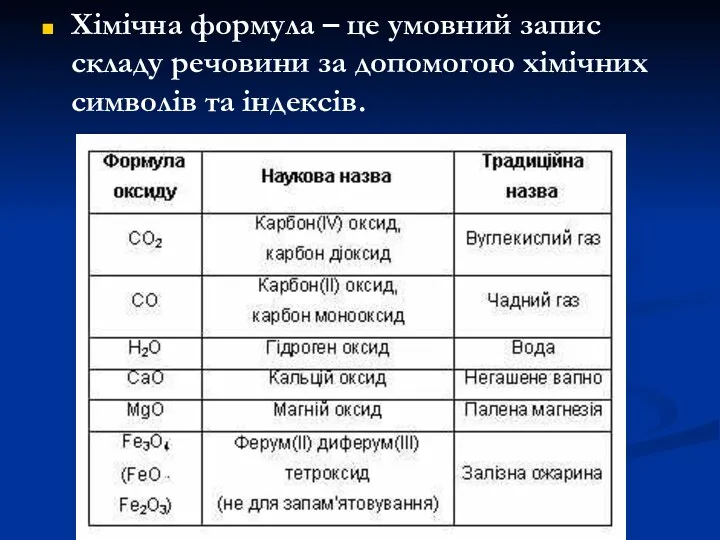
- 16. Хімічна формула – це умовний запис складу речовини за допомогою хімічних символів та індексів.
- 17. Щоб написати формулу, треба вказати знак відповідного хімічного елемента і праворуч від нього (трохи нижче) зазначити
- 18. Коефіцієнт — це число, яке записується перед хімічною формулою і позначає кількість молекул або окремих атомів
- 20. Скачать презентацию












 Железо. Fe (лат. Феррум)
Железо. Fe (лат. Феррум) Узагальнення й систематизація знань з теми Початкові хімічні поняття
Узагальнення й систематизація знань з теми Початкові хімічні поняття Аминокислоты. Пептиды. Хроматографические методы исследования
Аминокислоты. Пептиды. Хроматографические методы исследования Химическая связь
Химическая связь Розв'язування задач за рівнянням хімічних реакцій
Розв'язування задач за рівнянням хімічних реакцій NaHSO4. Гидросульфат натрия
NaHSO4. Гидросульфат натрия Молекулярно-массовые характеристики высокомолекулярных соединений
Молекулярно-массовые характеристики высокомолекулярных соединений Общие проблемы определения низких концентраций
Общие проблемы определения низких концентраций Ионные уравнения
Ионные уравнения Реакции ионного обмена
Реакции ионного обмена Установка производства олефинов для синтеза линейных алкилбензолов
Установка производства олефинов для синтеза линейных алкилбензолов Практикум по органической и биоорганической химии
Практикум по органической и биоорганической химии Строение вещества. Химические элементы
Строение вещества. Химические элементы Применение солей
Применение солей Обзор электродных процессов
Обзор электродных процессов Спроби класифікації хімічних елементів
Спроби класифікації хімічних елементів Металловедение. Классификация металлов
Металловедение. Классификация металлов Физико-химические методы в анализе ЛВ. Метод ионометрии в анализе ЛВ. Определение спирта в фармацевтических препаратах
Физико-химические методы в анализе ЛВ. Метод ионометрии в анализе ЛВ. Определение спирта в фармацевтических препаратах Окислительновосстановительное титрование
Окислительновосстановительное титрование Активационный анализ
Активационный анализ Твердотільний ямр
Твердотільний ямр Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение
Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение Наноматериалы. Свойства наноматериалов. Особенности свойств
Наноматериалы. Свойства наноматериалов. Особенности свойств Карбоновые кислоты
Карбоновые кислоты Значение периодического закона и периодической системы Д.И. Менделеева
Значение периодического закона и периодической системы Д.И. Менделеева Способы получения металлов
Способы получения металлов Химическая связь
Химическая связь Закон сохранения массы вещества. Химические уравнения
Закон сохранения массы вещества. Химические уравнения