Содержание
- 2. — наука, изучающая строение и свойства металлов и их сплавов, устанавливающая связь между их составом, строением
- 3. МЕТАЛЛОВЕДЕНИЕ — наука, которая, базируясь на основных положениях физики твердого тела, физической химии и электрохимии, исследует
- 4. (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ, обладающих характерными металлическими
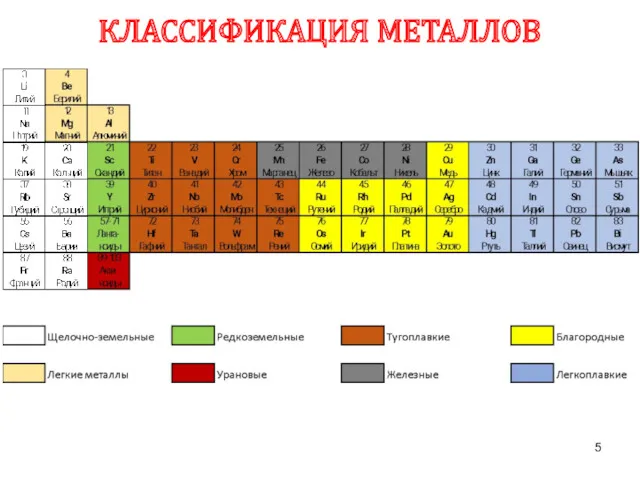
- 5. КЛАССИФИКАЦИЯ МЕТАЛЛОВ
- 6. Из 118 химических элементов, открытых на данный момент к металлам относят 94 элемента: Щелочные (6): Li,
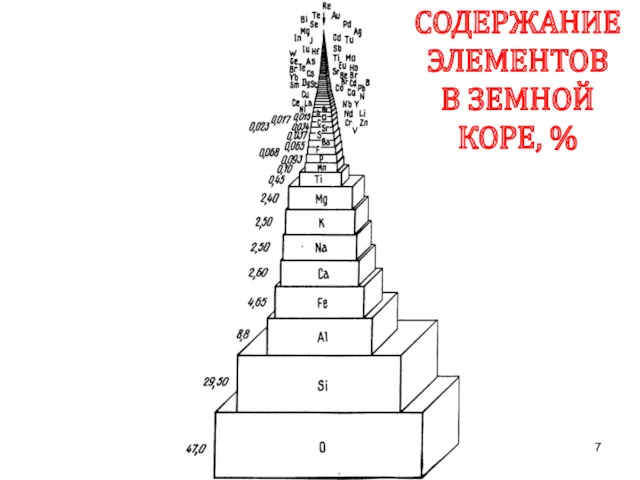
- 7. СОДЕРЖАНИЕ ЭЛЕМЕНТОВ В ЗЕМНОЙ КОРЕ, %
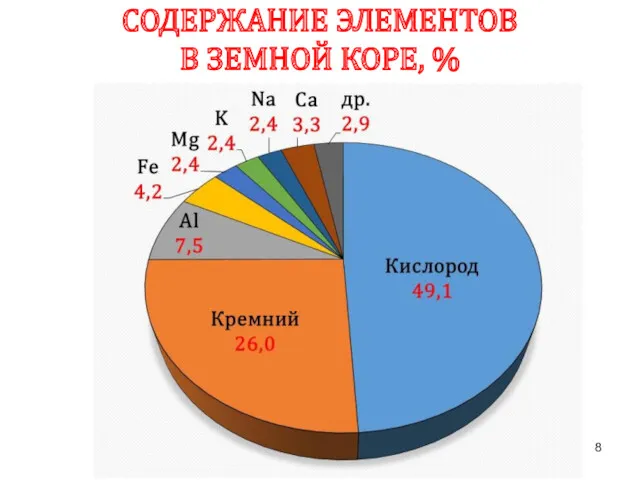
- 8. СОДЕРЖАНИЕ ЭЛЕМЕНТОВ В ЗЕМНОЙ КОРЕ, %
- 9. ЧЕРНЫЕ МЕТАЛЛЫ Характерные свойства: темно-серый цвет; большая плотность; высокая температура плавления; термоэлектронная эмиссия, (способность к испусканию
- 10. Характерные свойства: определенная окраска; высокая пластичность; малая твердость; относительно низкая температура плавления; отсутствие полиморфизма. Наиболее типичный
- 11. ЦВЕТНЫЕ МЕТАЛЛЫ. КЛАССИФИКАЦИЯ легкие металлы (Mg, Be, Al, Ti), обладающие малой плотностью; легкоплавкие металлы (Zn, Sn,
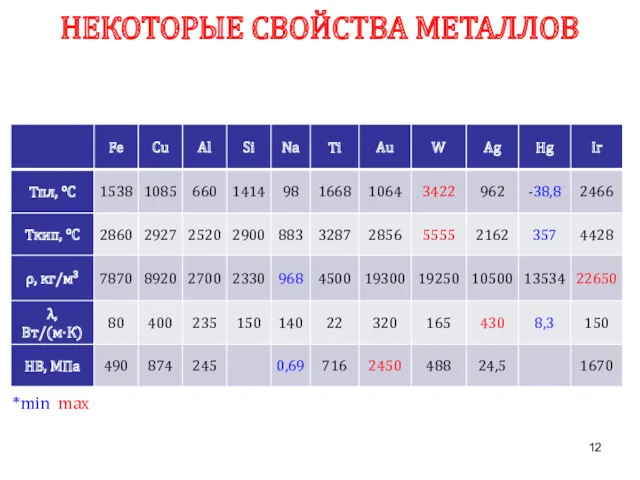
- 12. НЕКОТОРЫЕ СВОЙСТВА МЕТАЛЛОВ *min max
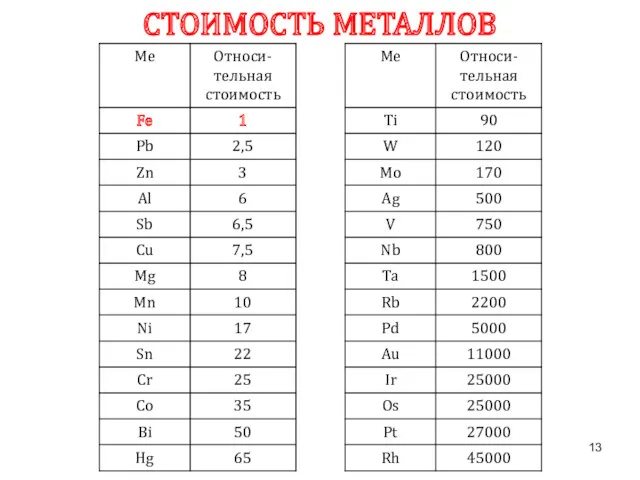
- 13. СТОИМОСТЬ МЕТАЛЛОВ
- 14. Характеризуется определенным закономерным расположением атомов в пространстве. Для описания атомно-кристаллической структуры используют понятие кристаллической решетки, являющейся
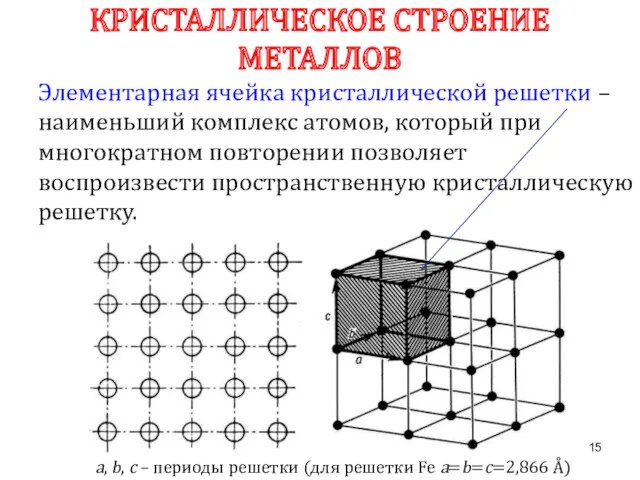
- 15. Элементарная ячейка кристаллической решетки – наименьший комплекс атомов, который при многократном повторении позволяет воспроизвести пространственную кристаллическую
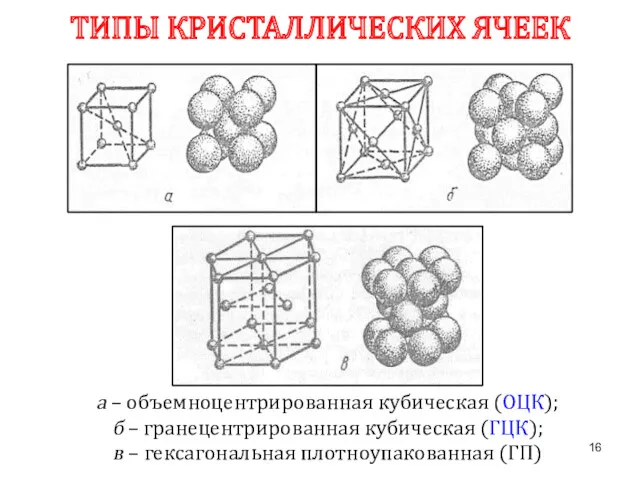
- 16. ТИПЫ КРИСТАЛЛИЧЕСКИХ ЯЧЕЕК
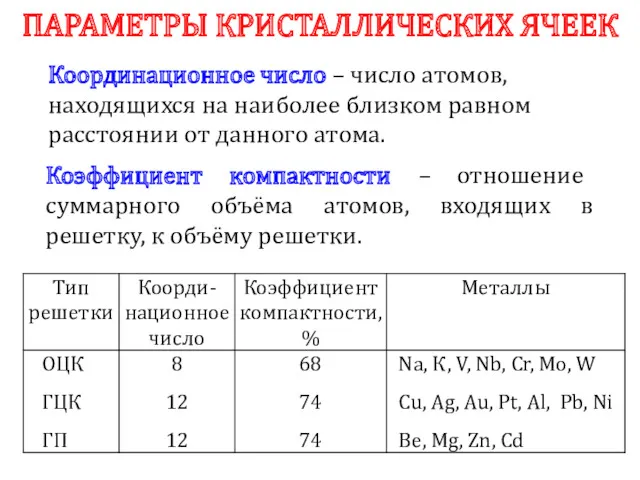
- 18. ПАРАМЕТРЫ КРИСТАЛЛИЧЕСКИХ ЯЧЕЕК Координационное число – число атомов, находящихся на наиболее близком равном расстоянии от данного
- 19. РЕАЛЬНОЕ СТРОЕНИЕ МЕТАЛЛИЧЕСКИХ КРИСТАЛЛОВ Строение металлов является поликристаллическим. Кристаллы неправильной формы в металле называют зёрнами. Ориентация
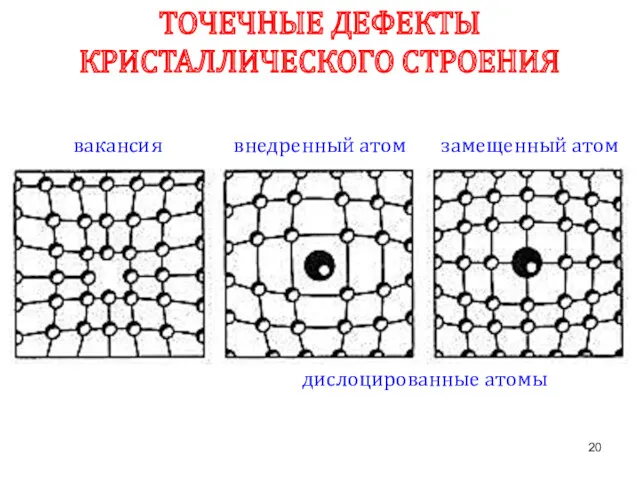
- 20. вакансия замещенный атом внедренный атом ТОЧЕЧНЫЕ ДЕФЕКТЫ КРИСТАЛЛИЧЕСКОГО СТРОЕНИЯ дислоцированные атомы
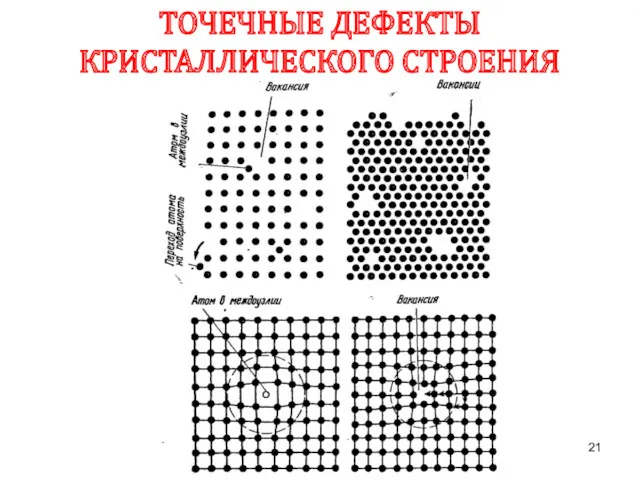
- 21. ТОЧЕЧНЫЕ ДЕФЕКТЫ КРИСТАЛЛИЧЕСКОГО СТРОЕНИЯ
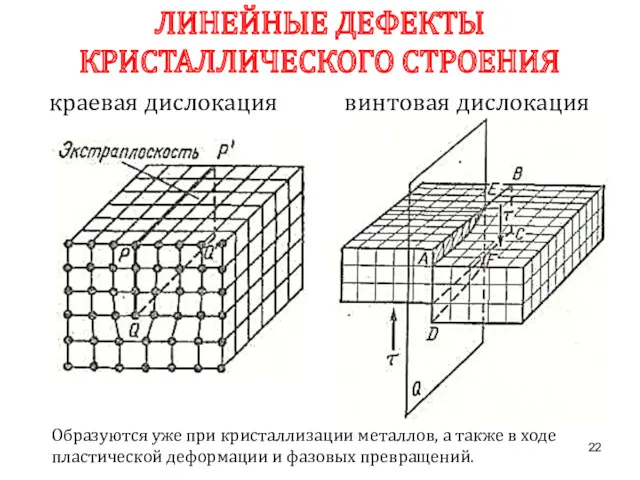
- 22. краевая дислокация винтовая дислокация ЛИНЕЙНЫЕ ДЕФЕКТЫ КРИСТАЛЛИЧЕСКОГО СТРОЕНИЯ Образуются уже при кристаллизации металлов, а также в
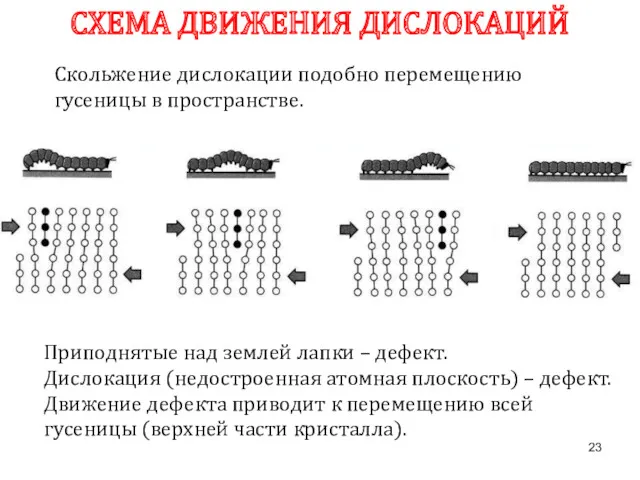
- 23. СХЕМА ДВИЖЕНИЯ ДИСЛОКАЦИЙ Скольжение дислокации подобно перемещению гусеницы в пространстве. Приподнятые над землей лапки – дефект.
- 24. ПОВЕРХНОСТНЫЕ ДЕФЕКТЫ КРИСТАЛЛИЧЕСКОГО СТРОЕНИЯ Граница зёрен Зерно 1 Зерно 2 Обычно это места стыка двух ориентированных
- 25. Под размером зерна принято понимать величину его среднего диаметра, выявляемого в поперечном сечении. Это определение условно,
- 26. Процесс пластического течения, а, следовательно, и предел текучести зависят от длины свободного пробега дислокаций до «непрозрачного»
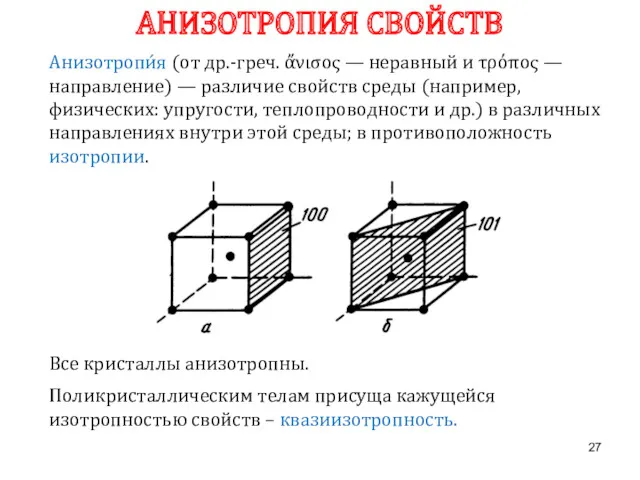
- 27. Анизотропи́я (от др.-греч. ἄνισος — неравный и τρόπος — направление) — различие свойств среды (например, физических:
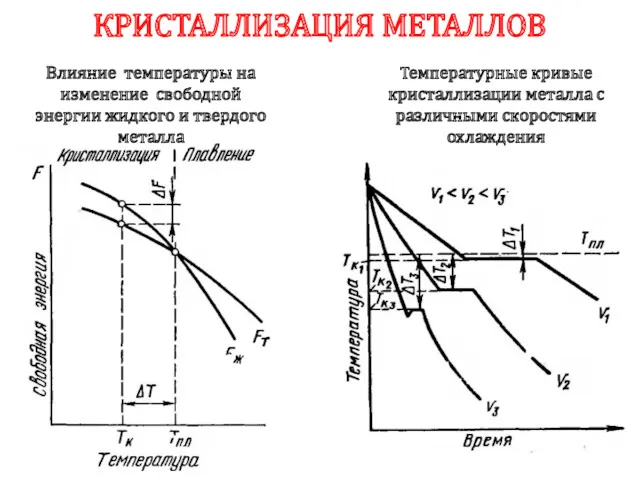
- 28. КРИСТАЛЛИЗАЦИЯ МЕТАЛЛОВ Влияние температуры на изменение свободной энергии жидкого и твердого металла Температурные кривые кристаллизации металла
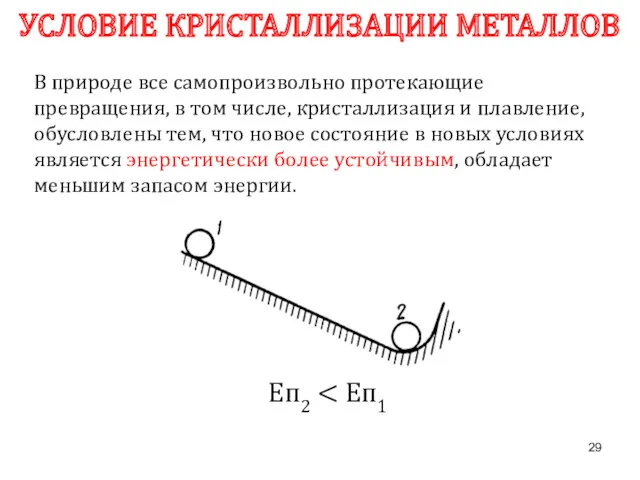
- 29. В природе все самопроизвольно протекающие превращения, в том числе, кристаллизация и плавление, обусловлены тем, что новое
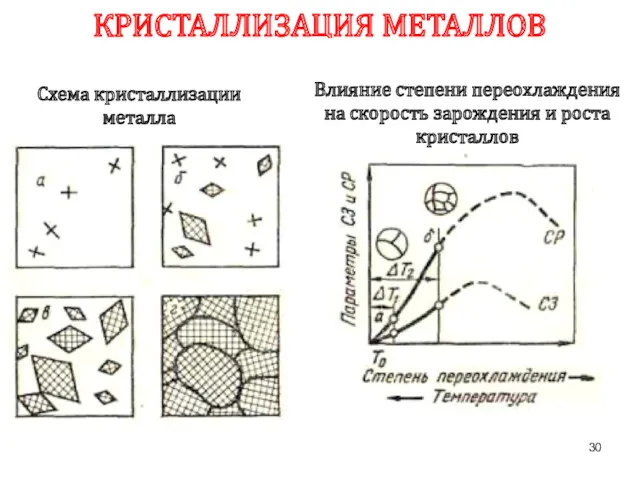
- 30. КРИСТАЛЛИЗАЦИЯ МЕТАЛЛОВ Влияние степени переохлаждения на скорость зарождения и роста кристаллов Схема кристаллизации металла
- 31. КРИСТАЛЛИЗАЦИЯ МЕТАЛЛОВ Изменение свободной энергии ΔF металла при образовании зародышей кристаллов в зависимости от их размера
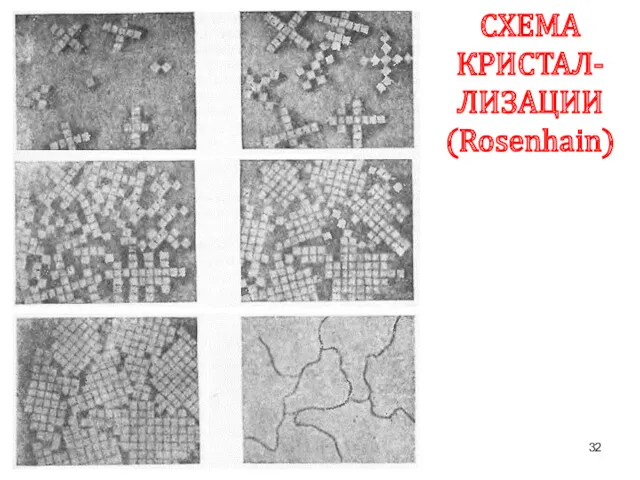
- 32. СХЕМА КРИСТАЛ- ЛИЗАЦИИ (Rosenhain)
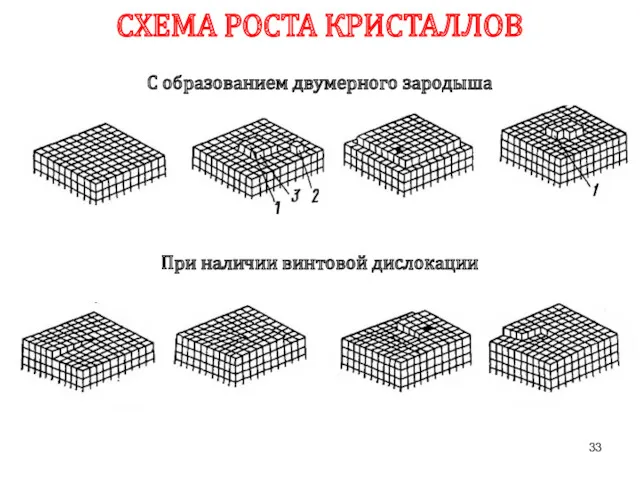
- 33. СХЕМА РОСТА КРИСТАЛЛОВ С образованием двумерного зародыша При наличии винтовой дислокации 1
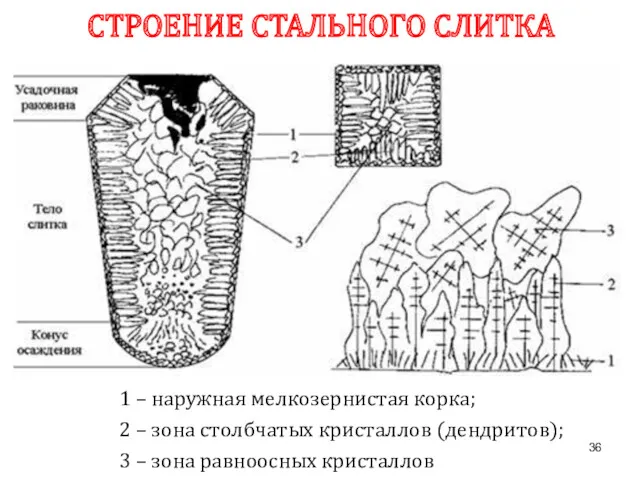
- 36. СТРОЕНИЕ СТАЛЬНОГО СЛИТКА 1 – наружная мелкозернистая корка; 2 – зона столбчатых кристаллов (дендритов); 3 –
- 37. КРИСТАЛЛ Д.К. ЧЕРНОВА (ДЕНДРИТ)
- 38. ДЕНДРИТНЫЕ КРИСТАЛЛЫ МЕДИ
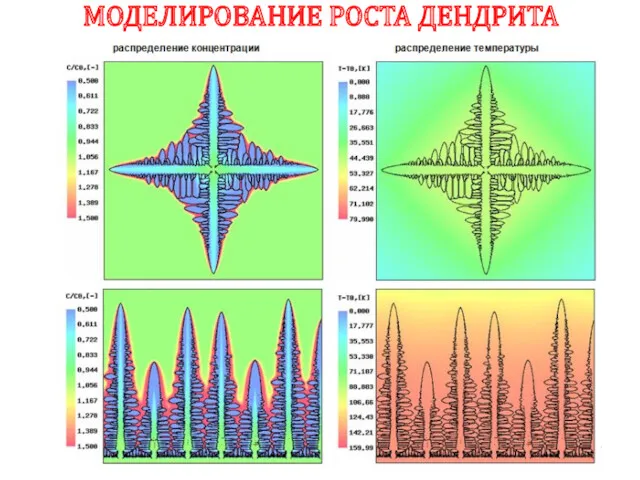
- 39. МОДЕЛИРОВАНИЕ РОСТА ДЕНДРИТА Время
- 40. МОДЕЛИРОВАНИЕ РОСТА ДЕНДРИТА
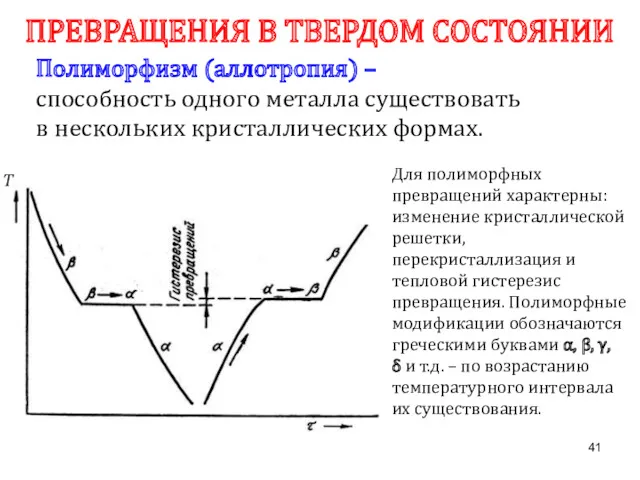
- 41. ПРЕВРАЩЕНИЯ В ТВЕРДОМ СОСТОЯНИИ Полиморфизм (аллотропия) – способность одного металла существовать в нескольких кристаллических формах. Для
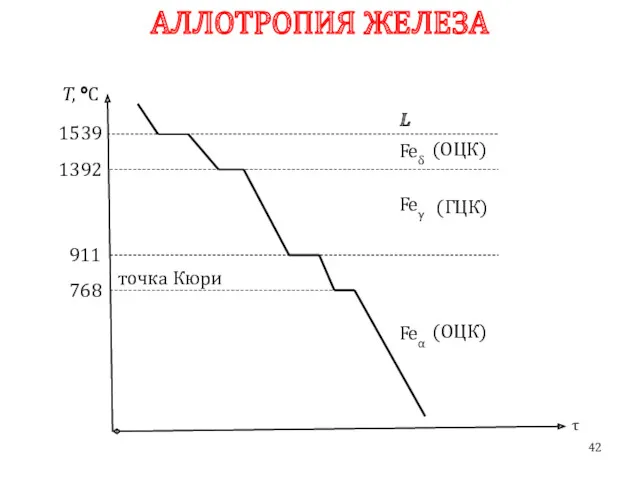
- 42. АЛЛОТРОПИЯ ЖЕЛЕЗА τ
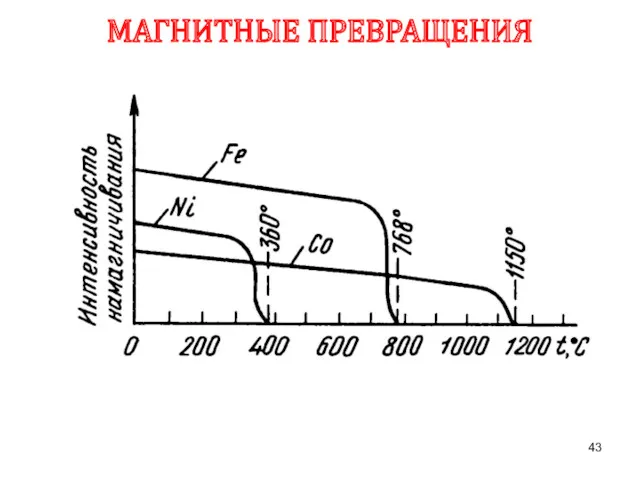
- 43. МАГНИТНЫЕ ПРЕВРАЩЕНИЯ
- 44. СПЛАВЫ Сплав – вещество, получаемое сплавлением двух или более компонентов. Система – группа тел выделяемых для
- 45. Компоненты, образующие сплав, не способны к взаимному растворению и не образуют химического соединения. Кристаллы А и
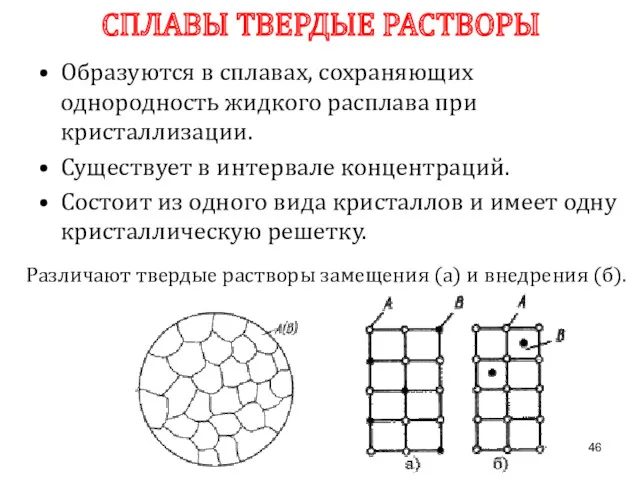
- 46. Образуются в сплавах, сохраняющих однородность жидкого расплава при кристаллизации. Существует в интервале концентраций. Состоит из одного
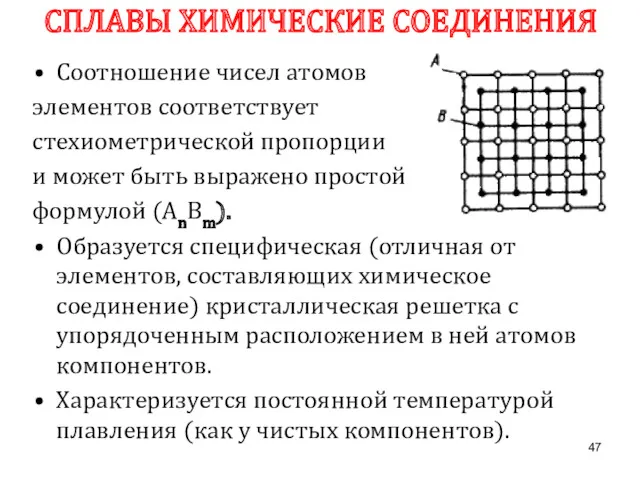
- 47. Соотношение чисел атомов элементов соответствует стехиометрической пропорции и может быть выражено простой формулой (АnВm). Образуется специфическая
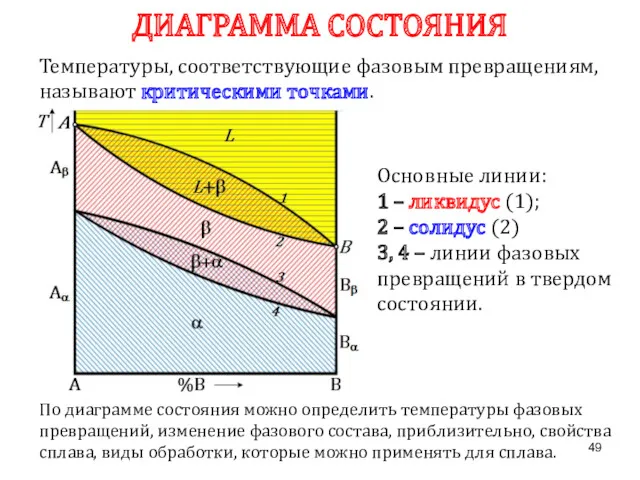
- 48. ДИАГРАММА СОСТОЯНИЯ Диаграмма состояния показывает изменение состояния в зависимости от температуры и концентрации (давление постоянно для
- 49. По диаграмме состояния можно определить температуры фазовых превращений, изменение фазового состава, приблизительно, свойства сплава, виды обработки,
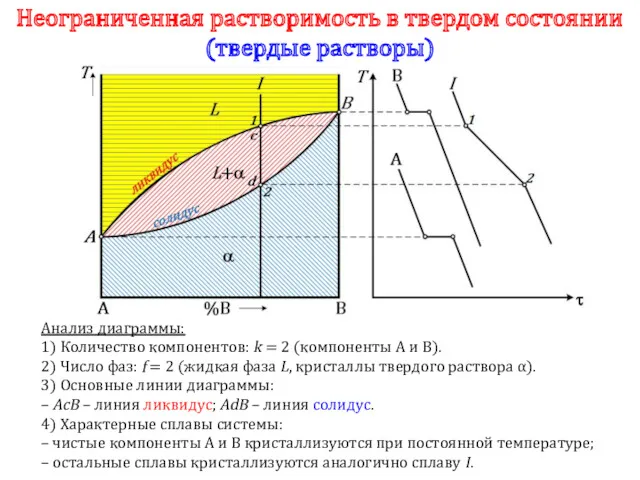
- 50. Неограниченная растворимость в твердом состоянии (твердые растворы) Анализ диаграммы: 1) Количество компонентов: k = 2 (компоненты
- 51. До точки 1 охлаждается сплав в жидком состоянии. При температуре, соответствующей точке 1, начинают образовываться центры
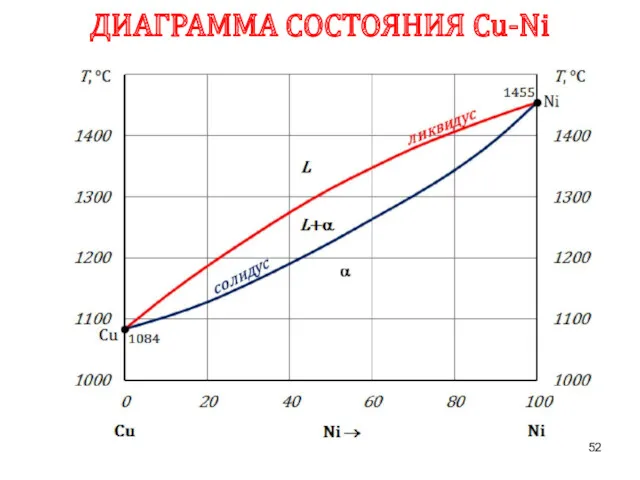
- 52. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
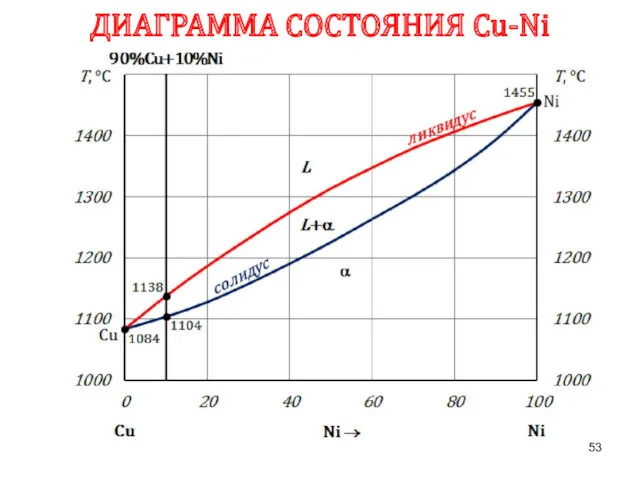
- 53. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
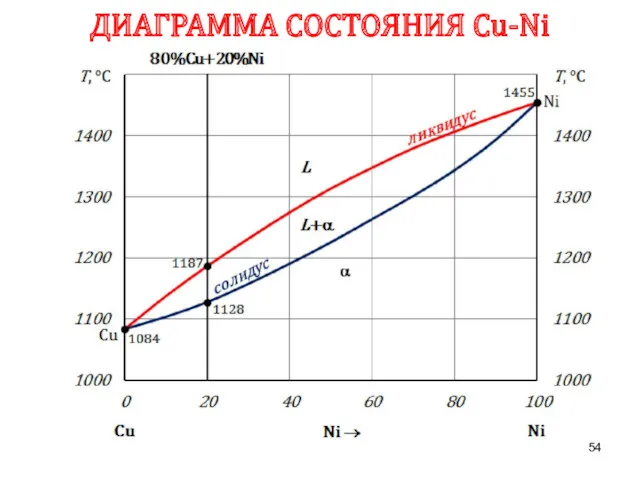
- 54. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
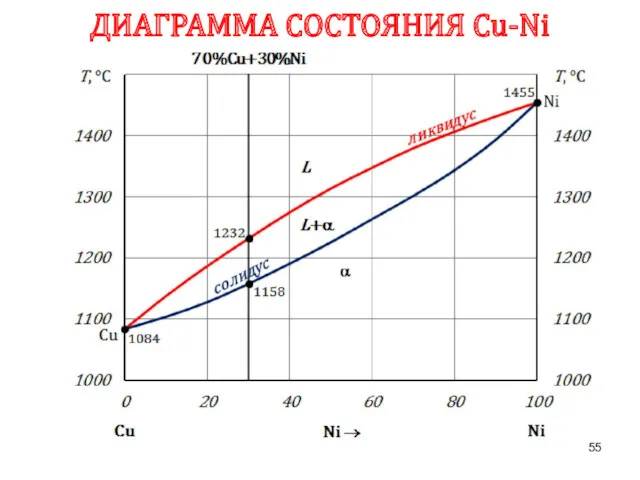
- 55. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
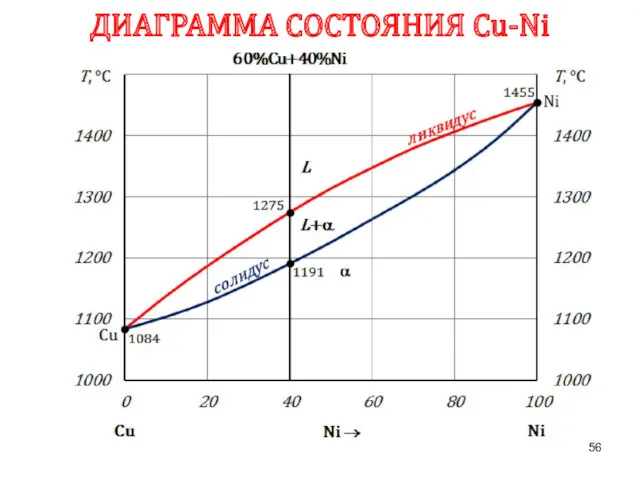
- 56. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
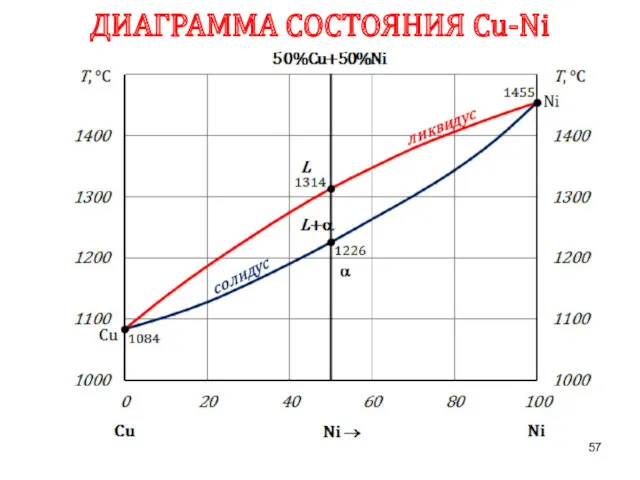
- 57. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
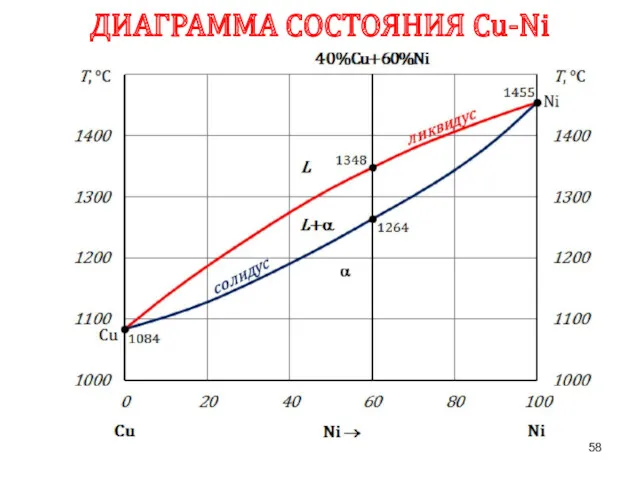
- 58. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
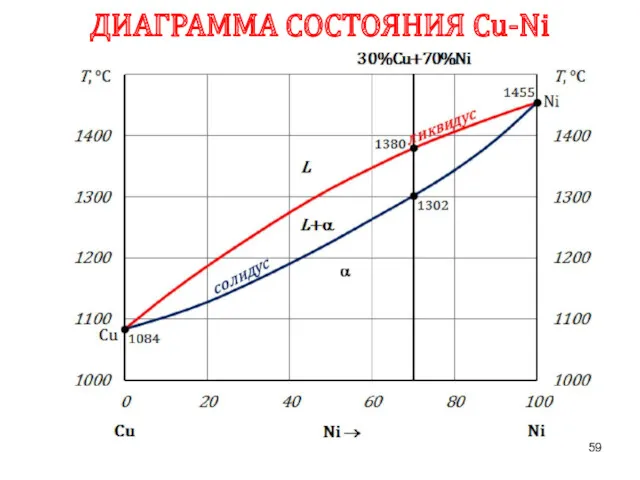
- 59. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
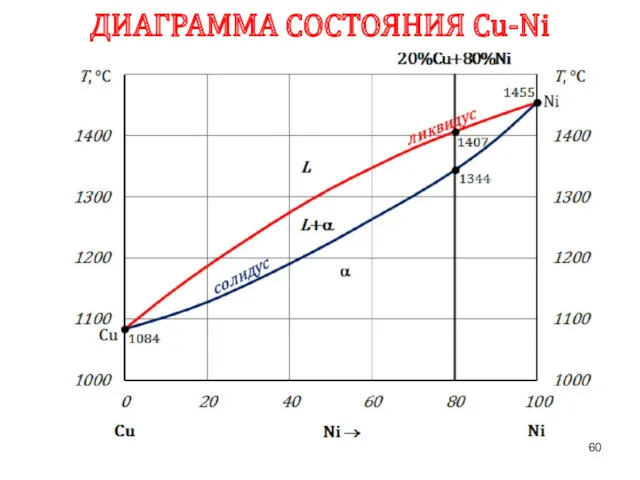
- 60. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
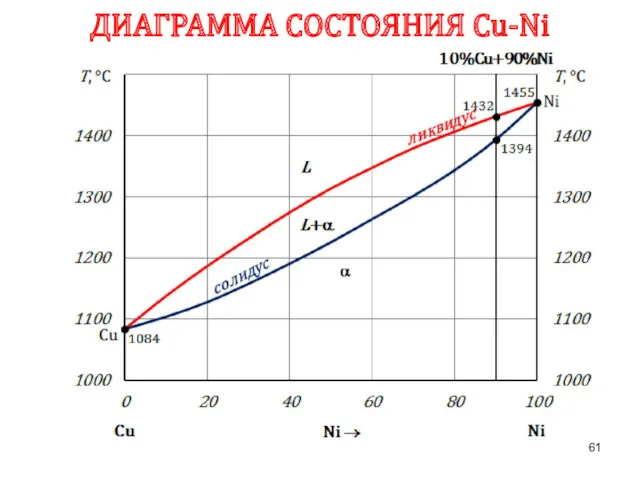
- 61. ДИАГРАММА СОСТОЯНИЯ Сu-Ni
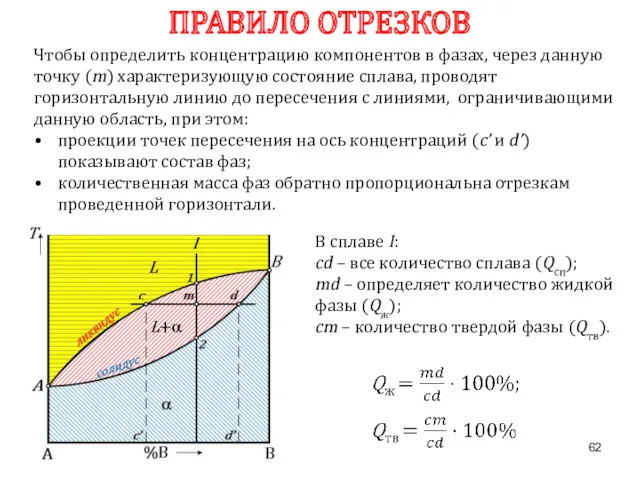
- 62. ПРАВИЛО ОТРЕЗКОВ Чтобы определить концентрацию компонентов в фазах, через данную точку (m) характеризующую состояние сплава, проводят
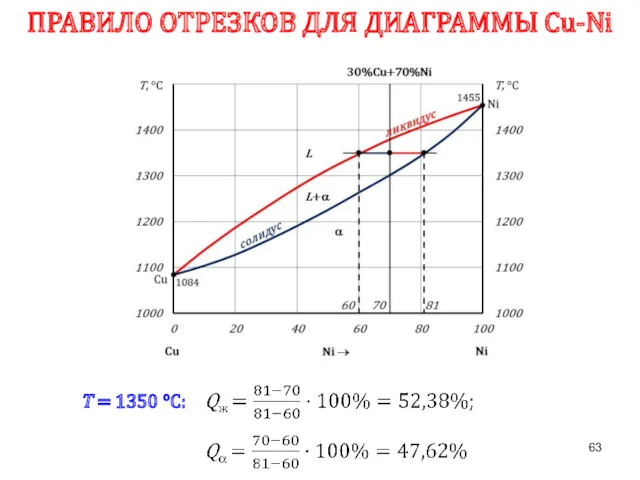
- 63. ПРАВИЛО ОТРЕЗКОВ ДЛЯ ДИАГРАММЫ Сu-Ni Т = 1350 °С:
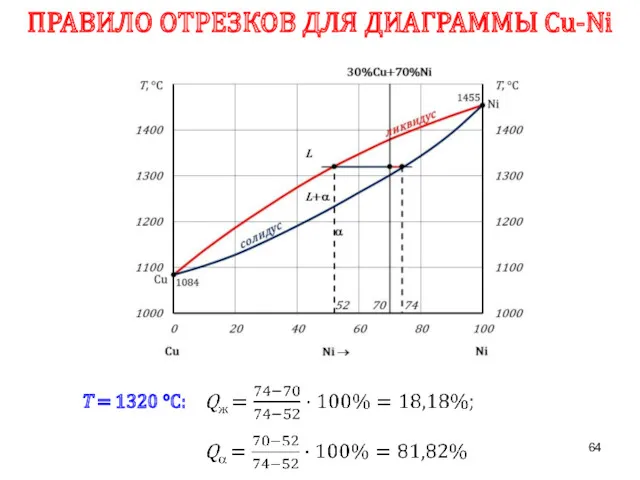
- 64. ПРАВИЛО ОТРЕЗКОВ ДЛЯ ДИАГРАММЫ Сu-Ni Т = 1320 °С:
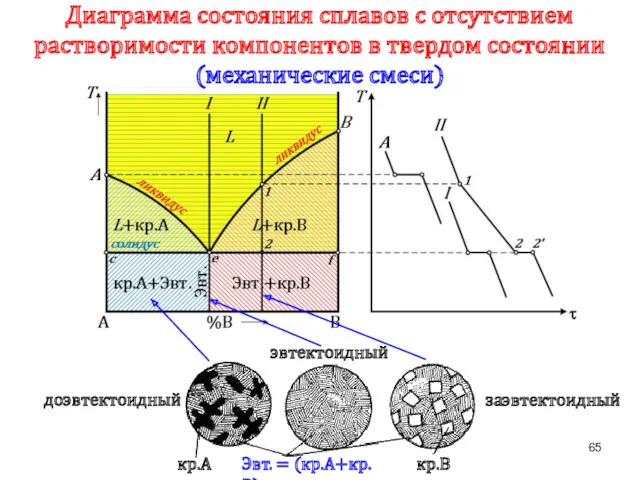
- 65. Диаграмма состояния сплавов с отсутствием растворимости компонентов в твердом состоянии (механические смеси) доэвтектоидный эвтектоидный заэвтектоидный Эвт.
- 66. Анализ диаграммы состояния сплавов с отсутствием растворимости компонентов в твердом состоянии (механические смеси) 1) Количество компонентов:
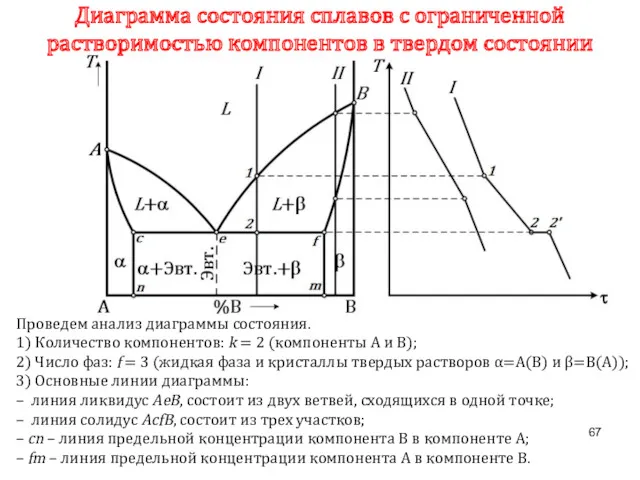
- 67. Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии Проведем анализ диаграммы состояния. 1) Количество
- 68. Типовые сплавы системы с ограниченной растворимостью компонентов в твердом состоянии При концентрации компонентов, не превышающей предельных
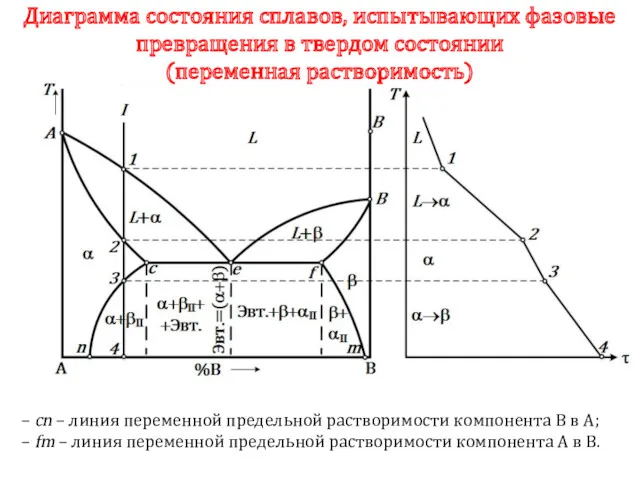
- 69. Диаграмма состояния сплавов, испытывающих фазовые превращения в твердом состоянии (переменная растворимость) – cn – линия переменной
- 70. До точки 1 охлаждается сплав в жидком состоянии. При температуре, соответствующей точке 1, начинают образовываться центры
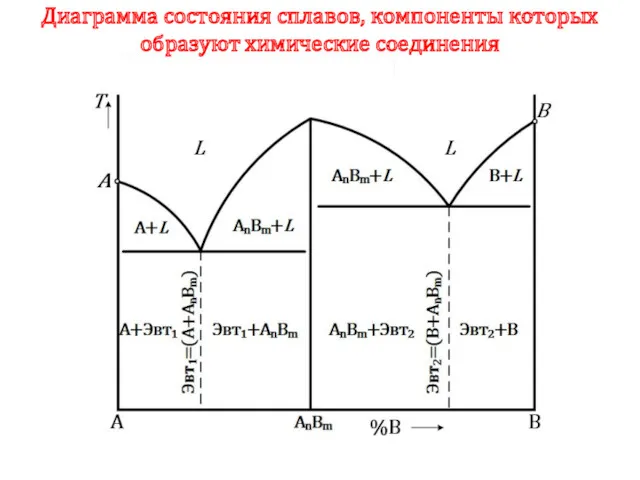
- 71. Диаграмма состояния сплавов, компоненты которых образуют химические соединения
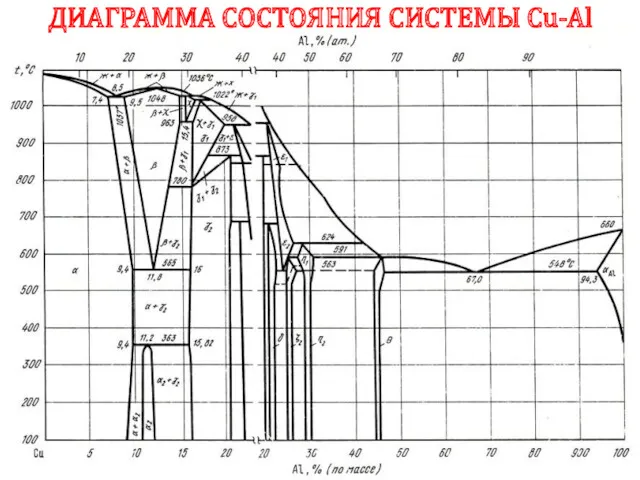
- 72. ДИАГРАММА СОСТОЯНИЯ СИСТЕМЫ Cu-Al
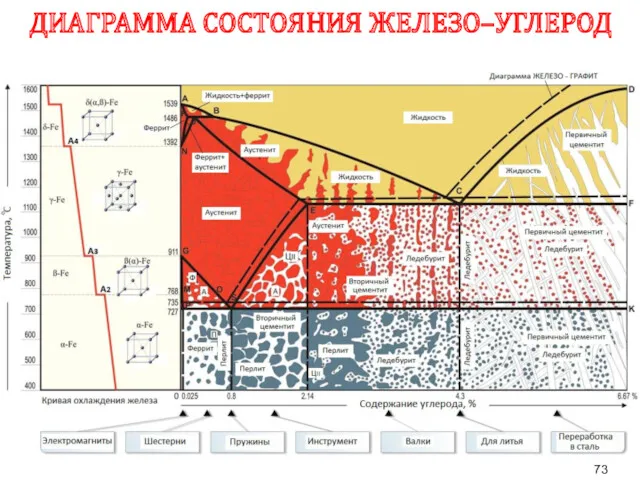
- 73. ДИАГРАММА СОСТОЯНИЯ ЖЕЛЕЗО–УГЛЕРОД
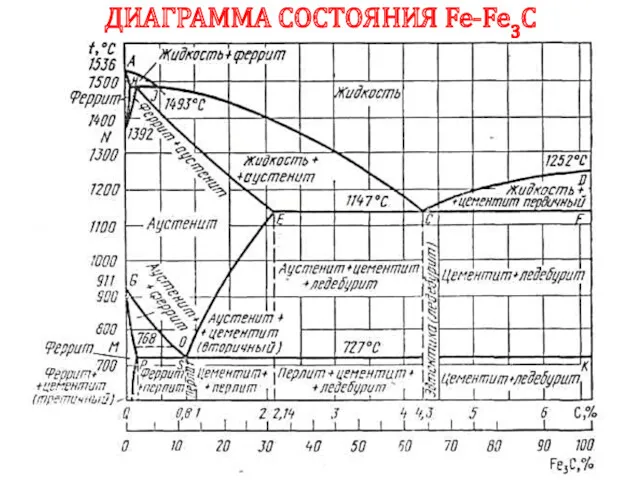
- 74. ДИАГРАММА СОСТОЯНИЯ Fe-Fe3C
- 75. ЛИНИИ ДИАГРАММЫ СОСТОЯНИЯ Fe-Fe3C ABCD – линия начала кристаллизации сплава (ликвидус) AHNJECF – линия конца кристаллизации
- 76. СВОЙСТВА И СТРОЕНИЕ КОМПОНЕНТОВ ДИАГРАММЫ ЖЕЛЕЗО-УГЛЕРОД Железо (Fe): Тпл = 1539° С; в твердом состоянии может
- 77. Феррит (обозначают Ф или α) — твердый раствор внедрения углерода в Feα. Различают низкотемпературный и высокотемпературный
- 78. СВОЙСТВА И СТРОЕНИЕ КОМПОНЕНТОВ ДИАГРАММЫ ЖЕЛЕЗО-УГЛЕРОД Перлит (П) – механическая смесь, состоящая из мелких зерен или
- 79. Нонвариантные реакции на диаграмме Т=1499°С (линия HJB): L(B)+Ф(H)→A(J) - перетектическая реакция, наблюдается только у сплавов с
- 80. Вторичная кристаллизация весьма малоуглеродистых сплавов Сплав типа I (С Сплав типа II (0,01
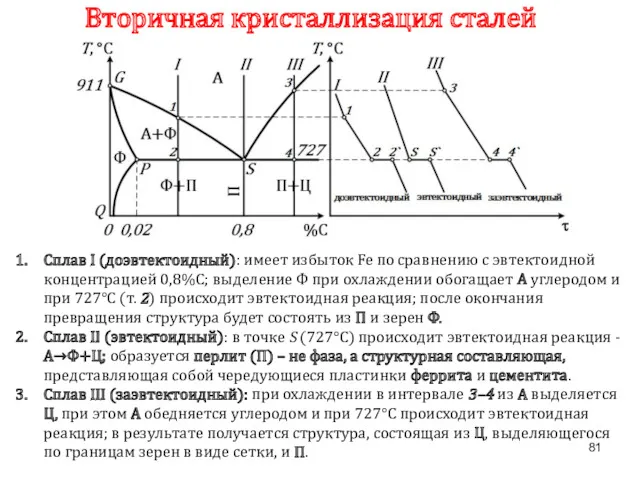
- 81. Вторичная кристаллизация сталей Сплав I (доэвтектоидный): имеет избыток Fe по сравнению с эвтектоидной концентрацией 0,8%С; выделение
- 82. Превращения при вторичной кристаллизации в высокоуглеродистых сплавах (чугунах) Сплав I (доэвтектический): первичные кристаллы А изменяют свою
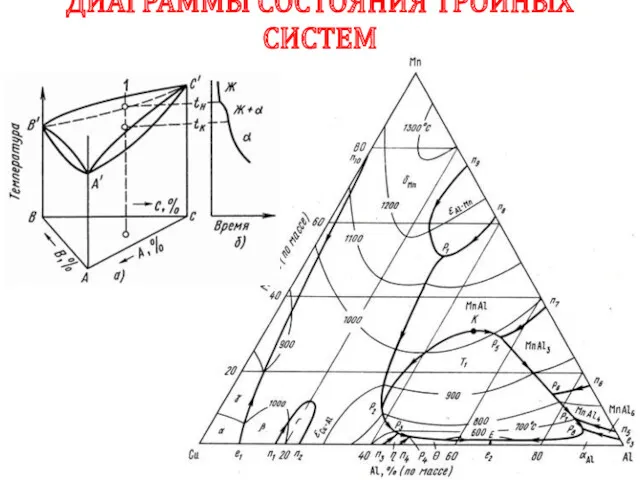
- 83. ДИАГРАММЫ СОСТОЯНИЯ ТРОЙНЫХ СИСТЕМ
- 84. КЛАССИФИКАЦИЯ СТАЛЕЙ По химсоставу: углеродистые и легированные (никелевые, хромистые, хромоникелевые и т.д.). По равновесной структуре: доэвтектоидные,
- 85. Классификация сталей по химическому составу Углеродистые стали: малоуглеродистые – среднеуглеродистые – 0,3...0,7% С; высокоуглеродистые – >
- 86. УГЛЕРОДИСТЫЕ СТАЛИ Основной металлический материал промышленности – углеродистая сталь. Технологические примеси: марганец, кремний. Постоянные примеси: сера,
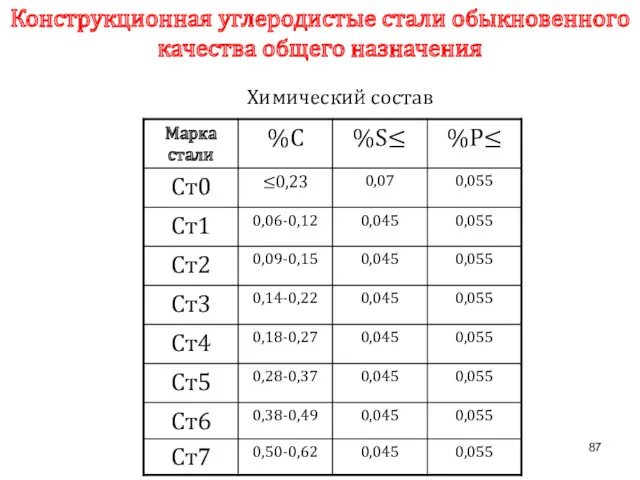
- 87. Конструкционная углеродистые стали обыкновенного качества общего назначения Химический состав
- 88. Маркировка различных групп углеродистых сталей обыкновенного качества Группа А – с гарантируемыми механическими свойствами (сталь не
- 89. Маркировка углеродистых сталей обычного качества разных способов раскисления В зависимости от способа раскисления (с целью удаления
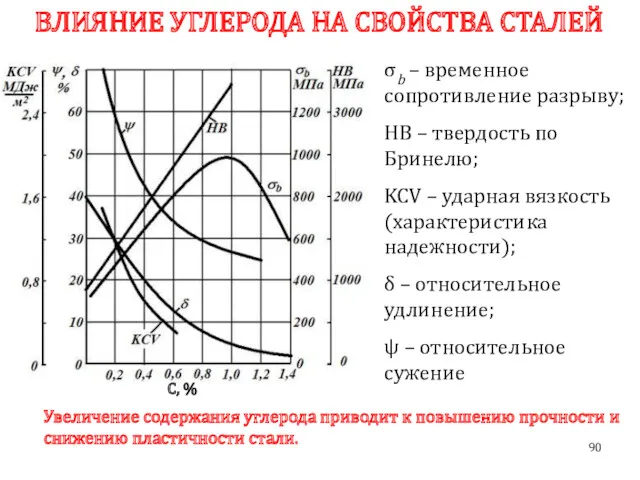
- 90. ВЛИЯНИЕ УГЛЕРОДА НА СВОЙСТВА СТАЛЕЙ Увеличение содержания углерода приводит к повышению прочности и снижению пластичности стали.
- 91. ВЛИЯНИЕ ПОСТОЯННЫХ ПРИМЕСЕЙ НА СВОЙСТВА СТАЛИ Марганец – вводится в любую сталь для раскисления, поэтому его
- 92. Применение конструкционных углеродистых сталей обыкновенного качества
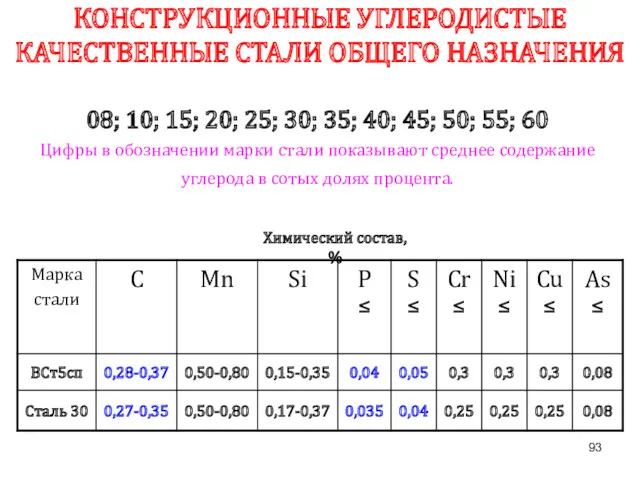
- 93. КОНСТРУКЦИОННЫЕ УГЛЕРОДИСТЫЕ КАЧЕСТВЕННЫЕ СТАЛИ ОБЩЕГО НАЗНАЧЕНИЯ 08; 10; 15; 20; 25; 30; 35; 40; 45; 50;
- 94. Применение конструкционных углеродистых качественных сталей общего назначения
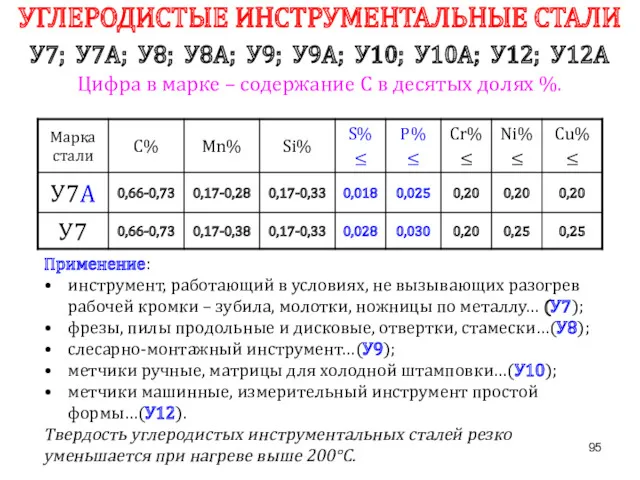
- 95. УГЛЕРОДИСТЫЕ ИНСТРУМЕНТАЛЬНЫЕ СТАЛИ У7; У7А; У8; У8А; У9; У9А; У10; У10А; У12; У12А Цифра в марке
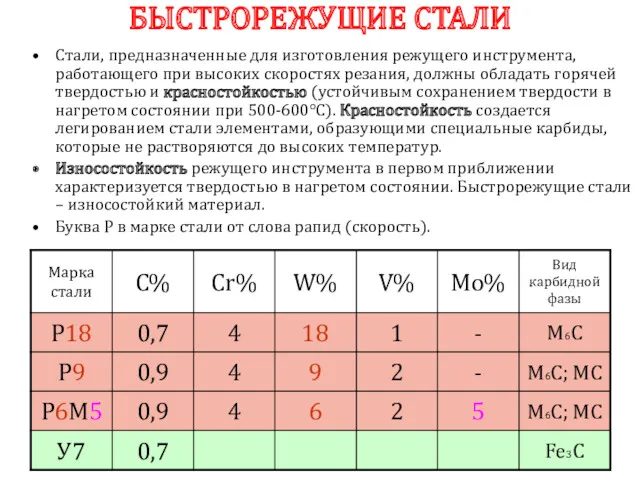
- 96. БЫСТРОРЕЖУЩИЕ СТАЛИ Стали, предназначенные для изготовления режущего инструмента, работающего при высоких скоростях резания, должны обладать горячей
- 97. КОНСТРУКЦИОННЫЕ ЛЕГИРОВАННЫЕ СТАЛИ. СИСТЕМА МАРКИРОВКИ ПО ГОСТУ Обозначения состоят из цифр и букв, указывающих на примерный
- 98. Примеры применения конструкционных легированных сталей
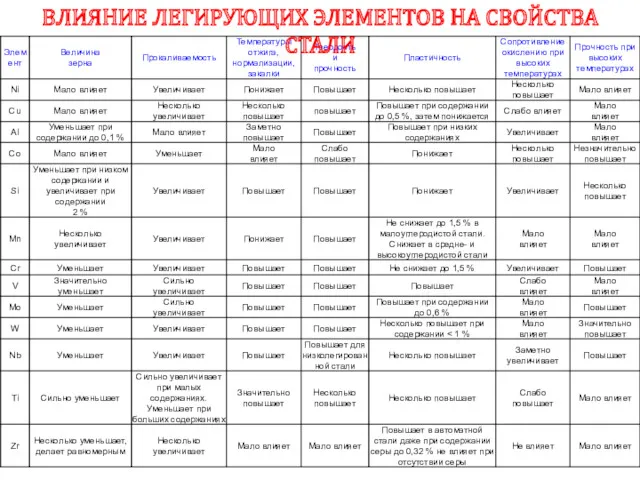
- 99. ВЛИЯНИЕ ЛЕГИРУЮЩИХ ЭЛЕМЕНТОВ НА СВОЙСТВА СТАЛИ
- 100. ЧУГУНЫ Белый чугун – название получил по матово-белому цвету излома; структура в не нагретом состоянии: Ц
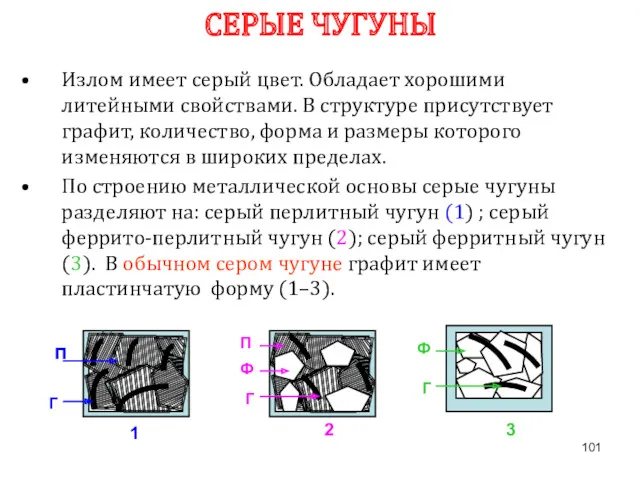
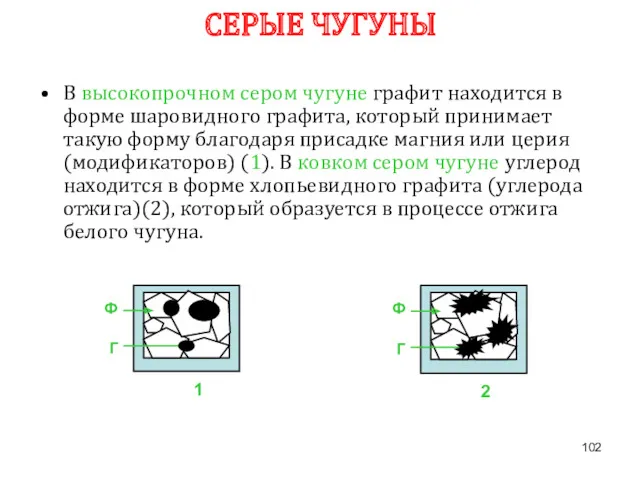
- 101. СЕРЫЕ ЧУГУНЫ Излом имеет серый цвет. Обладает хорошими литейными свойствами. В структуре присутствует графит, количество, форма
- 102. В высокопрочном сером чугуне графит находится в форме шаровидного графита, который принимает такую форму благодаря присадке
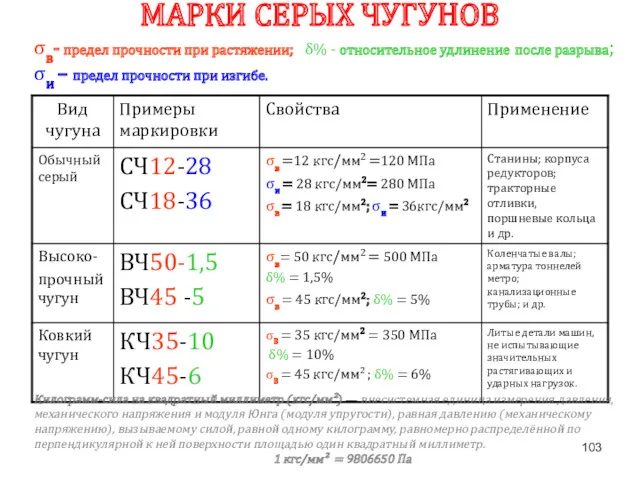
- 103. МАРКИ СЕРЫХ ЧУГУНОВ σв- предел прочности при растяжении; δ% - относительное удлинение после разрыва; σи –
- 104. СПЛАВЫ МЕДИ. ЛАТУНИ Латуни – сплавы меди с цинком – при содержании цинка до 45%. Свойства
- 105. Оловянистые бронзы – сплавы меди с оловом. Свойства оловянистых бронз: Бронзы, содержащие более 5% – 6%
- 106. Сплавы меди с алюминием, кремнием, бериллием и др. элементами также называют бронзами: алюминиевыми, кремнистыми, бериллиевыми и
- 107. МЕХАНИЧЕСКИЕ СВОЙСТВА МЕТАЛЛИЧЕСКИХ МАТЕРИАЛОВ Аспекты выбора материалов для изготовления деталей машин и механизмов: 1. Механические (конструкционные)
- 108. МЕХАНИЧЕСКИЕ СВОЙСТВА МЕТАЛЛИЧЕСКИХ МАТЕРИАЛОВ И МЕТОДЫ ИХ ОПРЕДЕЛЕНИЯ Способность материала в конструкции сопротивляться внешним воздействиям, (т.е.
- 109. Твердость характеризуется способностью металла противостоять проникновению в него другого, более твердого тела. Пределом прочности при растяжении
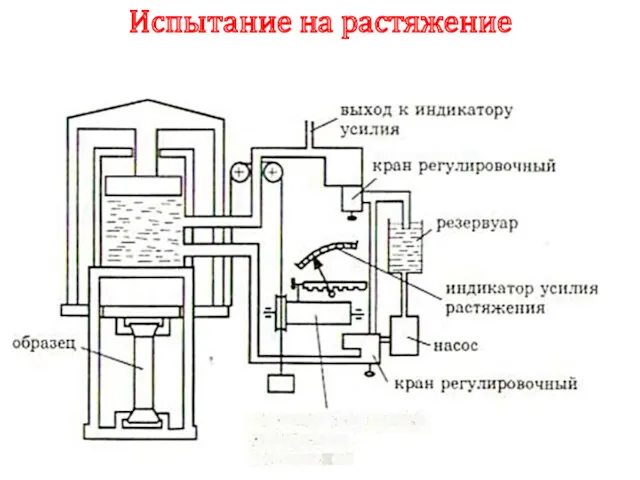
- 110. Испытание на растяжение
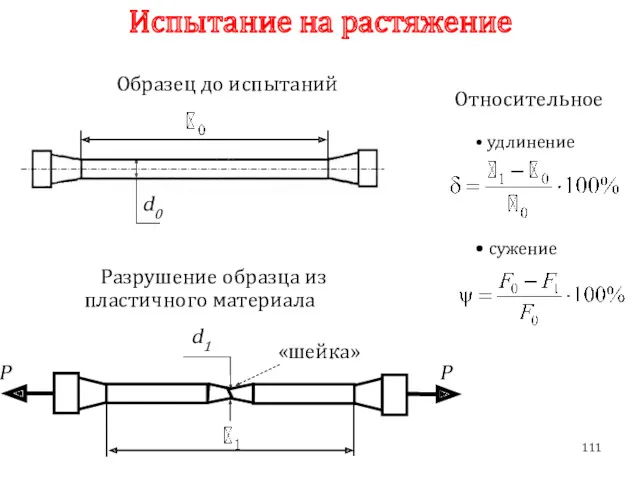
- 111. Испытание на растяжение Разрушение образца из пластичного материала Образец до испытаний Относительное удлинение сужение
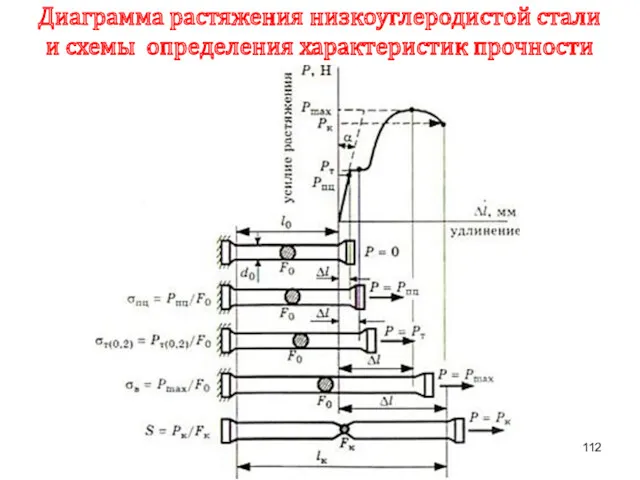
- 112. Диаграмма растяжения низкоуглеродистой стали и схемы определения характеристик прочности
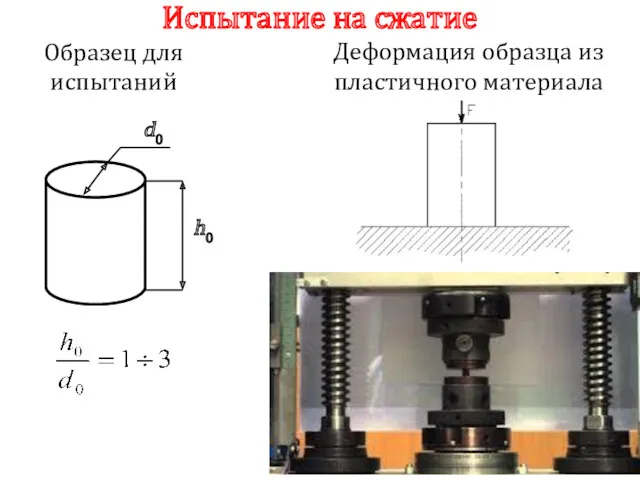
- 113. Испытание на сжатие d0 h0 Образец для испытаний Деформация образца из пластичного материала
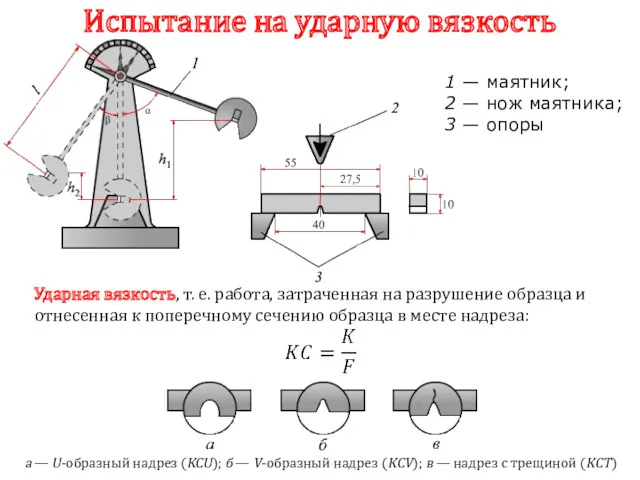
- 114. 1 — маятник; 2 — нож маятника; 3 — опоры Испытание на ударную вязкость Ударная вязкость,
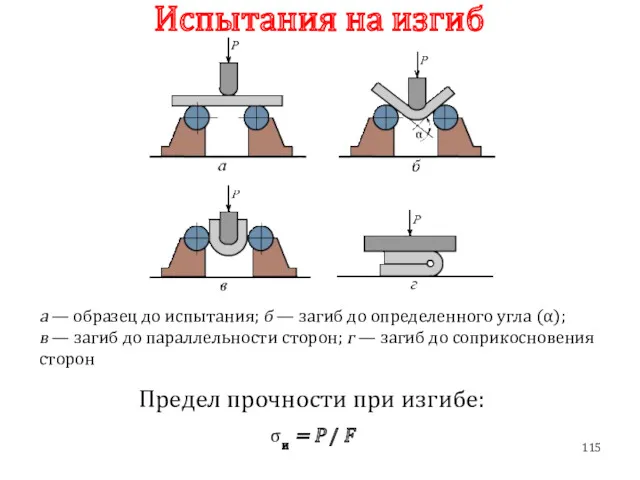
- 115. Испытания на изгиб Предел прочности при изгибе: σи = P / F а — образец до
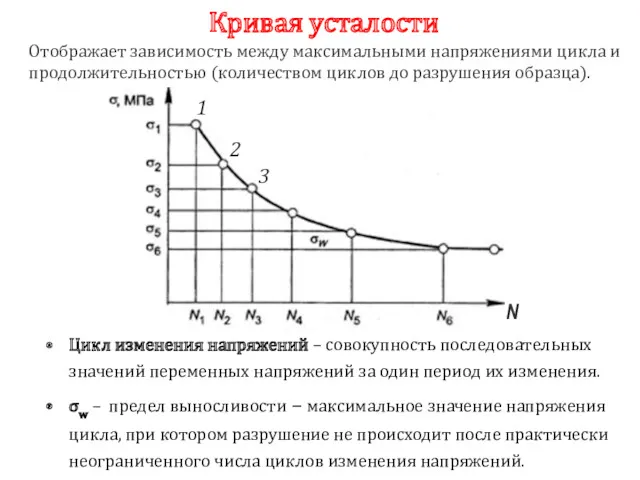
- 116. Кривая усталости Цикл изменения напряжений – совокупность последовательных значений переменных напряжений за один период их изменения.
- 117. МЕТОДЫ ОПРЕДЕЛЕНИЯ ТВЕРДОСТИ МАТЕРИАЛОВ Измерение твердости – упрощенный метод определения прочности. Твердость – одна из характеристик
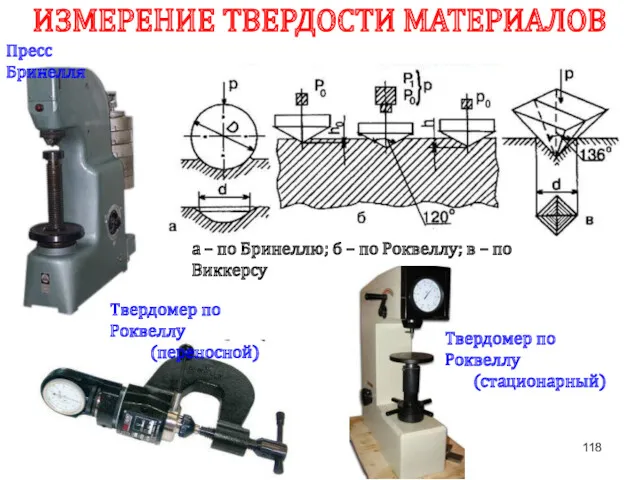
- 118. Пресс Бринелля ИЗМЕРЕНИЕ ТВЕРДОСТИ МАТЕРИАЛОВ а – по Бринеллю; б – по Роквеллу; в – по
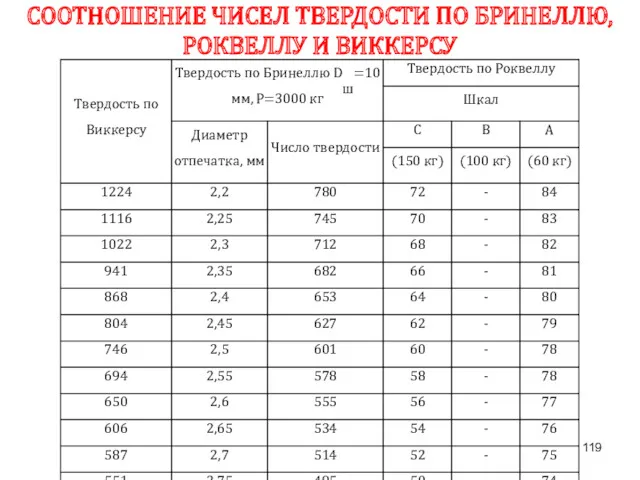
- 119. СООТНОШЕНИЕ ЧИСЕЛ ТВЕРДОСТИ ПО БРИНЕЛЛЮ, РОКВЕЛЛУ И ВИККЕРСУ
- 120. Методы HB и HRB применяют для мягких материалов; HRC – для твердых материалов (например, закаленных сталей);
- 121. ТЕРМИЧЕСКАЯ ОБРАБОТКА Термическая обработка – получение заданных свойств. Параметры термической обработки: Максимальная температура нагрева – Тmax.
- 122. ОСНОВНЫЕ ВИДЫ ТЕРМИЧЕСКОЙ ОБРАБОТКИ Отжиг (первого рода) – термическая операция, состоящая в нагреве металла, имеющего неустойчивое
- 123. СЛОЖНЫЕ ВИДЫ ТЕРМИЧЕСКОЙ ОБРАБОТКИ Химико-термическая обработка – нагрев сплава в соответствующих химических реагентах для изменения состава
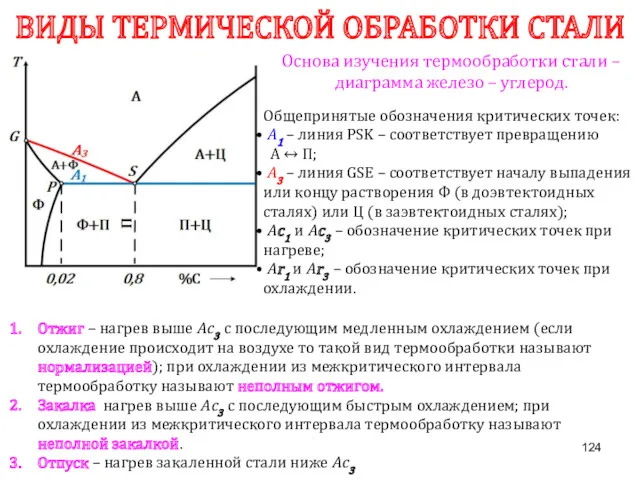
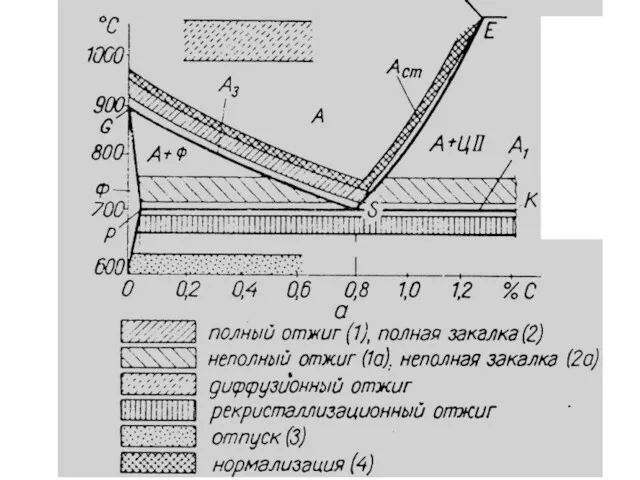
- 124. ВИДЫ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ Основа изучения термообработки стали – диаграмма железо – углерод. Общепринятые обозначения критических
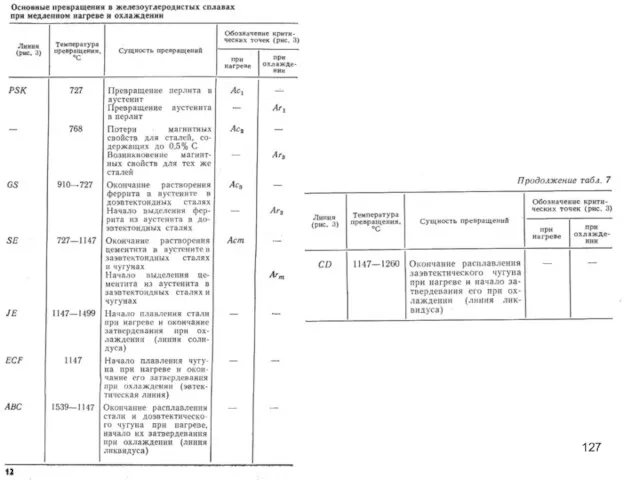
- 126. Основные превращения в стали при термической обработке Превращение перлита в аустенит при нагреве: П→А. Превращение аустенита
- 128. Практическое значение температуры рекристаллизации Горячая обработка давлением – пластическое деформирование выше температуры рекристаллизации. При этом упрочнение
- 129. ОБРАЗОВАНИЕ АУСТЕНИТА При обычных условиях нагрева: Для начала превращения необходим перегрев выше А1. Превращение происходит в
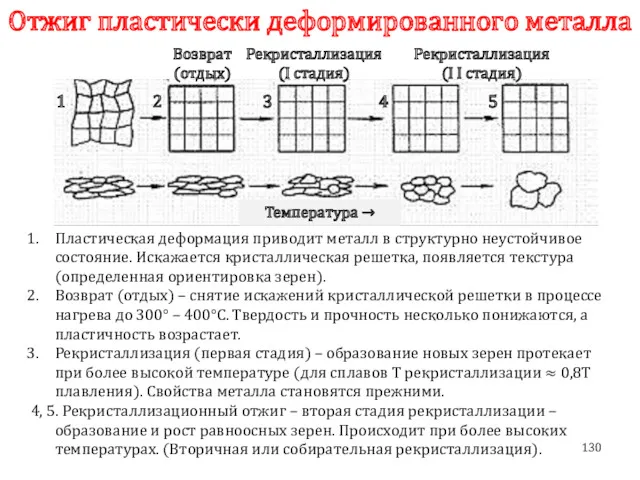
- 130. Отжиг пластически деформированного металла 1 2 3 4 5 Пластическая деформация приводит металл в структурно неустойчивое
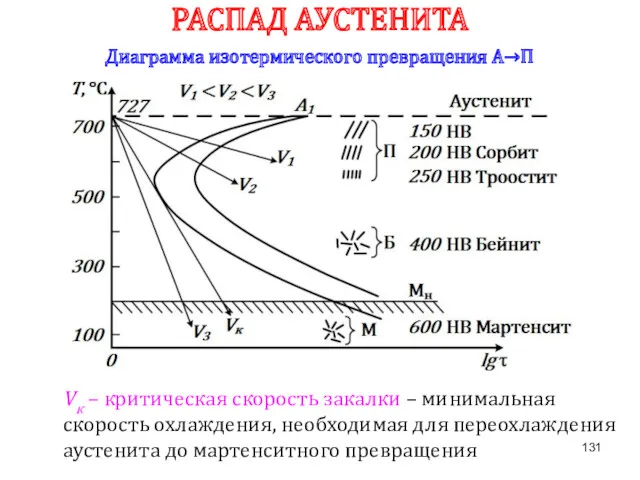
- 131. Vк – критическая скорость закалки – минимальная скорость охлаждения, необходимая для переохлаждения аустенита до мартенситного превращения
- 132. ПРЕВРАЩЕНИЯ ПРИ ОТПУСКЕ Исходная структура: мартенсит – структура закаленной стали, обладающая наибольшим объемом (аустенит – минимальным).
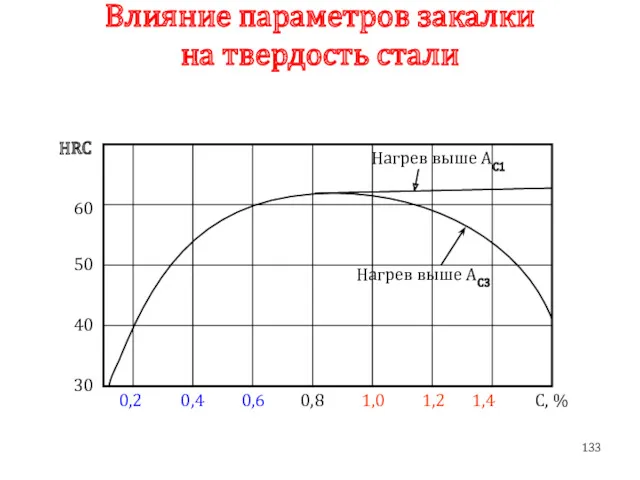
- 133. Влияние параметров закалки на твердость стали 30 40 50 60 HRC 0,2 0,4 0,6 0,8 1,0
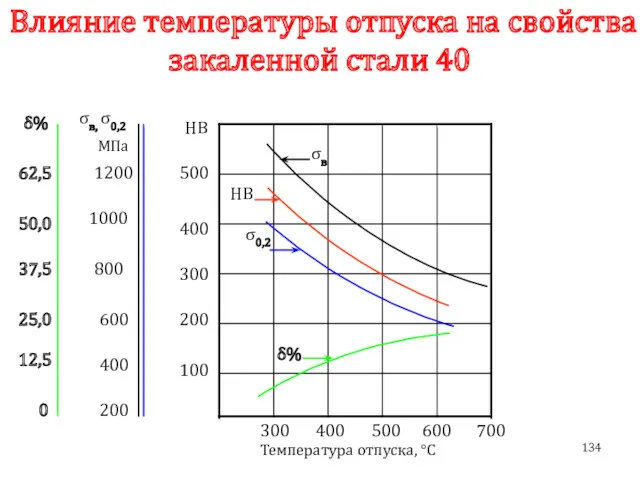
- 134. Влияние температуры отпуска на свойства закаленной стали 40 200 0 300 400 500 600 Температура отпуска,
- 135. ПРАКТИКА ТЕРМИЧЕСКОЙ ОБРАБОТКИ Закалка стали Закаливаемость – характеризуется максимальным значением твердости, приобретенным сталью в результате закалки.
- 136. ВНУТРЕННИЕ НАПРЯЖЕНИЯ ПРИ ЗАКАЛКЕ Внутренние напряжения первого рода (термические): зональные внутренние напряжения, возникающие между отдельными зонами
- 138. Скачать презентацию





























































 Обратимость химических реакций. Обратимые и необратимые химические реакции. Химическое равновесие
Обратимость химических реакций. Обратимые и необратимые химические реакции. Химическое равновесие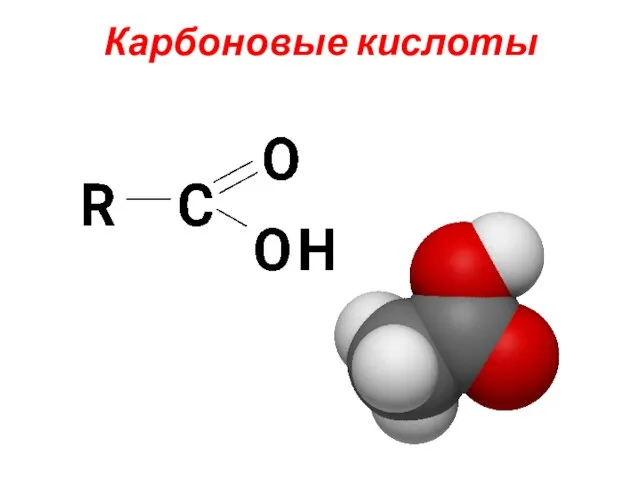 Карбоновые кислоты. Классификация карбоновых кислот
Карбоновые кислоты. Классификация карбоновых кислот Классы неорганических веществ (лекция № 4)
Классы неорганических веществ (лекция № 4) Взрывоопасные грузы
Взрывоопасные грузы Кремний и его соединения
Кремний и его соединения Коллоидная химия
Коллоидная химия Вывод формул веществ по массовым долям элементов. 10 класс
Вывод формул веществ по массовым долям элементов. 10 класс Чистые вещества и смеси. Способы разделения смесей
Чистые вещества и смеси. Способы разделения смесей Лекция_3_Химические_и_физические_свойства_алканов_и_циклоалканов (1)
Лекция_3_Химические_и_физические_свойства_алканов_и_циклоалканов (1) Азотная кислота
Азотная кислота Типы химических реакций
Типы химических реакций Оксиды, их классификация и свойства
Оксиды, их классификация и свойства Кристаллы и минералы
Кристаллы и минералы Знатоки химии. Викторина
Знатоки химии. Викторина Особенности строения, реакционной способности и методы синтеза карбоновых кислот и функциональных производных
Особенности строения, реакционной способности и методы синтеза карбоновых кислот и функциональных производных Свойства смесей ПАВ
Свойства смесей ПАВ Реологические свойства полимеров
Реологические свойства полимеров Камни и Телец
Камни и Телец Химическая связь
Химическая связь Основные понятия и законы химии
Основные понятия и законы химии Основные положения теории растворов электролитов, используемых в аналитической химии
Основные положения теории растворов электролитов, используемых в аналитической химии Химические профессии на стройках Олимпиады
Химические профессии на стройках Олимпиады Гибридизация атомных орбиталей
Гибридизация атомных орбиталей Көмірсутектерді пиролиздеу арқылы қарапайым олефиндерді алу
Көмірсутектерді пиролиздеу арқылы қарапайым олефиндерді алу Номенклатура органических соединений
Номенклатура органических соединений Қышқылдар мен сілтілер тепе-теңдігі
Қышқылдар мен сілтілер тепе-теңдігі Открытие Д.И. Менделеевым периодического закона. Периодическая система химических элементов
Открытие Д.И. Менделеевым периодического закона. Периодическая система химических элементов Неметаллические и композиционные материалы
Неметаллические и композиционные материалы