Открытие Д.И. Менделеевым периодического закона. Периодическая система химических элементов презентация
Содержание
- 2. Домашняя работа Какое число молекул содержится в 2,5 моль O2? N(O2)=n·Na= 2,5·6·1023=1,5·1024 молекул n=N/Na N=n·Na
- 3. Еще алхимики пытались найти закон природы, на основе которого можно было бы систематизировать химические элементы. Но
- 4. Триады Дёберейнера В 1829 году немецкий химик Иоганн Вольфганг Дёберейнер предпринял первую значимую попытку систематизации элементов.
- 5. Спираль Шанкуртуа Недостатком спирали Шанкуртуа было то обстоятельство, что на одной линии с близкими по своей
- 6. В 1865 году английский химик Джон Александр Ньюлендс упорядочил элементы в соответствии с их атомными массами
- 7. В 1870 году появилась первая таблица немецкого химика Ю.Л. Мейера под названием « Природа элемента, как
- 8. В основе классификации два их основных признака: величина атомной массы свойства образованных химическими элементами веществ Открытие
- 9. Свойства химических элементов и образуемых ими соединений находятся в периодической зависимости от величины заряда их атомных
- 10. Периодическая таблица химических элементов Открытый Д. И. Менделеевым закон и построенная на основе закона периодическая система
- 13. Периоды Периоды - горизонтальные ряды химических элементов, всего 7 периодов. Периоды делятся на малые (I,II,III) и
- 14. Каждый период (за исключением первого) начинается типичным металлом (Li, Nа, К, Rb, Cs, Fr) и заканчивается
- 15. Группы вертикальные столбцы элементов с одинаковым числом электронов на внешнем электронном уровне, равным номеру группы.
- 16. Различают главные (А) и побочные подгруппы (Б). Главные подгруппы состоят из элементов малых и больших периодов.
- 17. Зеленые – Металлы Желтые- неметаллы
- 19. Скачать презентацию
 Углеводы. Общая характеристика углеводов
Углеводы. Общая характеристика углеводов Открытие Периодического закона
Открытие Периодического закона Студенттің өзіндік жұмысы
Студенттің өзіндік жұмысы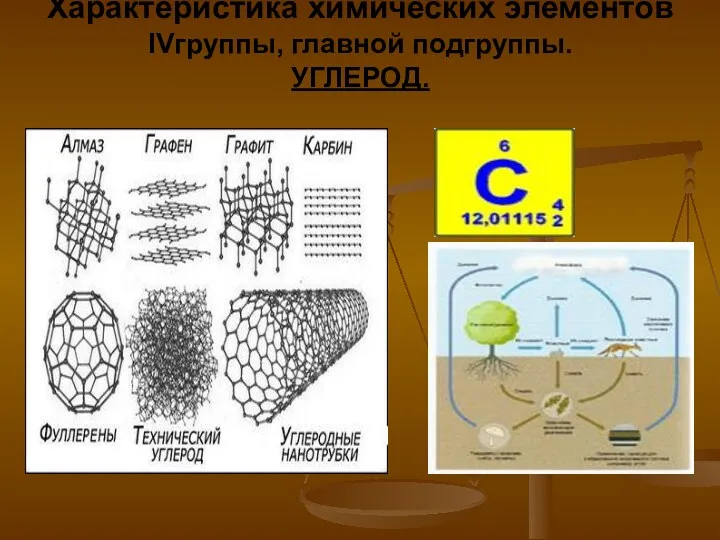 Характеристика химических элементов IV группы, главной подгруппы. Углерод
Характеристика химических элементов IV группы, главной подгруппы. Углерод Закономерности изменения свойств элементов в периодах и группах. Химия. 8 класс
Закономерности изменения свойств элементов в периодах и группах. Химия. 8 класс Нефть. Лекция 5
Нефть. Лекция 5 Водород и щелочные металлы
Водород и щелочные металлы Iodine
Iodine Продолжение лекции Химическая связь
Продолжение лекции Химическая связь Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Самоспалахування. Фактори, що впливають на температуру самоспалахування. Лекція 5
Самоспалахування. Фактори, що впливають на температуру самоспалахування. Лекція 5 Строение атома и периодический закон. (Тема 2)
Строение атома и периодический закон. (Тема 2) циклоалканы170
циклоалканы170 Химическая промышленность
Химическая промышленность Основные положения теории растворов электролитов, используемых в аналитической химии
Основные положения теории растворов электролитов, используемых в аналитической химии Описание основных типов магматических горных пород
Описание основных типов магматических горных пород Физико-химические свойства сырья, продукции, реагентов и материалов (часть 2)
Физико-химические свойства сырья, продукции, реагентов и материалов (часть 2) Хозяйственный механизм НГХК
Хозяйственный механизм НГХК Растворы. Концентрация растворов
Растворы. Концентрация растворов Органические производные титана со связью Ti-C
Органические производные титана со связью Ti-C Роль хімії у суспільстві
Роль хімії у суспільстві Приборы и методы исследования в химической технологии
Приборы и методы исследования в химической технологии Кислоты и их свойства
Кислоты и их свойства Применение центрифугирования
Применение центрифугирования Тұндыру әдістері
Тұндыру әдістері В мире химии. Периодический закон и ПСХЭ
В мире химии. Периодический закон и ПСХЭ Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Основные свойства жиров и их роль в жизни человека
Основные свойства жиров и их роль в жизни человека