Содержание
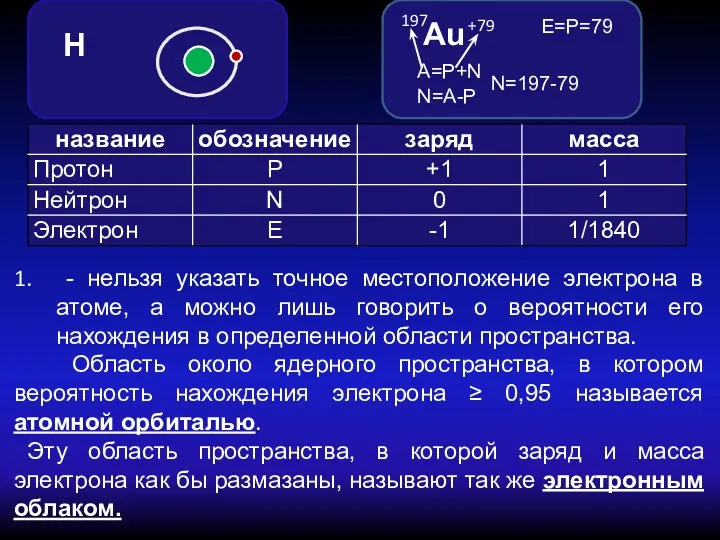
- 2. - нельзя указать точное местоположение электрона в атоме, а можно лишь говорить о вероятности его нахождения
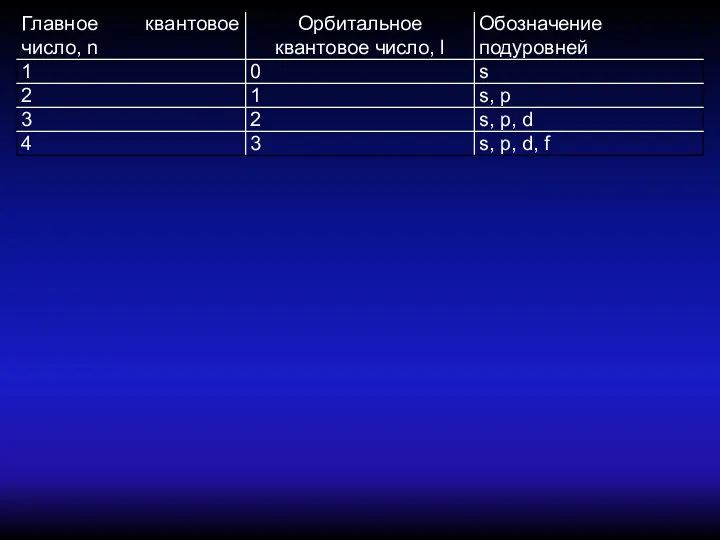
- 3. 2. - Электрон в атоме может иметь не любые, а только строго определенные значения энергии Главное
- 5. Энергия подуровней одного и того же уровня возрастает в ряду Es Форма орбитали S - подуровня
- 6. Спиновое квантовое число « ms » не связано с движением электрона относительно ядра, а определяет его
- 8. Принцип Паули и правило Гунда. Согласно принципу минимальной энергии электроны заполняют уровни и подуровни в порядке
- 9. Правило Гунда: заполнение орбиталей в атоме начинается одиночными электронами с одинаковыми значениями спиновых чисел. Заполнение орбиталей
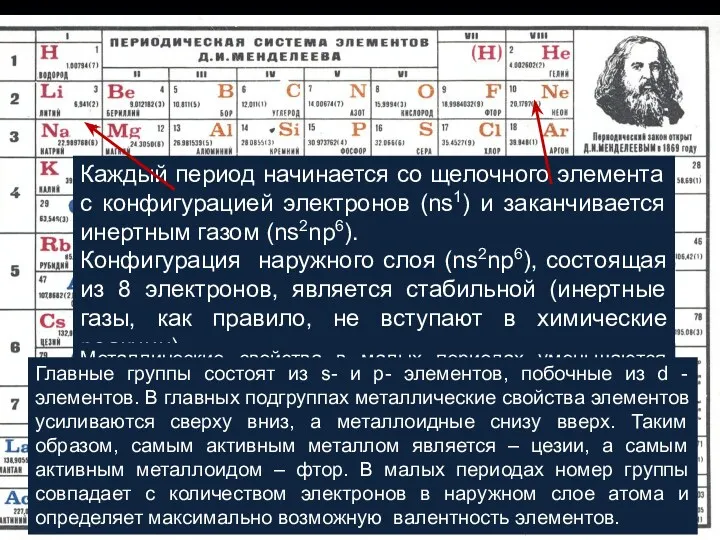
- 10. Периодическая система элементов Д.И. Менделеева Периодический закон открыт в 1869 г. Современная формулировка закона: «Свойства химических
- 11. Металлические свойства в малых периодах уменьшаются слева – направо, а металлоидные – усиливаются. Главные группы состоят
- 12. Электроотрицательности элементов по Полингу Способность атомов при образовании молекул притягивать к себе электроны других атомов называется
- 13. Список литературы Вовченко Г.Д.Третьяков Ю.Д. Общая химия 1980 2. Глинка Н.Л. Общая химия 2000 3. Глазов
- 14. Химическая связь Под химической связью понимаются различные взаимодействия, обуславливающие устойчивое состояние молекул, ионов, кристаллов и иных
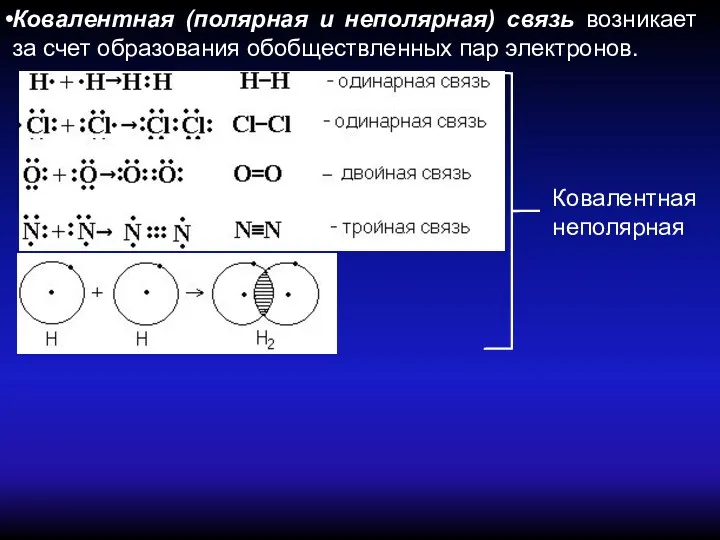
- 15. Ковалентная (полярная и неполярная) связь возникает за счет образования обобществленных пар электронов. Ковалентная неполярная
- 16. Если Э.О. взаимодействующих атомов различны, но не очень отличаются, то между ними возникает ковалентная полярная связь.
- 17. Условный заряд, возникающий у атомов при образовании молекул за счет смещения электронов, называется степенью окисления (С.О.)
- 18. Связь межмолекулярная При сближении молекул газа между ними возникает притяжение, что обуславливает образование жидкого и твердого
- 19. Индукционное взаимодействие. Диполи могут воздействовать на неполярные молекулы, превращая их в индуцированные (наведенные) диполи. Притяжение, возникающие
- 21. Скачать презентацию














 Карбоновые кислоты. Тест
Карбоновые кислоты. Тест Кремний и его соединения
Кремний и его соединения Водородная связь
Водородная связь Природные источники углеводородов, их переработка, применение и экологические проблемы
Природные источники углеводородов, их переработка, применение и экологические проблемы Металлы и их свойства. Способы получения
Металлы и их свойства. Способы получения Органическая химия. Вещества
Органическая химия. Вещества Магматизм. (Лекция 6)
Магматизм. (Лекция 6) Кислород
Кислород Спроби класифікації хімічних елементів
Спроби класифікації хімічних елементів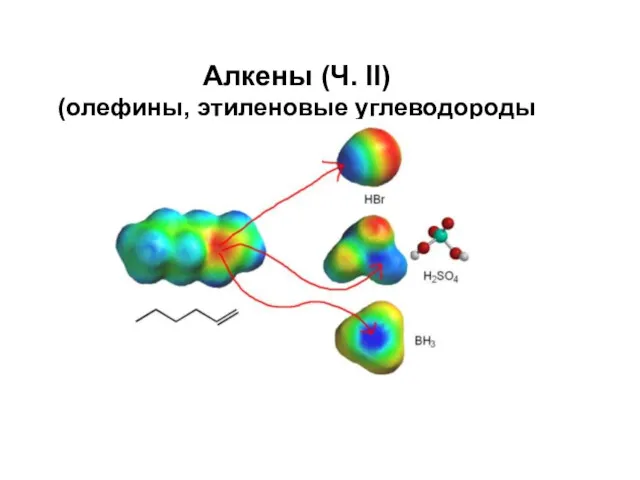 Алкены (олефины, этиленовые углеводороды)
Алкены (олефины, этиленовые углеводороды) Прочность полимеров
Прочность полимеров Амфотерные органические и неорганические соединения
Амфотерные органические и неорганические соединения Буферные растворы
Буферные растворы Місце хімії серед наук про природу
Місце хімії серед наук про природу Химические волокна
Химические волокна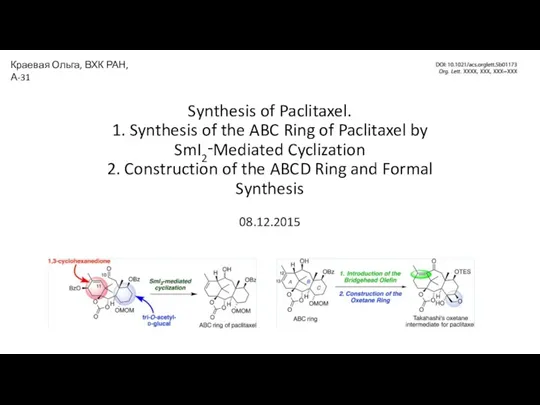 Synthesis of Paclitaxel
Synthesis of Paclitaxel Строение атома. 8 класс
Строение атома. 8 класс Лекция 3. Разновидности химических связей
Лекция 3. Разновидности химических связей Витамины. Ашылу тарихы
Витамины. Ашылу тарихы ГИА-9 Химия. А4
ГИА-9 Химия. А4 Массовая и объемная доли компонентов смеси (раствора)
Массовая и объемная доли компонентов смеси (раствора) Классификация органических соединений, углеводородов
Классификация органических соединений, углеводородов Рідкі кристали
Рідкі кристали Спирты
Спирты Химические уравнения
Химические уравнения Вещества молекулярного и немолекулярного строения
Вещества молекулярного и немолекулярного строения Применение алюминия и его сплава в машиностроении
Применение алюминия и его сплава в машиностроении Химическая связь. 8 класс
Химическая связь. 8 класс