Строение атома пз и пс Д.И. Менделеева в свете квантовомеханической теории строения атома презентация
Содержание
- 2. Ученые древности о строении вещества Древнегреческий ученый Демокрит 2500 лет назад считал, что любое вещество состоит
- 3. Наименьшая электронейтральная частица химического элемента, являющаяся носителем его свойств. Атом
- 4. В 1808 г. английский химик Дальтон сформулировал атомистическую теорию. «Все вещества состоят из атомов, мельчайших неделимых
- 5. Джозеф Джон Томсон(1856-1940) В конце 19-го века открыл электрон. Масса электрона оказалась примерно в две тысячи
- 6. Модель атома Томсона Внутри положительно заряженного шара диаметром около 10 м находятся отрицательно заряженные электроны. -10
- 7. Эрнест Резерфорд(1871-1937) В начале 20-го века английский физик Эрнест Резерфорд открыл атомное ядро. Оказалось, что в
- 8. Планетарная модель атома Резерфорда в центре атома - положительно заряженное ядро : заряд ядра q =
- 9. В 1913 г Нильс Бор (Дания) предположил, что электрон движется не по любым, а лишь по
- 11. Изотопы. Так называются атомы, имеющие одинаковый заряд ядра , но различную массу. Все изотопы одного и
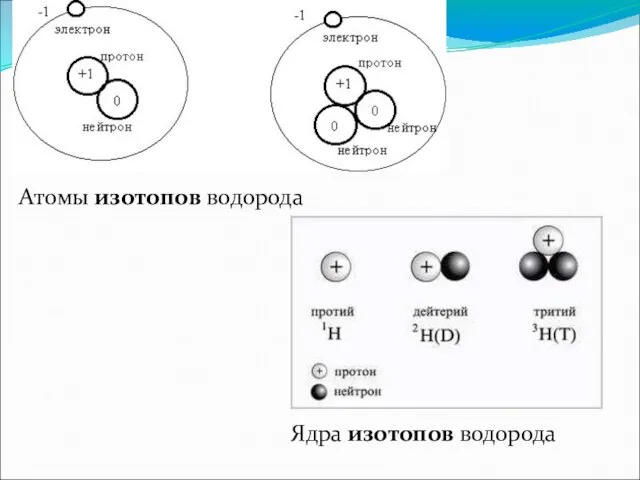
- 12. Атомы изотопов водорода Ядра изотопов водорода
- 13. В 1924 г французский учёный Луи де Бройль высказал предположение о двойственной природе материальных частиц, в
- 14. 1. Электрон в атоме можно рассматривать как частицу, которая при движении проявляет волновые свойства. Т.е. нельзя
- 15. …электронным облаком. … атомной орбиталью (АО) (или электронной плотностью). Термин "орбита" (из модели Бора) в волновой
- 16. Важным следствием теории квантовой механики является то, что вся совокупность сложных движений электрона в атоме описывается
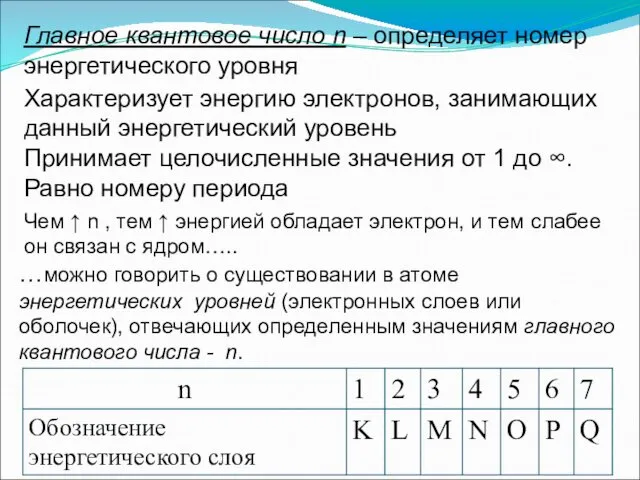
- 17. Главное квантовое число n – определяет номер энергетического уровня Принимает целочисленные значения от 1 до ∞.
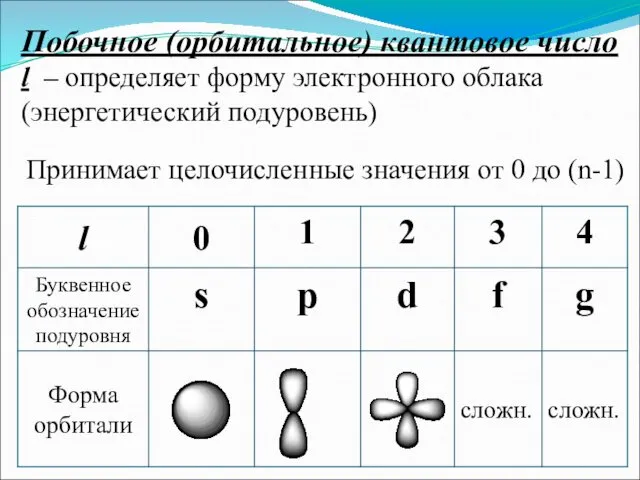
- 18. Побочное (орбитальное) квантовое число l – определяет форму электронного облака (энергетический подуровень) Принимает целочисленные значения от
- 19. Число подуровней, на которые расщепляется энергетический уровень равно номеру уровня. Например, Т.о., энергетический подуровень – это
- 20. Магнитное квантовое число ml – Оно принимает все целочисленные значения от – l до + l.
- 21. Следовательно, можно сказать, что число значений ml указывает на число орбиталей с данным значением l. s-cостоянию
- 23. Состояние электрона в атоме, характеризующееся определенными значениями чисел n, l,ml называется атомной орбиталью.
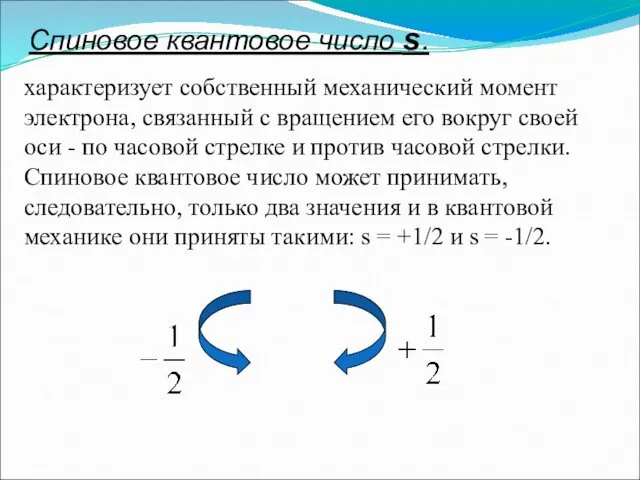
- 24. Спиновое квантовое число s. характеризует собственный механический момент электрона, связанный с вращением его вокруг своей оси
- 25. Общая характеристика состояния электрона в многоэлектронном атоме определяется принципом Паули: в атоме не может быть двух
- 26. Электронные конфигурации атомов (порядок заполнения атомных орбиталей) Принцип min энергии – электроны занимают в первую очередь
- 27. Может быть заполнение электронами энергетических уровней и подуровней идет в следующем порядке: …3s 3p 3d 4s
- 28. Последовательность заполнения электронами уровней и подуровней: 1s22s22p63s23p64s23d104p65s24d105p66s2 4f145d106p67s25f146d107p6…
- 29. При наличии однотипных орбиталей их заполнение происходит в соответствии с правилом Хунда: в пределах энергетического подуровня
- 30. Атом хлора +17 Cl )2 )8 )7 схема строения атома. 1s2 2s2 2p6 3s2 3p5 это
- 31. «Проскок» электрона Установлено, что у d-орбиталей особо устойчивыми конфигурациями являются d5 и d10 , а у
- 32. Периодический закон Д.И. Менделеева. Открыт в 1869 г. великим русским ученым Д.М. Менделеевым. “Свойства элементов и
- 33. Первым вариантом системы элементов, предложенным Д. И. Менделеевым 1 марта 1869 г., был так называемый вариант
- 36. Периодом в ПС называется – горизонтальный ряд элементов, в пределах которого свойства элементов изменяются последовательно. Элементы
- 37. Периодически меняющиеся свойства атомов Атомные и ионные радиусы 2. Энергия ионизации 3. Сродство к электрону 4.
- 38. Эффективный атомный радиус – радиус сферы действия атома или иона Атомные радиусы – характеристика атома, позволяющая
- 39. 2. Энергия ионизации (Еион) [кДж/моль] или [эВ/атом] (1эВ/атом= 100 кДж/моль. ) – минимальная энергия, необходимая для
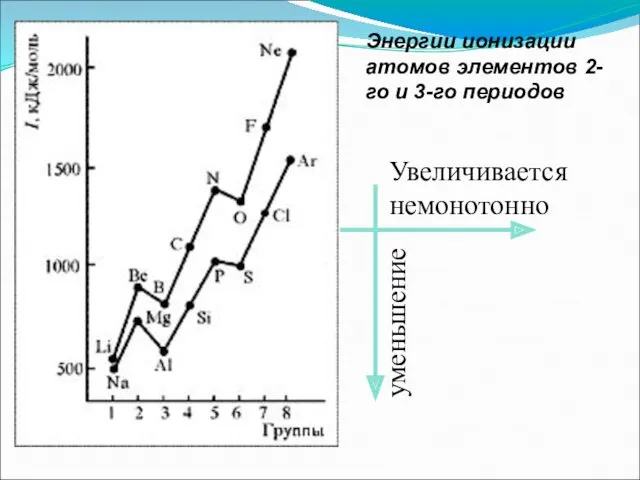
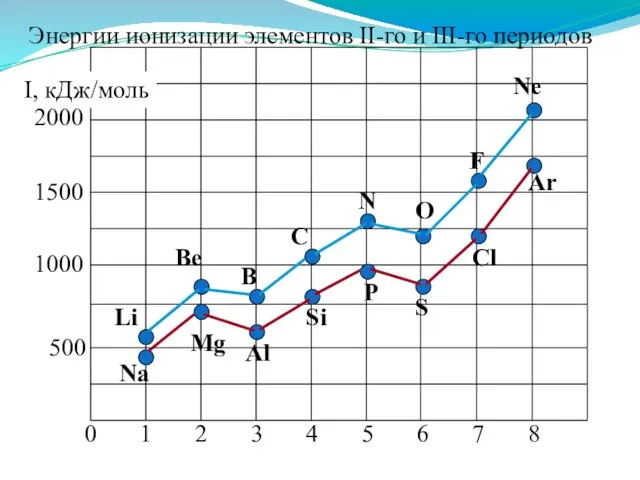
- 40. Энергии ионизации атомов элементов 2-го и 3-го периодов Увеличивается немонотонно уменьшение
- 42. Анализ изменения Еион позволяет сделать некоторые выводы: 1. В периодах Еион ↑, что вызвано сжатием электронной
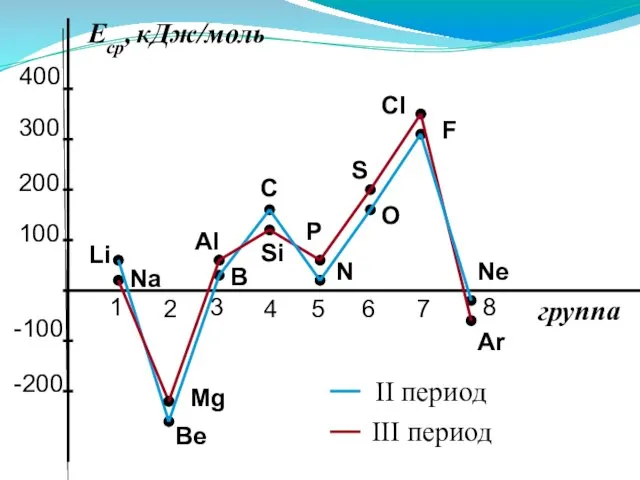
- 43. 2. Сродство к электрону (Еср.) [кДж/моль] или [эВ/атом] - энергетический эффект присоединения электрона к нейтральному атому
- 45. Анализ изменения СЭ позволяет сделать некоторые выводы: 1. Min (отрицательное) СЭ наблюдается у атомов, имеющих завершенные
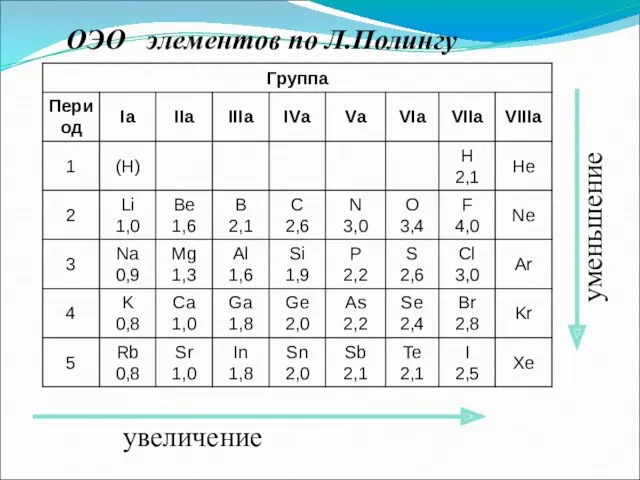
- 46. 3. Электроотрицательность (χ) [кДж/моль] или [эВ/атом] – характеризует способность атома в химическом соединении притягивать к себе
- 47. увеличение уменьшение ОЭО элементов по Л.Полингу
- 49. Скачать презентацию
































![2. Энергия ионизации (Еион) [кДж/моль] или [эВ/атом] (1эВ/атом= 100 кДж/моль.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/108724/slide-38.jpg)

![2. Сродство к электрону (Еср.) [кДж/моль] или [эВ/атом] - энергетический](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/108724/slide-42.jpg)

![3. Электроотрицательность (χ) [кДж/моль] или [эВ/атом] – характеризует способность атома](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/108724/slide-45.jpg)
 Генетическая связь между классами веществ
Генетическая связь между классами веществ Эколого-химическая характеристика качества почвы
Эколого-химическая характеристика качества почвы Химический эквивалент. Формульные единицы
Химический эквивалент. Формульные единицы Свойства алкадиенов и их получение
Свойства алкадиенов и их получение Ионные уравнения реакций
Ионные уравнения реакций Элементы VII группы периодической таблицы Д.И. Менделеева
Элементы VII группы периодической таблицы Д.И. Менделеева Свойства фосфора
Свойства фосфора Азотсодержащие органические соединения
Азотсодержащие органические соединения Ерiтiндiлер туралы iлiм. Сұйытылған бейэлектролит және электролит ерiтiнндiлерiнiң коллигативтiк қасиеттерi
Ерiтiндiлер туралы iлiм. Сұйытылған бейэлектролит және электролит ерiтiнндiлерiнiң коллигативтiк қасиеттерi Месторождения нефрита
Месторождения нефрита Значение органической химии в жизни человека
Значение органической химии в жизни человека Получение и распознавание водорода
Получение и распознавание водорода Метаморфогенные месторождения
Метаморфогенные месторождения Теоретические аспекты химического осаждения из газовой фазы
Теоретические аспекты химического осаждения из газовой фазы Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури
Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури Геохимия ландшафтов
Геохимия ландшафтов ПРИРОДНЫЕ ИСТОЧНИКИ УГЛЕВОДОРОДОВ
ПРИРОДНЫЕ ИСТОЧНИКИ УГЛЕВОДОРОДОВ Цветные металлы и сплавы
Цветные металлы и сплавы Серебро. История
Серебро. История Оксиды (1 этап изучения). 8 класс
Оксиды (1 этап изучения). 8 класс Базовое нефтехимическое сырье
Базовое нефтехимическое сырье Күйдіргіш натрий
Күйдіргіш натрий Никель – тяжелый металл
Никель – тяжелый металл Prezentatsia
Prezentatsia Серная кислота H2SO4
Серная кислота H2SO4 Застосування неметалів
Застосування неметалів Кислород
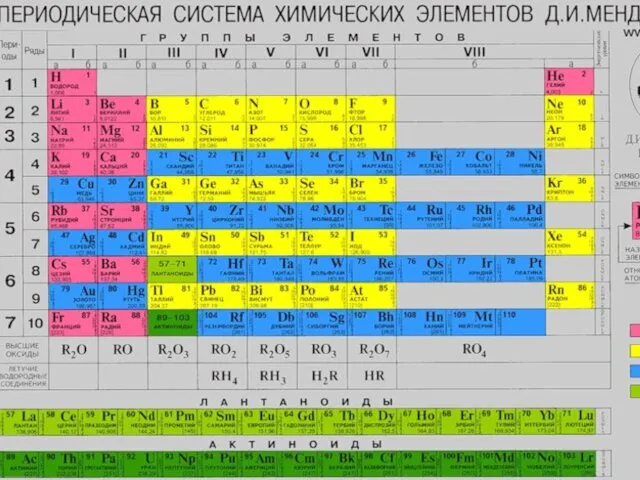
Кислород Периодическая система химических элементов Д.И.Менделеева
Периодическая система химических элементов Д.И.Менделеева