Содержание
- 2. Биохимия (bios – жизнь) – химия жизни; наука о структуре химических веществ, входящих в состав живой
- 3. Биохимия Структурная биохимия – изучает структуру химических веществ, входящих в состав живых организмов. Динамическая биохимия исследует
- 4. Структурная биохимия – разделы Биоэлементы и биомолекулы. Вода. Аминокислоты. Белки. Нуклеиновые кислоты. Углеводы. Водорастворимые витамины. Липиды.
- 5. Особенности живой материи Высокий уровень структурной организации. Способность к преобразованию и использованию энергии. Обмен веществ с
- 6. АМИНОКИСЛОТЫ. ПОЛИПЕПТИДНАЯ ТЕОРИЯ СТРОЕНИЯ БЕЛКОВ
- 7. Аминокислоты – гетерофункциональные соединения, содержащие аминогруппу и карбоксильную группу (производные карбоновых кислот, у которых один атом
- 9. α-аминокислоты – производные карбоновых кислот, у которых один атом водорода в α-положении замещен на аминогруппу. Карбоновая
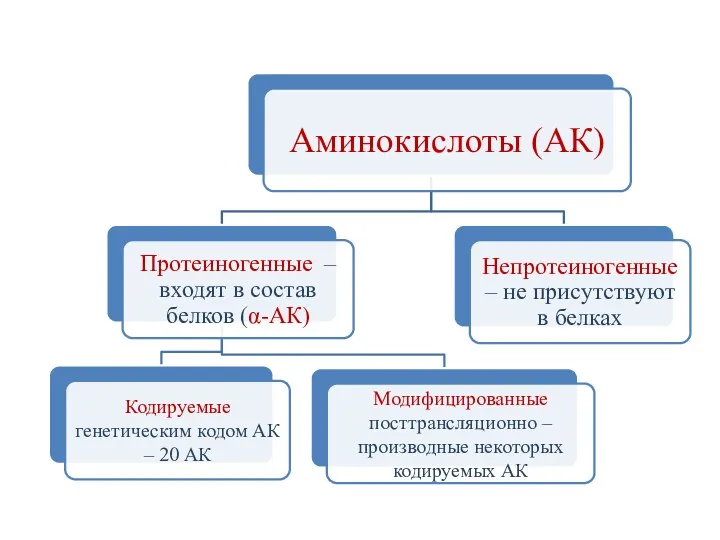
- 10. Стереоизомерия аминокислот За исключением глицина, у всех аминокислот 4 группы, связанные с α-углеродным атомом, различны. Протеиногенные
- 11. Классификация аминокислот Структурный принцип Алифатические аминокислоты: А. Моноаминомонокарбоновые – Gly, Ala, Val, Leu, Ile. В. Моноаминодикарбоновые
- 12. Структура алифатических аминокислот А. Моноаминомонокарбоновые АК Глицин (Gly) Аланин (Ala) Валин (Val) Изолейцин (Ile) Лейцин (Leu)
- 13. В. Моноаминодикарбоновые АК и их амиды Аспарагиновая кислота (Asp ) Аспарагин (Asn) Глутаминовая кислота (Glu) Глутамин
- 14. С. Диаминомонокарбоновые АК Аргинин (Arg) Лизин (Lys) Структура алифатических аминокислот
- 15. Д. Гидроксиаминокислоты Е. Тиоаминокислоты Серин (Ser) Треонин (Thr) Цистеин (Cys) Метионин (Met) Структура алифатических аминокислот
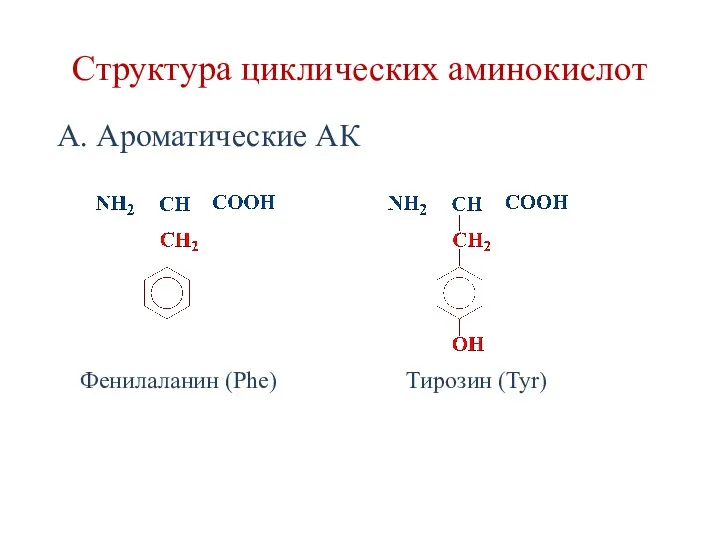
- 16. А. Ароматические АК Тирозин (Tyr) Фенилаланин (Phe) Структура циклических аминокислот
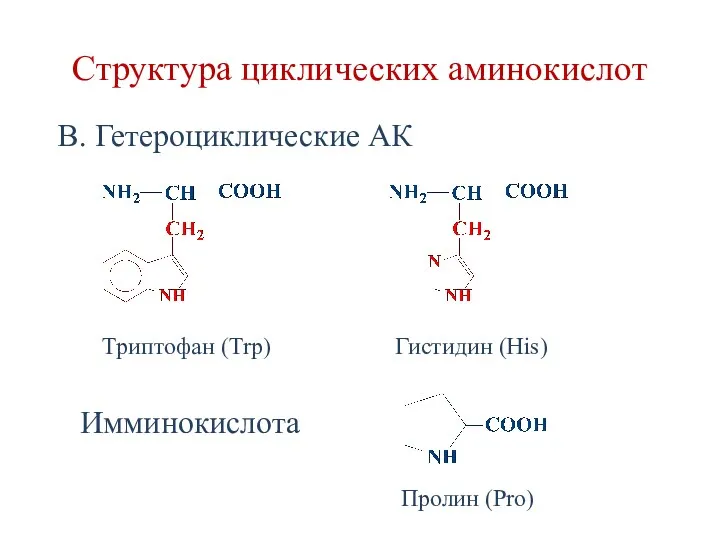
- 17. Структура циклических аминокислот В. Гетероциклические АК Триптофан (Trp) Гистидин (His) Пролин (Pro) Имминокислота
- 18. Классификация аминокислот Биологический принцип Незаменимые (не синтезируются в тканях человеческого организма) – Val, Leu, Ile, Lys,
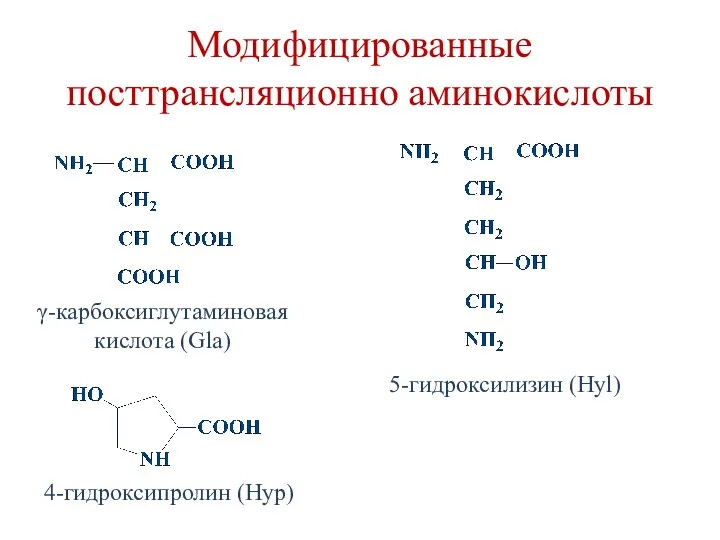
- 19. Модифицированные посттрансляционно аминокислоты 5-гидроксилизин (Hyl) 4-гидроксипролин (Hyp) γ-карбоксиглутаминовая кислота (Gla)
- 20. Модифицированные посттрансляционно аминокислоты 4-гидроксипролин и 5-гидроксилизин синтезируются из пролина и лизина в ходе посттрансляционных изменений в
- 21. Непротеиногенные аминокислоты Гомоцистеин – промежуточное вещество в обмене метионина; фактор риска атеросклероза Орнитин – промежуточное вещество
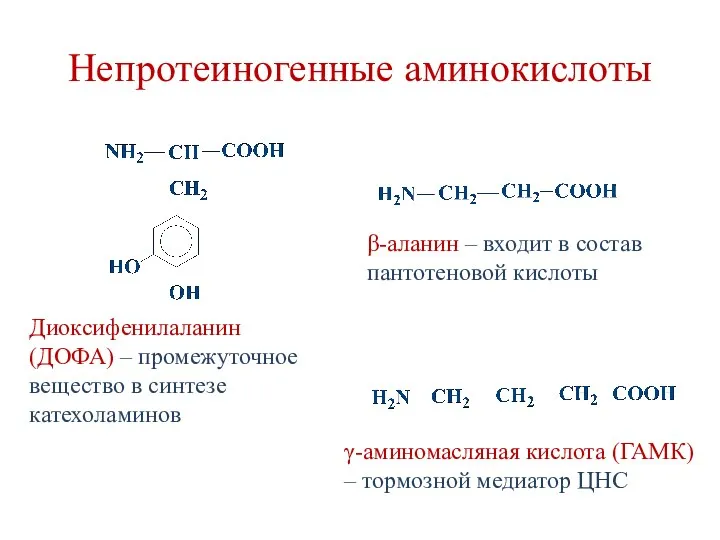
- 22. Непротеиногенные аминокислоты Диоксифенилаланин (ДОФА) – промежуточное вещество в синтезе катехоламинов β-аланин – входит в состав пантотеновой
- 23. Электрохимические свойства аминокислот Аминокислоты имеют минимум одну карбоксильную (кислую) группу и одну аминогруппу (основную), поэтому обладают
- 24. Электрохимический принцип классификации аминокислот Нейтральные аминокислоты. Кислые аминокислоты – Glu, Asp. Основные аминокислоты – Lys, Arg,
- 25. Кислые аминокислоты Аспарагиновая кислота (Asp ) Глутаминовая кислота (Glu)
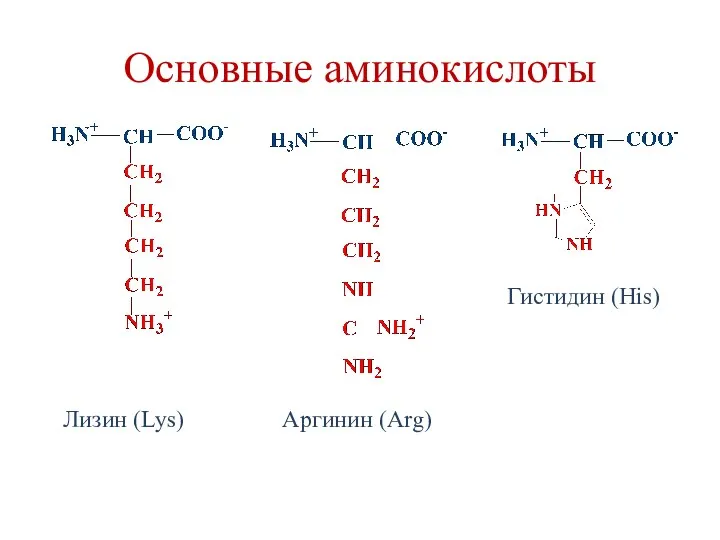
- 26. Основные аминокислоты Аргинин (Arg) Лизин (Lys) Гистидин (His)
- 27. Электрохимические свойства аминокислот Суммарный заряд АК зависит от рН. Значение рН, при котором суммарный заряд АК
- 28. Электрохимические свойства аминокислот рI нейтральных АК – рН около 6. рI кислых АК – кисляя среда
- 29. Электрохимические свойства аминокислот В изоэлектрической точке суммарный заряд аминокислоты = 0, аминокислота не перемещается в электрическом
- 30. Электрохимические свойства аминокислот pH = pI Суммарный заряд = 0 pH Суммарный заряд «+» Катион pH
- 31. Растворимость аминокислот Аминокислоты содержат полярные заряженные и незаряженные группы, поэтому хорошо растворяются в полярных растворителях (вода,
- 32. Классификация аминокислот по растворимости радикалов в воде: Неполярные (гидрофобные) – Gly, Ala, Val, Leu, Ile, Met,
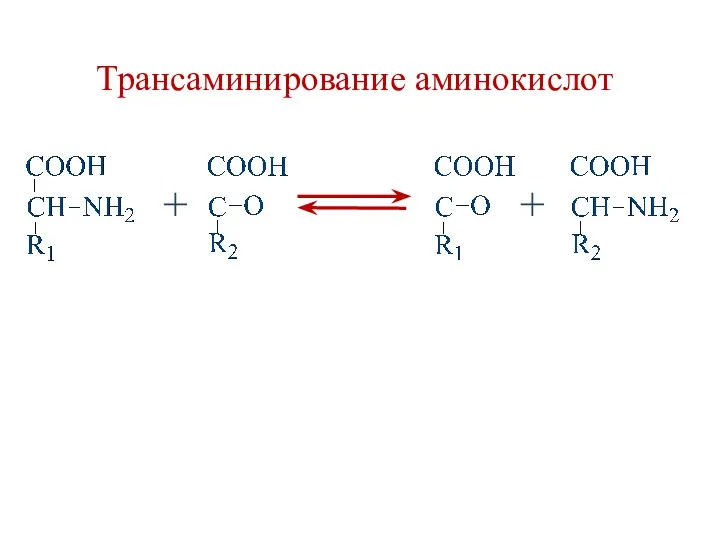
- 33. Трансаминирование (ТА) аминокислот реакция переноса аминогруппы (NH2—) с α-аминокислоты на α-кетокислоту и перенос кетогруппы с α-кетокислоты
- 34. Трансаминирование аминокислот + +
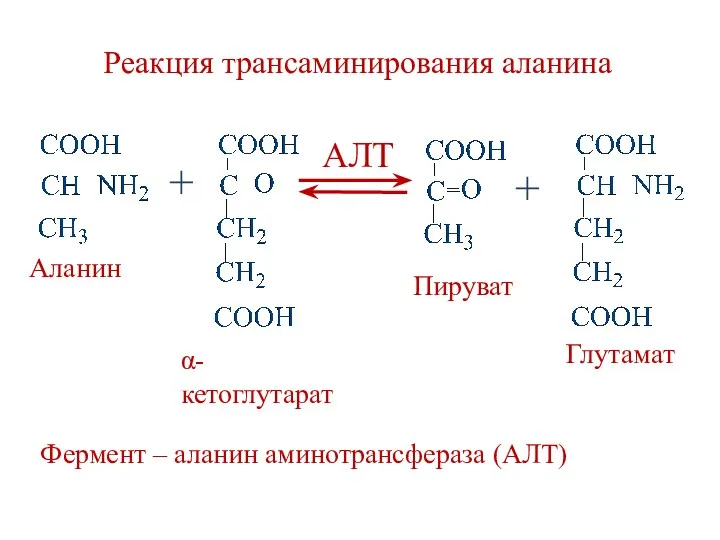
- 35. Реакция трансаминирования аланина Фермент – аланин аминотрансфераза (АЛТ) + + АЛТ Аланин Пируват Глутамат α-кетоглутарат
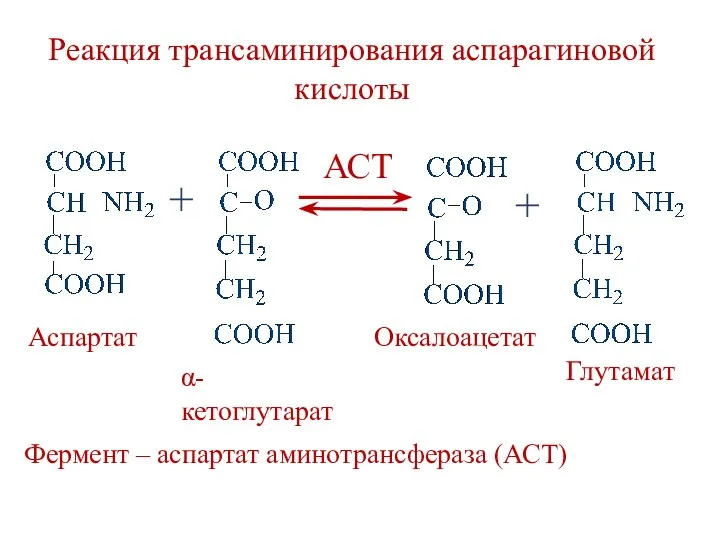
- 36. Реакция трансаминирования аспарагиновой кислоты Фермент – аспартат аминотрансфераза (АСТ) + + АСТ Аспартат Оксалоацетат Глутамат α-кетоглутарат
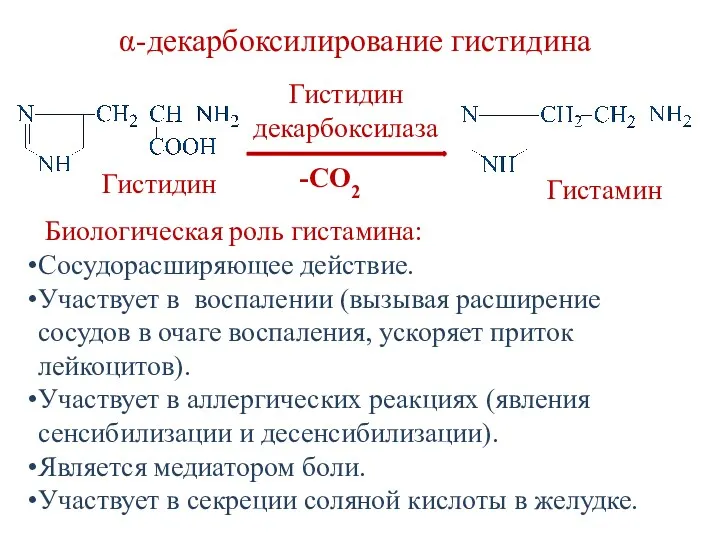
- 37. Декарбоксилирование аминокислот реакция отщепления карбоксильной группы от аминокислот в виде СО2. α-декарбоксилирование аминокислот приводит к образованию
- 38. Биологическая роль гистамина: Сосудорасширяющее действие. Участвует в воспалении (вызывая расширение сосудов в очаге воспаления, ускоряет приток
- 39. α-декарбоксилирование глутаминовой кислоты -СО2 Глутамат декарбоксилаза Глутамат γ-аминомасляная кислота (ГАМК) Тормозящие действие на ЦНС. ГАМК и
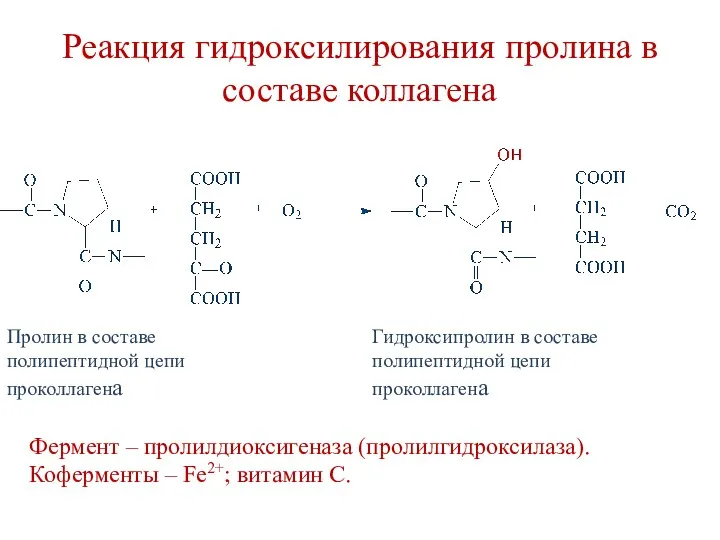
- 40. Реакция гидроксилирования пролина в составе коллагена Пролин в составе полипептидной цепи проколлагена Гидроксипролин в составе полипептидной
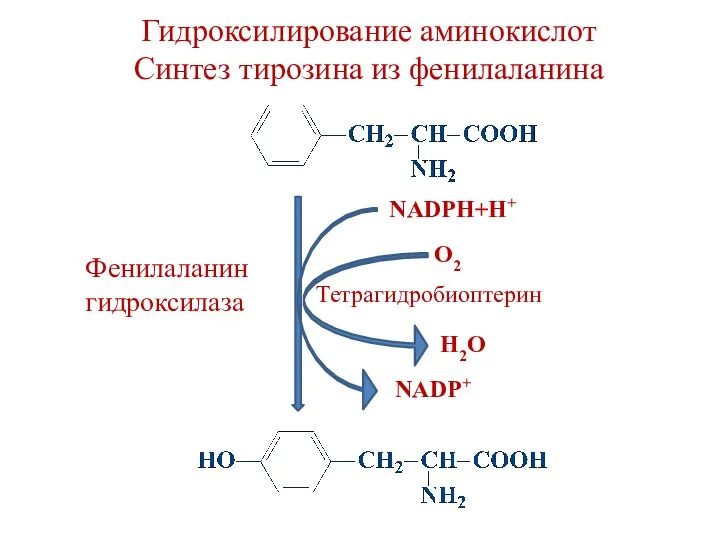
- 41. Гидроксилирование аминокислот Синтез тирозина из фенилаланина NADPH+H+ NADP+ H2O O2 Тетрагидробиоптерин Фенилаланин гидроксилаза
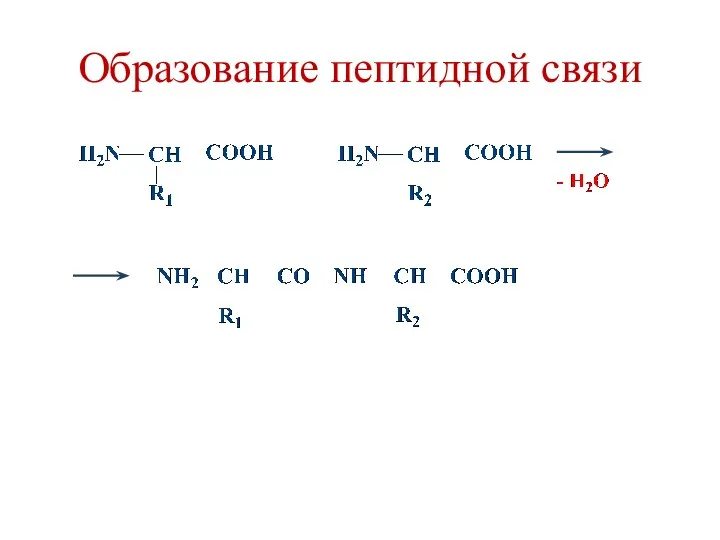
- 42. Полипептидная теория строения белков (Фишер, 1902) Белки являются полипептидами, в которых аминокислоты связаны между собой пептидными
- 43. Образование пептидной связи
- 44. Каждый пептид имеет одну свободную α-аминогруппу (N-конец) и одну свободную α-карбоксильную группу (С-конец). Направление пептидов N→С.
- 45. СТРУКТУРА БЕЛКОВ. КЛАССИФИКАЦИЯ БЕЛКОВ
- 46. Белки – высокомолекулярные азотсодержащие органические вещества, состоящие из аминокислот, соединенных пептидными связями и обладающие сложной структурной
- 47. Функции белков Структурная Опорная, механическая Каталитическая Гормональная, регуляторная Рецепторная Иммунологическая Транспортная Сократительная Резервная Энергетическая
- 48. Уровни структурной организации белков Первичная структура Вторичная структура Третичная структура Четвертичная структура
- 49. Первичная структура белка состав и последовательность аминокислотных остатков в полипептидной цепи. Генетически детерминирована, т.е. закодирована в
- 50. Свойства пептидной связи Частично двойная связь (1,32А), поэтому она короче, чем остальные связи пептидного остова, и
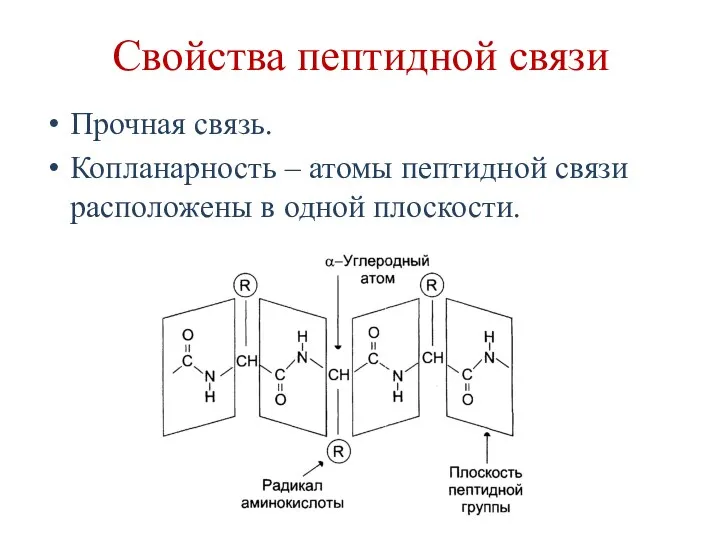
- 51. Свойства пептидной связи Прочная связь. Копланарность – атомы пептидной связи расположены в одной плоскости.
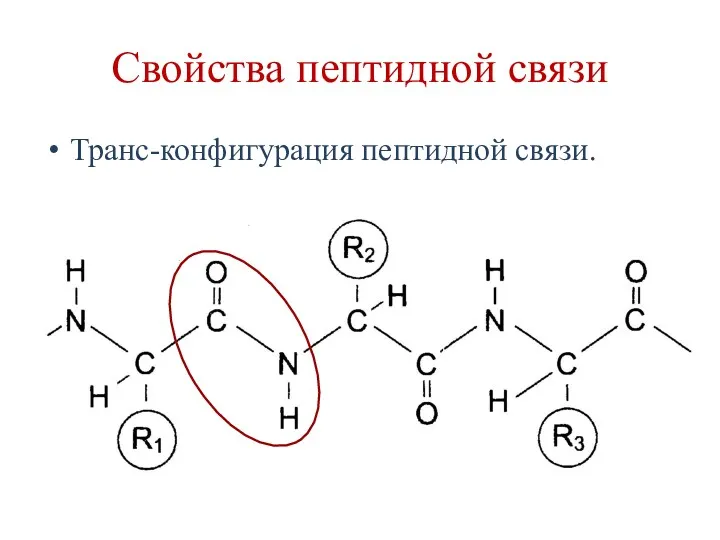
- 52. Свойства пептидной связи Транс-конфигурация пептидной связи.
- 53. Свойства пептидной связи Способность образовать 2 водородные связи. Способность существовать в 2-х таутомерных формах (кето-енол): кето
- 54. Определение первичной структуры белка Два основных этапа: Определение аминокислотного состава; Определение аминокислотной последовательности.
- 55. Определение аминокислотного состава белка – этапы Полный гидролиз белка (кислотный гидролиз). Разделение аминокислот (ионообменная хроматография). Количественный
- 56. Определение аминокислотной последовательности в белке – этапы 1. Определение N-концевой аминокислоты. 2. Определение С-концевой аминокислоты. 3.
- 57. Определение N-концевой аминокислоты Метод Сэнгера. Метод Эдмана.
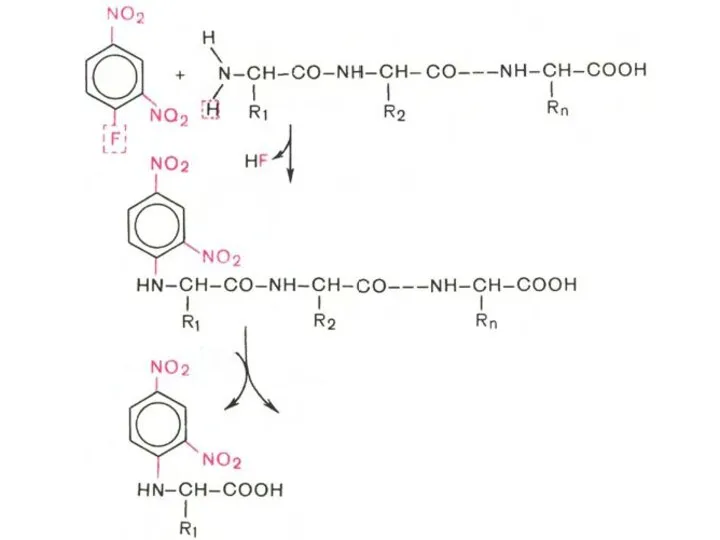
- 58. Определение N-концевой аминокислоты Метод Сэнгера: Используют 2,4-динитрофторбензол, который образует с N-концевой аминокислотой окрашенное в желтый цвет
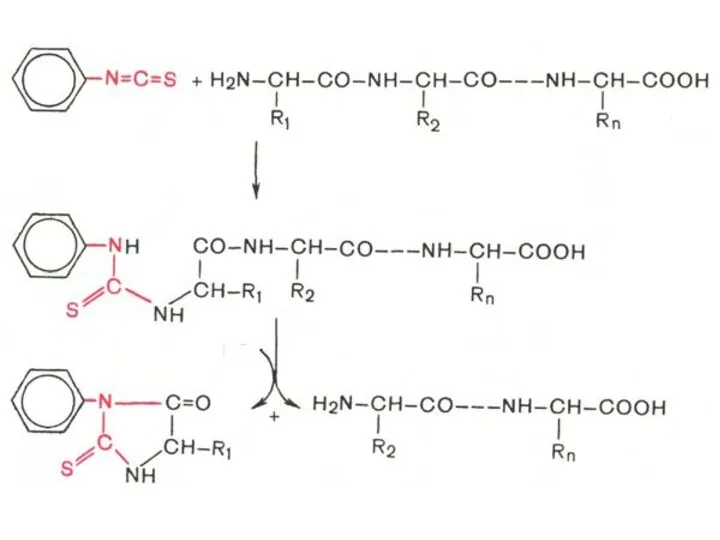
- 60. Определение N-концевой аминокислоты Метод Эдмана: Фенилизотиоцианат реагирует со свободной α-аминогруппой N-концевой аминокислоты полипептида с образованием фенилтиокарбамоилпептида.
- 61. Определение N-концевой аминокислоты Метод Эдмана Обрабатывают продукт реакции кислотой, что приводит к циклизации и освобождению фенилтиогидантоина
- 63. Определение N-концевой аминокислоты Метод Эдмана является основой для определения первичной структуры белков и пептидов в специальном
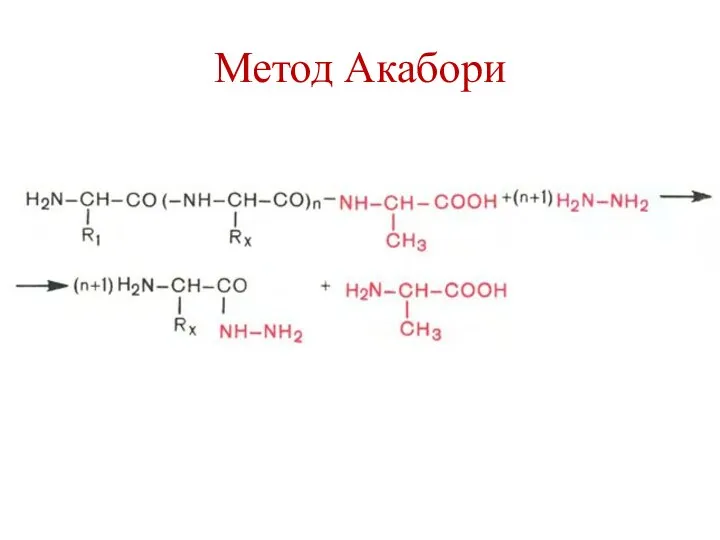
- 64. Определение С-концевой аминокислоты Метод Акабори (гидразин). Обработка боргидридом натрия. Ферментативный метод (карбоксипептидазы).
- 65. Метод Акабори
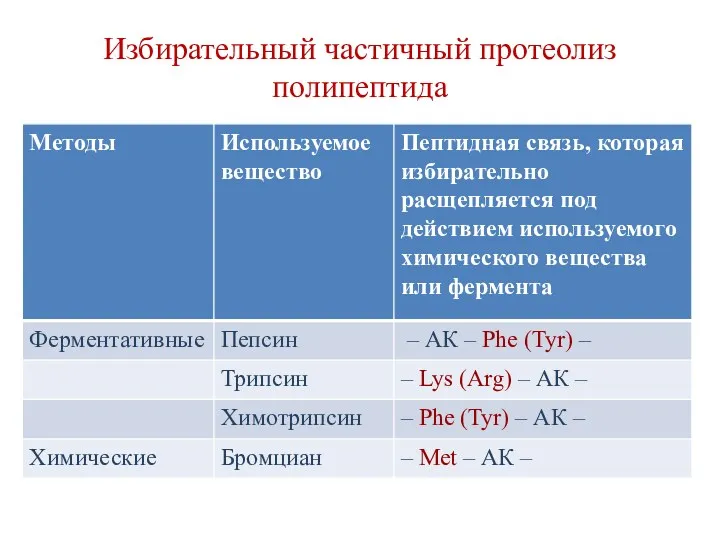
- 66. Избирательный частичный протеолиз полипептида
- 67. Установление аминокислотной последовательности пептида
- 68. Биомедицинское значение определения аминокислотной последовательности белка Изучение закономерностей образования пространственной структуры белков. Диагностика и прогнозирование генетических
- 69. Вторичная структура белка Упаковка полипептидной цепи в упорядоченную структуру. Стабилизируется водородными связями между атомами пептидных связей.
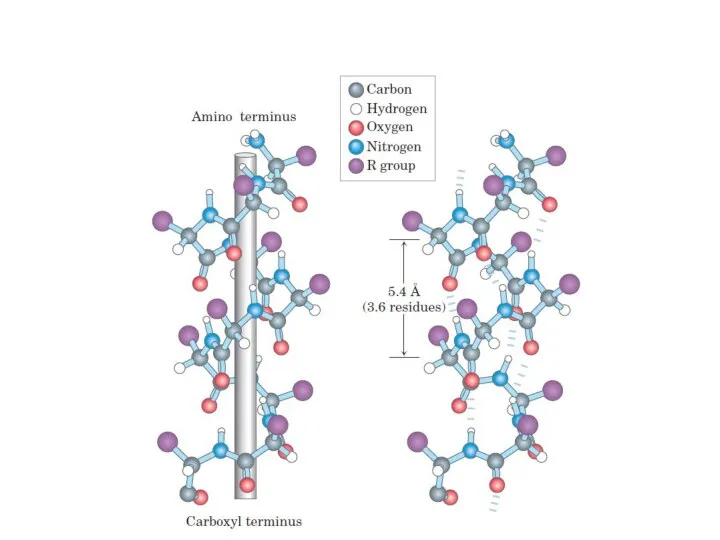
- 70. α-спираль Правозакрученная спираль. 1 виток – 3,6 аминокислот. Водородные связи – между атомами пептидных групп1 и
- 73. Аминокилоты, дестабилизирующие α-спираль Пролин и гидроксипролин; Одинаково заряженные радикалы; Объемные радикалы.
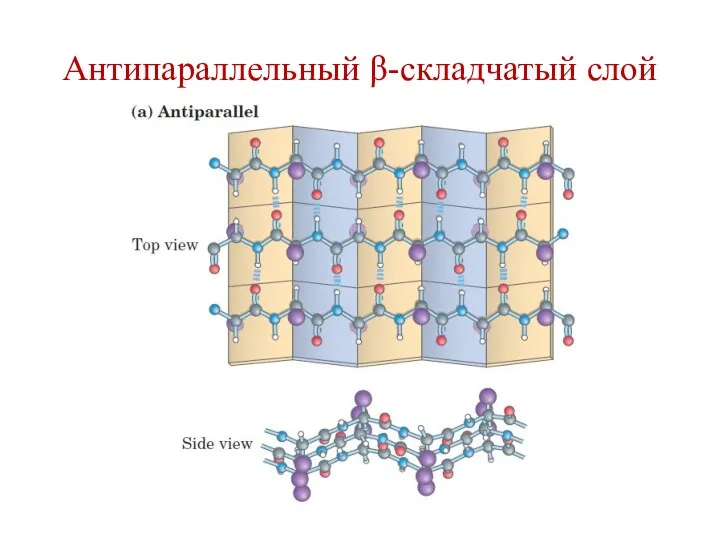
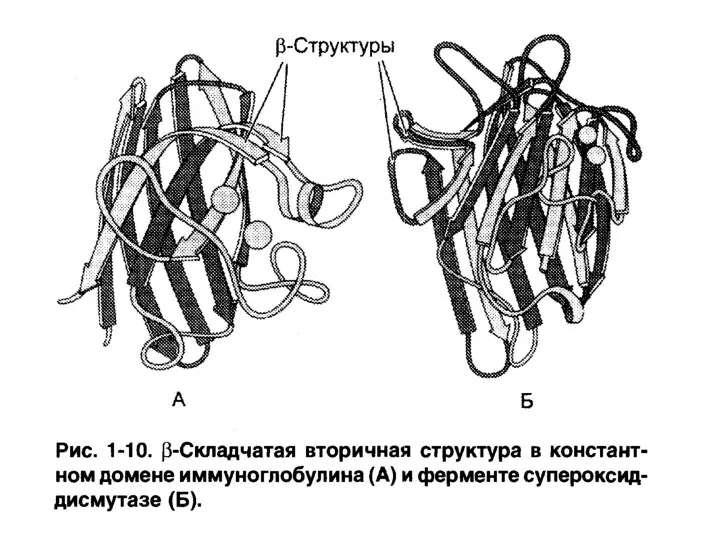
- 74. β-структура (β-складчатый слой) Образуется между несколькими полипептидными цепями или в пределах одной полипептидной цепи, делающей изгиб.
- 75. Антипараллельный β-складчатый слой
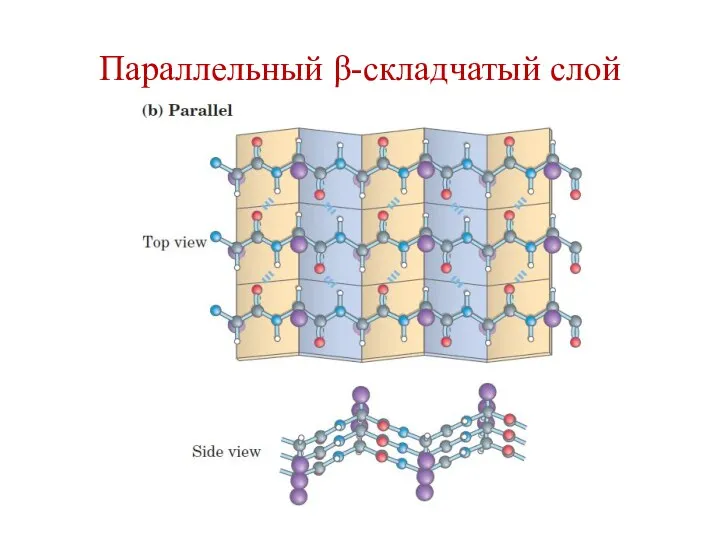
- 76. Параллельный β-складчатый слой
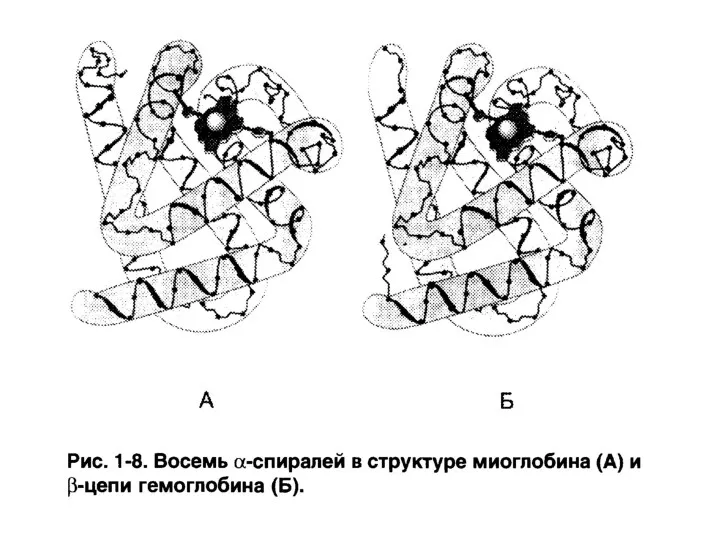
- 77. Классификация белков по содержанию разных типов вторичных структур Состоящие только из α-спиралей (примеры – миоглобин, гемоглобин).
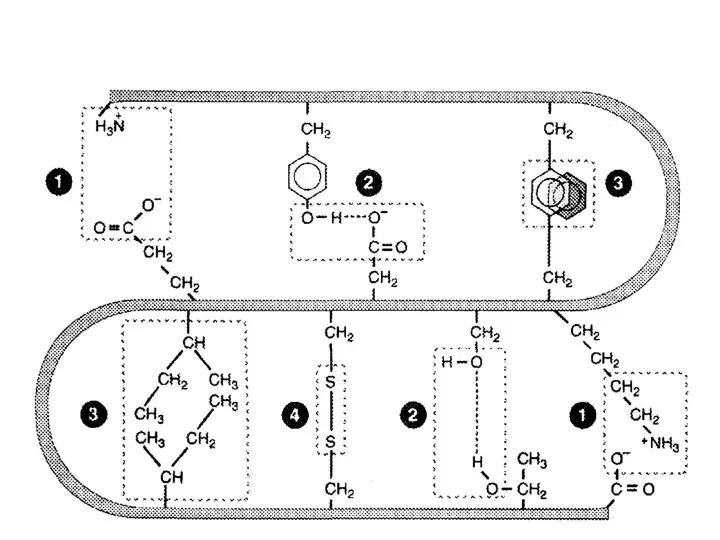
- 81. Третичная структура белка Пространственная структура (укладка полипептидной цепи в определенную конформацию). Стабилизируется за счет связей между
- 82. Связи, участвующие в формировании третичной структуры белка Ковалентные связи: Дисульфидные; Эфирные; Псевдопептидные. Нековалентные связи: Ионные; Водородные;
- 84. Третичная структура функционально активная конформация, «нативная структура»!!!
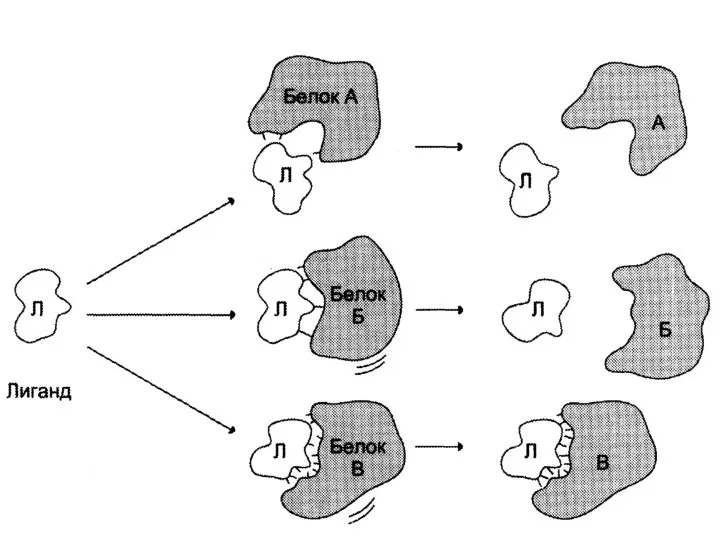
- 85. Конформационная лабильность белков – склонность к небольшим изменениям конформации за счет разрыва одних и образования других
- 86. Функционирование белков осуществляется за счет связывания белка с лигандом. Высокая специфичность связывания белка с лигандом обеспечивается
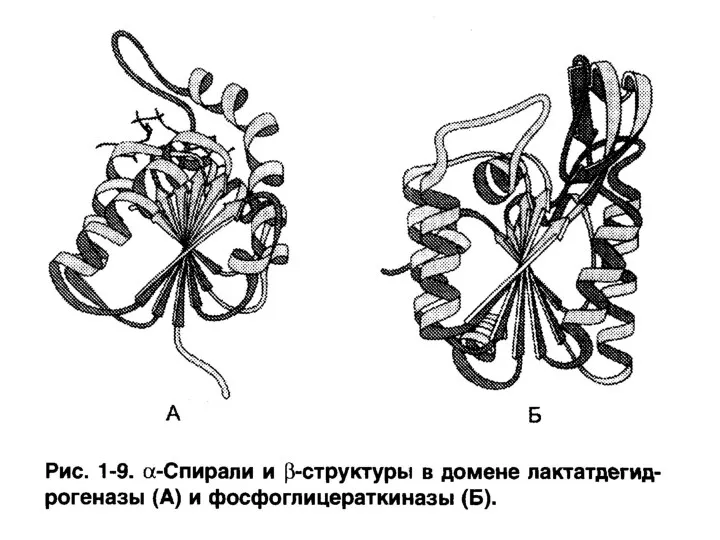
- 88. Доменная структура белков Домен – участок полипептидной цепи, который в процессе формирования пространственной структуры приобрел независимо
- 89. Четвертичная структура белков характерна для белков, состоящих их 2-х или более полипептидных цепей, каждая из которых
- 90. Четвертичная структура белков протомеры могут быть одинаковые или разные; количество протомеров – от 2-х до десятков.
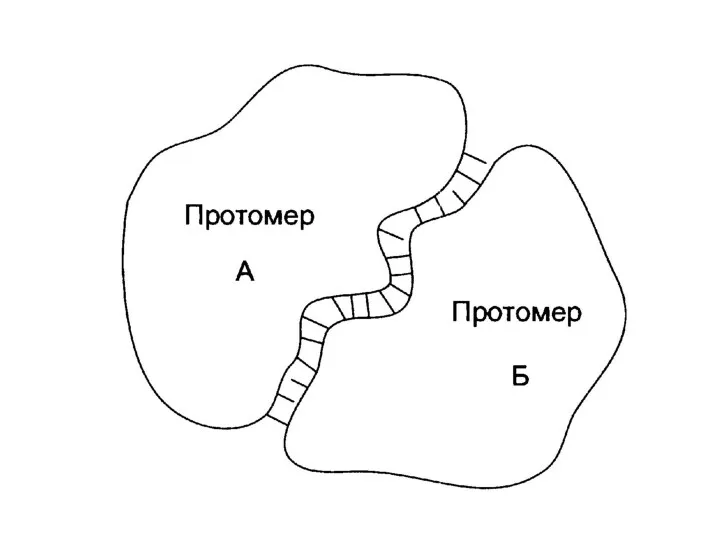
- 91. Комплементарность протомеров Сборка олигомерного белка осуществляется за счет контактных участков. Специфичность связывания контактных участков определяется их
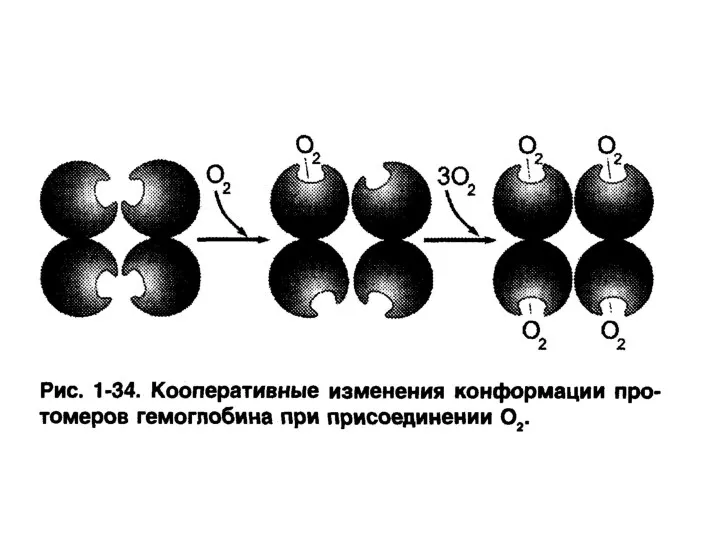
- 93. Особенности функционирования олигомерных белков – кооперативность изменения конформации протомеров. Пример – гемоглобин.
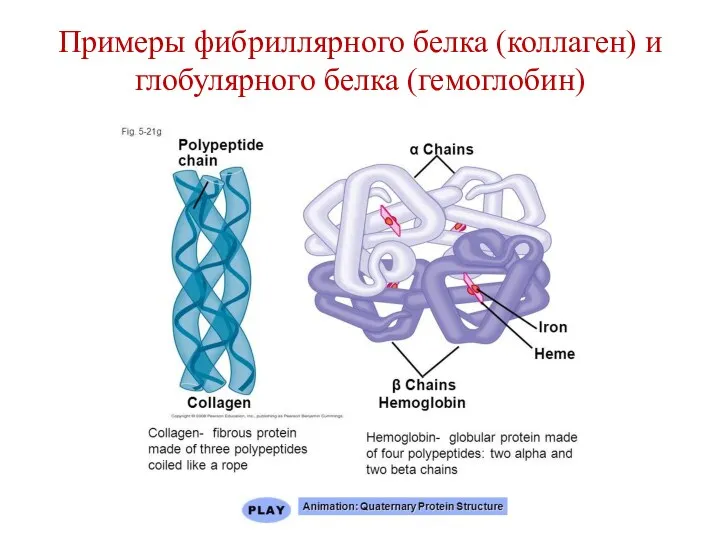
- 95. Классификация белков (по форме молекул) Глобулярные: Миоглобин; Гемоглобин. Фибриллярные: Коллаген; Кератин; Миозин; Фибриноген.
- 96. Примеры фибриллярного белка (коллаген) и глобулярного белка (гемоглобин)
- 97. Классификация белков (структурный принцип) Простые: Гистоны; Альбумины; Эластин. Сложные – холопротеины: Белковая часть (апобелок); Небелковая часть
- 98. Классы сложных белков Нуклеопротеины = белок + нуклеиновые кислоты. Примеры – хроматин, рибосомы. Связи между белком
- 99. Классы сложных белков Липопротеины = белок + липиды. Пример – клеточные мембраны. Связи между белком и
- 100. Классы сложных белков Фосфопротеины = белок + фосфорная кислота. Пример – казеин молока. Связи между белком
- 101. Классы сложных белков Хромопротеины – окрашенные белки: А) Гемопротеины = белок + гем (содержит железо) –
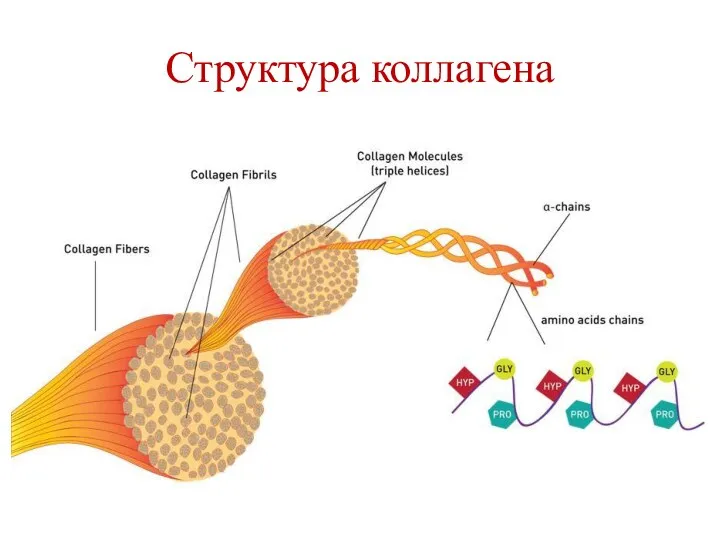
- 102. Коллаген Фибриллярный белок, синтезируемый клетками соединительной ткани. Содержится в межклеточном веществе. Составляет ¼ всех белков организма.
- 103. Первичная структура коллагена – α-коллагеновая цепь Различают 20 типов коллагеновых цепей. α-коллагеновая цепь состоит из ≈
- 104. Особенности вторичной структуры коллагена Альфа-коллагеновая спираль: левозакрученная спиральная конформация – за счет пролина, который создает изгиб
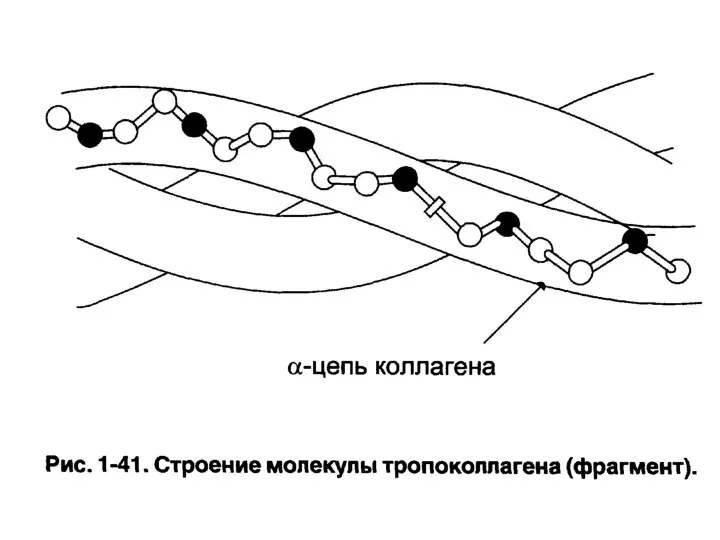
- 105. Тропоколлаген Трехцепочечная правозакрученная суперспиральная молекула. Является структурной единицей коллагена. Стабилизируется тропоколлаген водородными связями между атомами пептидной
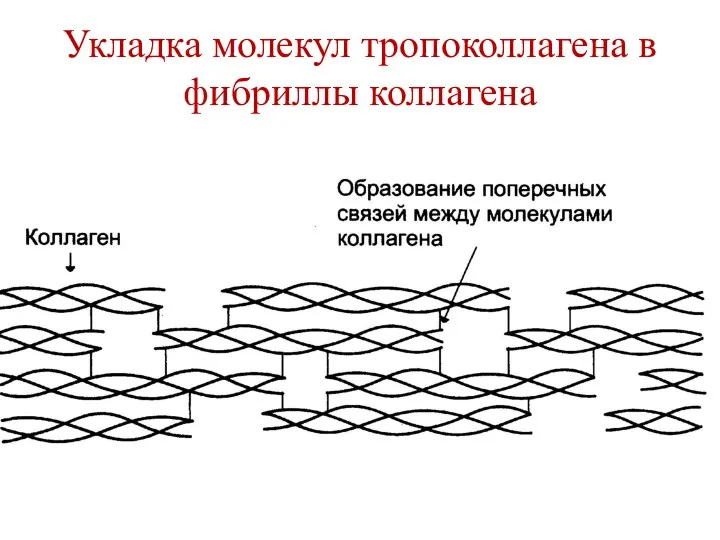
- 107. Фибриллы коллагена Молекулы тропоколлагена объединяются в фибриллы за счет взаимодействия комплементарных участков. Нити коллагена сдвинуты по
- 108. Укладка молекул тропоколлагена в фибриллы коллагена
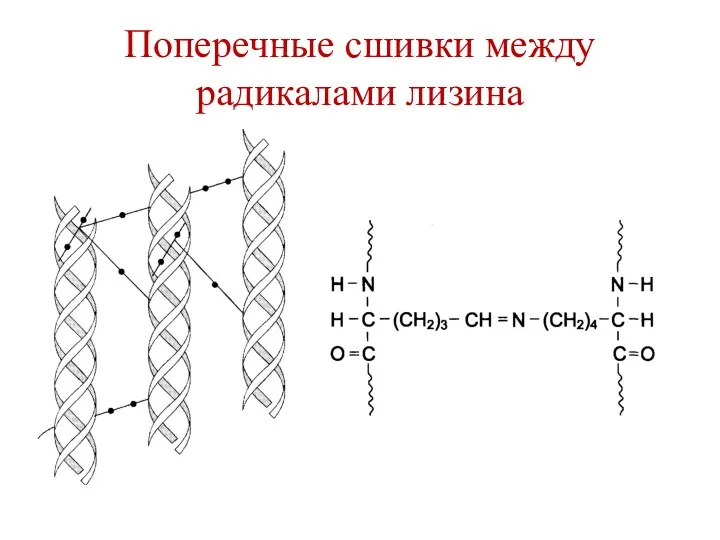
- 109. Поперечные сшивки между радикалами лизина
- 110. Структура коллагена
- 111. Эластин Белок межклеточного вещества соединительной ткани. Входит в состав соединительной ткани – кожа, легкие, стенки сосудов,
- 112. Эластин Полипептидная цепь эластина содержит около 800 остатков аминокислот. Содержит много глицина, аланина, валина, сравнительно много
- 113. Эластин Наличие большого количества гидрофобных радикалов препятствует образованию стабильной глобулы. Цепи эластина не формируют регулярные вторичную
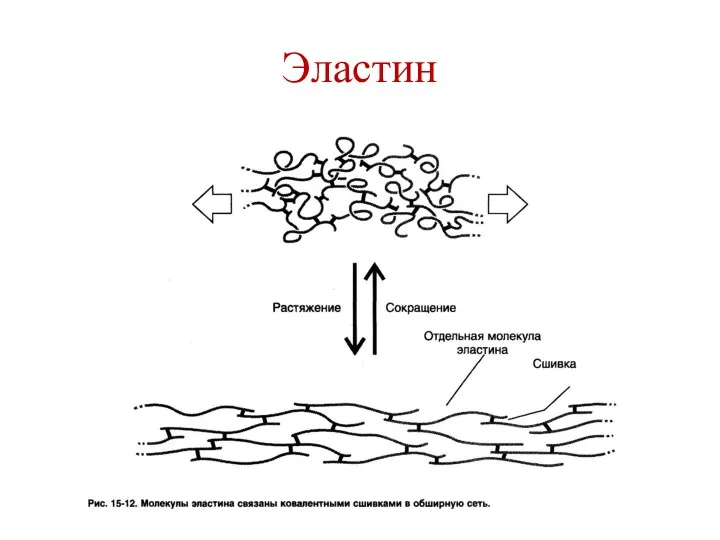
- 114. Эластин В межклеточном матриксе молекулы эластина образуют волокна, в которых пептидные цепи связаны между собой поперечными
- 115. Эластин
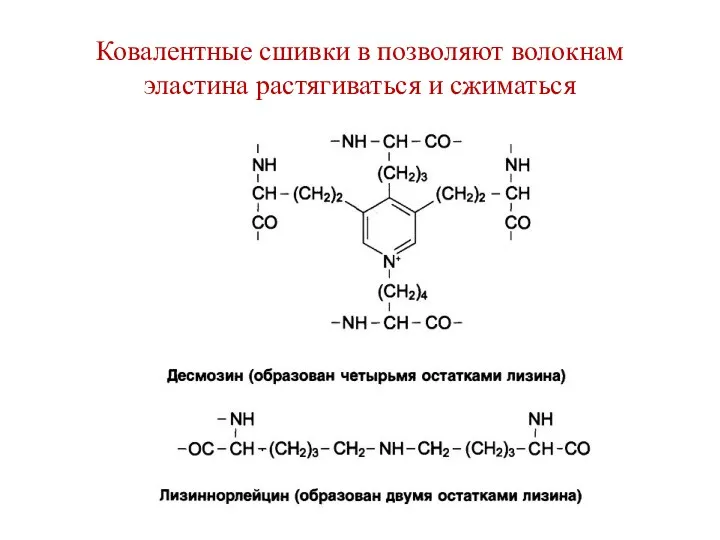
- 116. Ковалентные сшивки в позволяют волокнам эластина растягиваться и сжиматься
- 117. Кальций-связывающие белки Кальмодулин; Кальций-переносящий белок энтероцитов (кальбиндин); Коллаген; Факторы свертывания крови (II, VII, IX, X); Са2+-АТФ-аза.
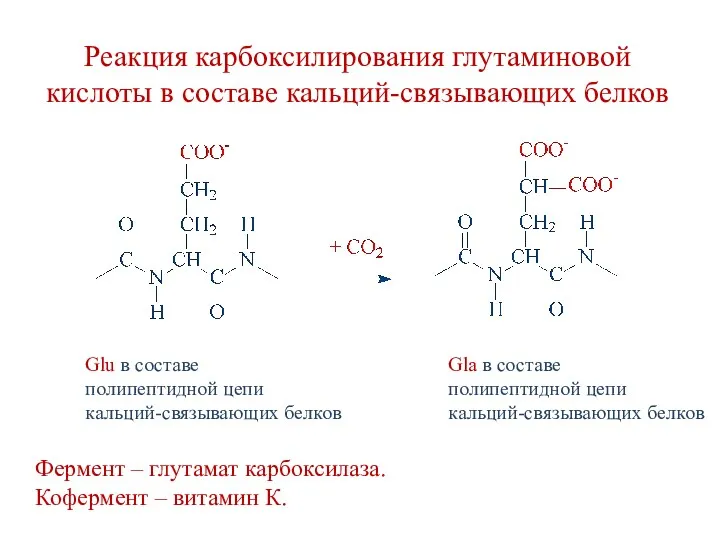
- 118. Структурные особенности кальций-связывающих белков Содержат γ-карбоксиглутаминовую кислоту (Gla). γ-карбоксиглутаминовая кислота образуется из глутаминовой кислоты в ходе
- 119. Реакция карбоксилирования глутаминовой кислоты в составе кальций-связывающих белков Фермент – глутамат карбоксилаза. Кофермент – витамин К.
- 120. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЛКОВ. МЕТОДЫ ОЧИСТКИ И РАЗДЕЛЕНИЯ БЕЛКОВ
- 121. Молекулярная масса белков Белки – высокомолекулярные соединения (молекулярная масса – 6000-1000000 Д). Методы определения молекулярной массы
- 122. Электро-химические свойства белков Обусловлены присутствием в составе белков кислых (Glu, Asp) и основных аминокислот (Lys, Arg,
- 123. Электро-химическая классификация белков Нейтральные. Кислые (преобладают Glu, Asp). Основные (преобладают Lys, Arg, His).
- 124. Электро-химические свойства белков Степень ионизации функциональных групп радикалов кислых и основных аминокислот зависит от рН среды.
- 125. Электро-химические свойства белков Значение рН, при котором белок приобретает нулевой заряд, называется изоэлектрической точкой и обозначается
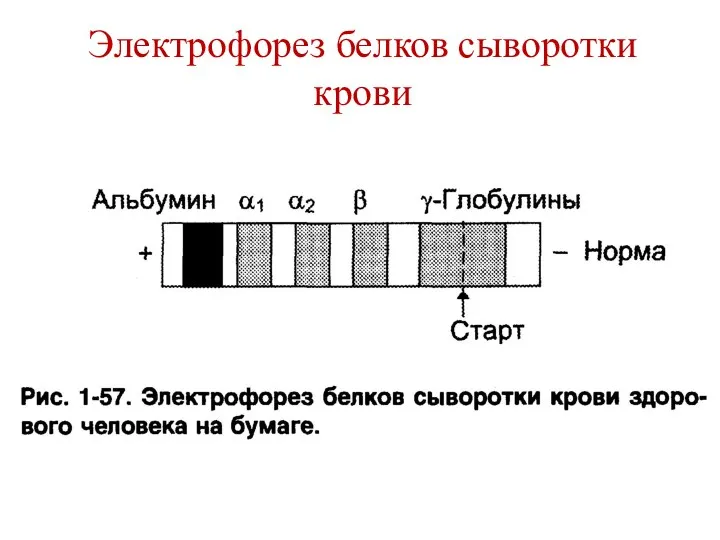
- 126. Электро-химические свойства белков Лежат в основе электрофореза. Электрофорез – движение заряженных частиц в электрическом поле. В
- 127. Электрофорез белков сыворотки крови
- 128. Растворимость белков Зависит от: Содержания полярных и неполярных групп; Заряда белка; Массы белка; Формы белка.
- 129. Факторы, влияющие на растворимость белков Присутствие нейтральных солей – (NH4)2SO4, Na2 SO4, NaCl, MgCl2. В низких
- 130. Факторы, стабилизирующие белковые растворы Заряд белка – одноименно заряженные молекулы белка отталкиваются друг от друга. Гидратная
- 131. Высаливание белков Метод очистки белков, основанный на различиях в их растворимости при разной концентрации соли в
- 132. Свойства коллоидных белковых растворов Оптические свойства. При боковом освещении белкового раствора образуется светящийся конус – эффект
- 133. Свойства коллоидных белковых растворов Малая скорость диффузии. Диффузия – самопроизвольное движение молекул растворенных веществ. Белки обладают
- 134. Свойства коллоидных белковых растворов Осмотические свойства. Белки являются высокомолекулярными веществами, потому не проходят через полупроницаемые мембраны.
- 135. Свойства коллоидных белковых растворов Неспособность белков диффундировать через мембраны вызывает явление осмоса, т.е. перемещение воды через
- 136. Свойства коллоидных белковых растворов То давление, которое нужно приложить, чтобы остановить ток воды, называется осмотическим давлением
- 137. Свойства коллоидных белковых растворов Высокая вязкость Обусловлена силами сцепления между молекулами белка и зависит от формы
- 138. Свойства коллоидных белковых растворов Способность к образованию гелей Взаимодействие макромолекул белка приводит к образованию структурных сеток,
- 139. Денатурация белков Нарушение нативной структуры белка. При денатурации происходит разрыв связей, стабилизирующих четвертичную, третичную и вторичную
- 140. Факторы, вызывающие денатурацию белков Высокая температура; Органические вещества (этанол, фенол, мочевина); Кислоты и щелочи; Соли тяжелых
- 141. Применение денатурирующих агентов в медицинской практике Стерилизация медицинских инструментов и материала (высокая температура в автоклавах). Антисептики
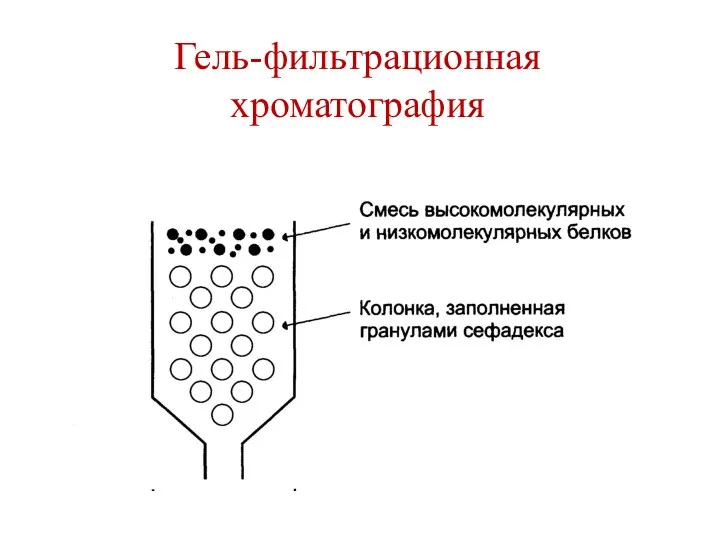
- 142. Методы разделения белков Высаливание. Гель-фильтрационная хроматография (метод молекулярных сит). Ионообменная хроматография. Аффинная хроматография. Ультрацентрифугирование.
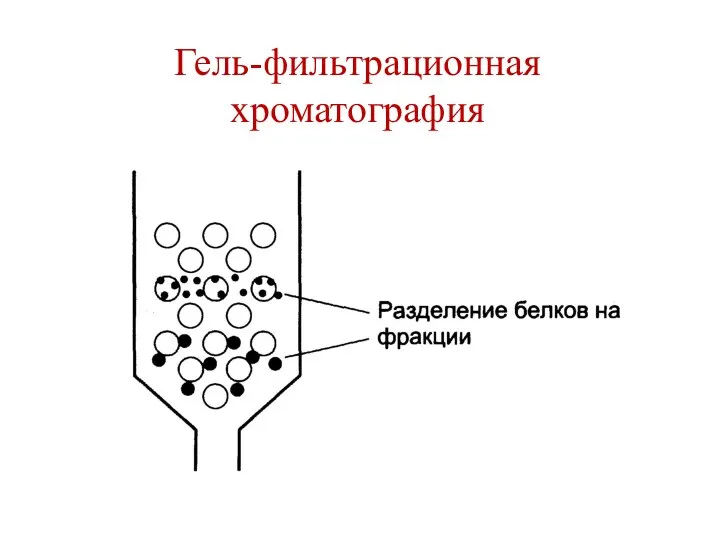
- 143. Гель-фильтрационная хроматография
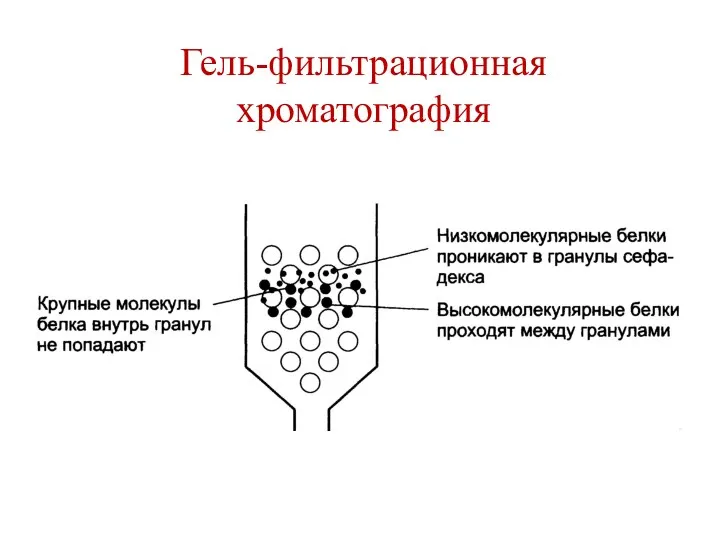
- 144. Гель-фильтрационная хроматография
- 145. Гель-фильтрационная хроматография
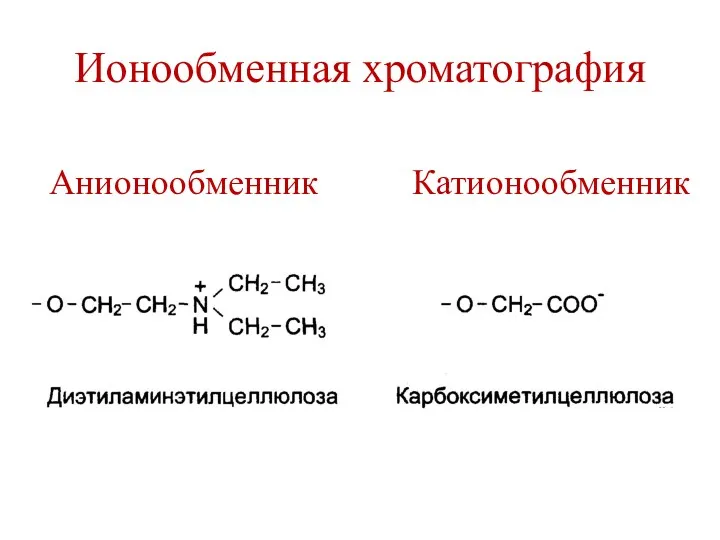
- 146. Ионообменная хроматография Анионообменник Катионообменник
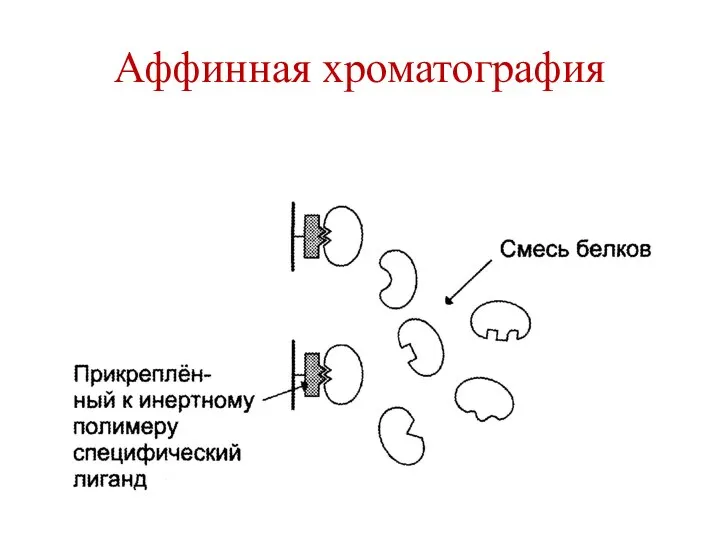
- 147. Аффинная хроматография
- 149. Скачать презентацию







































































































 Железо. Fe (лат. Феррум)
Железо. Fe (лат. Феррум) Узагальнення й систематизація знань з теми Початкові хімічні поняття
Узагальнення й систематизація знань з теми Початкові хімічні поняття Аминокислоты. Пептиды. Хроматографические методы исследования
Аминокислоты. Пептиды. Хроматографические методы исследования Химическая связь
Химическая связь Розв'язування задач за рівнянням хімічних реакцій
Розв'язування задач за рівнянням хімічних реакцій NaHSO4. Гидросульфат натрия
NaHSO4. Гидросульфат натрия Молекулярно-массовые характеристики высокомолекулярных соединений
Молекулярно-массовые характеристики высокомолекулярных соединений Общие проблемы определения низких концентраций
Общие проблемы определения низких концентраций Ионные уравнения
Ионные уравнения Реакции ионного обмена
Реакции ионного обмена Установка производства олефинов для синтеза линейных алкилбензолов
Установка производства олефинов для синтеза линейных алкилбензолов Практикум по органической и биоорганической химии
Практикум по органической и биоорганической химии Строение вещества. Химические элементы
Строение вещества. Химические элементы Применение солей
Применение солей Обзор электродных процессов
Обзор электродных процессов Спроби класифікації хімічних елементів
Спроби класифікації хімічних елементів Металловедение. Классификация металлов
Металловедение. Классификация металлов Физико-химические методы в анализе ЛВ. Метод ионометрии в анализе ЛВ. Определение спирта в фармацевтических препаратах
Физико-химические методы в анализе ЛВ. Метод ионометрии в анализе ЛВ. Определение спирта в фармацевтических препаратах Окислительновосстановительное титрование
Окислительновосстановительное титрование Активационный анализ
Активационный анализ Твердотільний ямр
Твердотільний ямр Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение
Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение Наноматериалы. Свойства наноматериалов. Особенности свойств
Наноматериалы. Свойства наноматериалов. Особенности свойств Карбоновые кислоты
Карбоновые кислоты Значение периодического закона и периодической системы Д.И. Менделеева
Значение периодического закона и периодической системы Д.И. Менделеева Способы получения металлов
Способы получения металлов Химическая связь
Химическая связь Закон сохранения массы вещества. Химические уравнения
Закон сохранения массы вещества. Химические уравнения