Содержание
- 2. Задание: Что здесь написано? NaCl, K2O, CuO, SO2. CH4 SnF2
- 3. . Рассчитайте относительную молекулярную массу данных веществ: CuO, SO2, KClO3 Справочные данные: Аr (Cu) = 64
- 4. Что общего в составе молекул? Чем они отличаются друг от друга? Задание: сравните качественный и количественный
- 5. Вывод: У атомов разная способность удерживать определённое количество других атомов в соединениях. Это называется валентностью. Слово
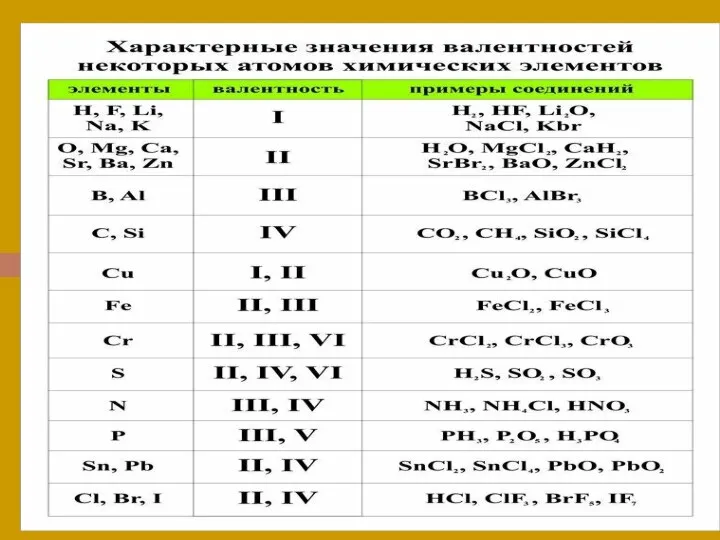
- 6. Тема: Валентность Валентность – это способность химического элемента образовывать определенное количество химических связей с другими элементами.
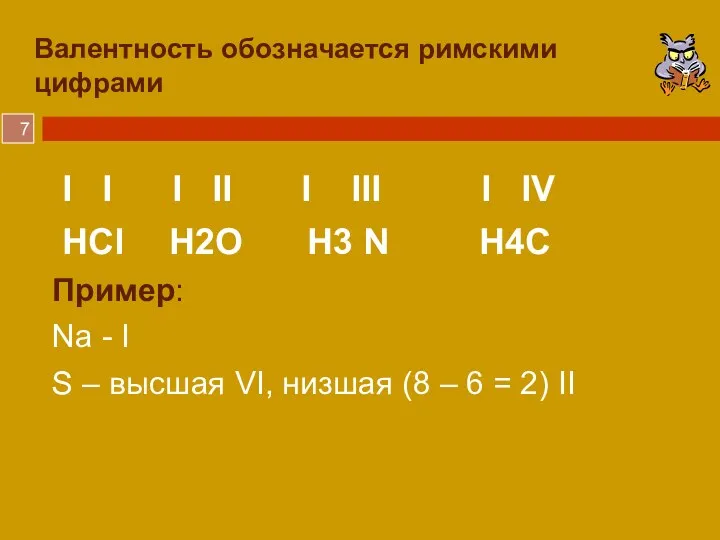
- 7. Валентность обозначается римскими цифрами I I I II I III I IV HCl H2O H3 N
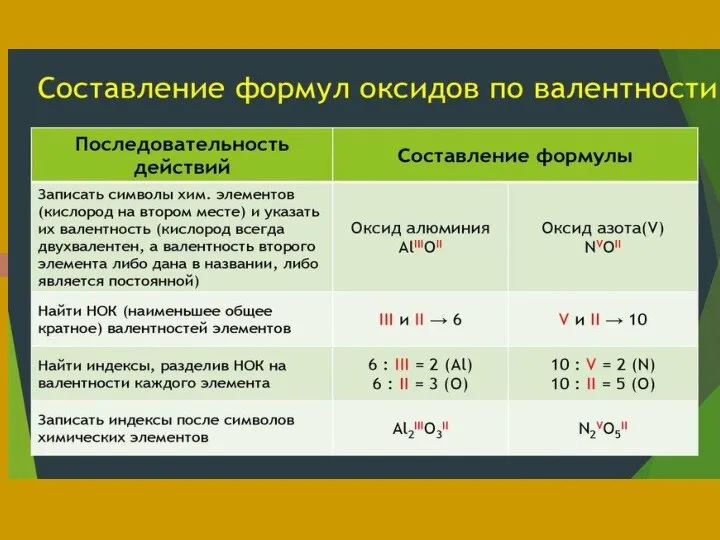
- 8. Составление химических формул по валентности научимся составлять химические формулы
- 9. 1. Запиши рядом знаки химических элементов, которые входят в состав вещества. Пример: Составить химическую формулу оксида
- 10. 2. Над знаками химических элементов поставь их валентность. Пример: Составить химическую формулу оксида бора. B O
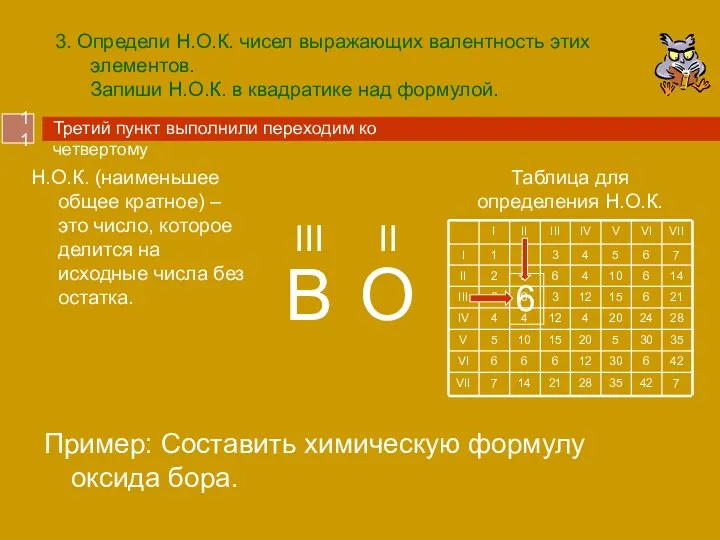
- 11. 3. Определи Н.О.К. чисел выражающих валентность этих элементов. Запиши Н.О.К. в квадратике над формулой. Пример: Составить
- 12. 4. Раздели Н.О.К. на валентность каждого элемента. Запиши полученный индекс. Пример: Составить химическую формулу оксида бора.
- 13. Тема: Валентность. I. Валентность – это способность химического элемента образовывать определенное количество химических связей. Нахождение валентности
- 17. Рассчитайте относительную молекулярную массу данных веществ: NaCl, K2O. Справочные данные: Аr (Na) = 23 Аr (Cl)
- 18. Рассчитайте относительную молекулярную массу данных веществ: Cu2O, SO3, СuSO4 Справочные данные: Аr (Cu) = 64 Аr
- 19. Рассчитайте относительную молекулярную массу данных веществ: CH4, NO, N2O5 Справочные данные: Аr (С) = 12 Аr
- 20. Эффективность зубных паст в профилактике кариеса можно сравнить по содержанию в них активного фтора, способного взаимодействовать
- 21. определить валентность элементов в веществах: SiH4, CrO3, H2S, CO2, CO, SO3, SO2, Fe2O3, FeO, HCl, HBr,
- 22. Задание 1.Определите валентность атомов химических элементов по формулам соединений: NH3, Au2O3, SiH4, CuO. Оценка «3» 2.Из
- 24. Скачать презентацию
















 Газовые законы для идеальных и реальных газов. Лекция 1
Газовые законы для идеальных и реальных газов. Лекция 1 Фотоэлектрические и информационные свойства фоточувствительных карбазолилсодержащих олигомерных пленочных композитов
Фотоэлектрические и информационные свойства фоточувствительных карбазолилсодержащих олигомерных пленочных композитов Ископаемые углеводороды
Ископаемые углеводороды Методы прямого секвенирования белков (пептидов)
Методы прямого секвенирования белков (пептидов) Неметаллы. Обобщающий урок. 9 класс
Неметаллы. Обобщающий урок. 9 класс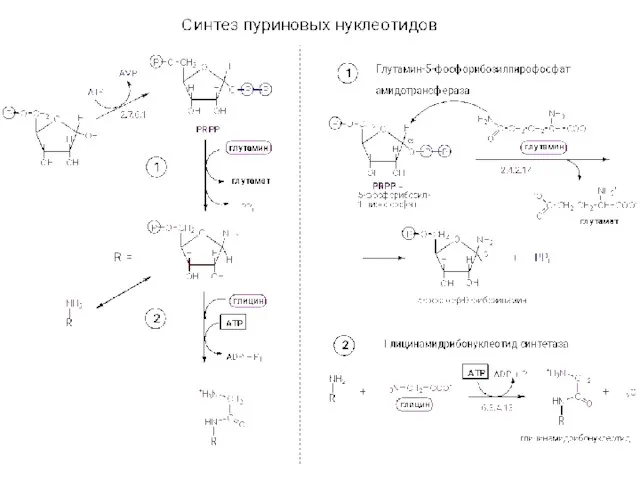 Синтез нуклеотидов
Синтез нуклеотидов Методы пробоотбора воздуха. Лекция 2
Методы пробоотбора воздуха. Лекция 2 Химическая стойкость тугоплавких металлов в различных реагентах
Химическая стойкость тугоплавких металлов в различных реагентах Соединения углерода
Соединения углерода The chemistri of life and the micro universe
The chemistri of life and the micro universe Определение химического элемента на основании расчетов по химическим реакциям
Определение химического элемента на основании расчетов по химическим реакциям Классификация органических соединений. Урок химии в 10 классе
Классификация органических соединений. Урок химии в 10 классе Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма)
Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма) Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Миграция химических элементов (геохимическая миграция)
Миграция химических элементов (геохимическая миграция) Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей
Вычисление массы растворённого вещества, содержащегося в определённой массе раствора с известной массовой долей Кислородсодержащие соединения. Ароматические соединения
Кислородсодержащие соединения. Ароматические соединения Серная кислота
Серная кислота Трансмиссионные масла
Трансмиссионные масла Хімічні властивості кислот
Хімічні властивості кислот Неметаллы: атомы и простые вещества. Воздух. Кислород. Озон
Неметаллы: атомы и простые вещества. Воздух. Кислород. Озон Комплексные соединения
Комплексные соединения Кислоты в свете теории электролитической диссоциации (ТЭД), 8 класс
Кислоты в свете теории электролитической диссоциации (ТЭД), 8 класс Аналитическая химия. Предмет и задачи
Аналитическая химия. Предмет и задачи Теория электрической диссоциации
Теория электрической диссоциации NaOH. Гидроксид натрия
NaOH. Гидроксид натрия Углеводы Cn(H2O)m
Углеводы Cn(H2O)m Ансамбль пор в реальном твердом теле
Ансамбль пор в реальном твердом теле