Содержание
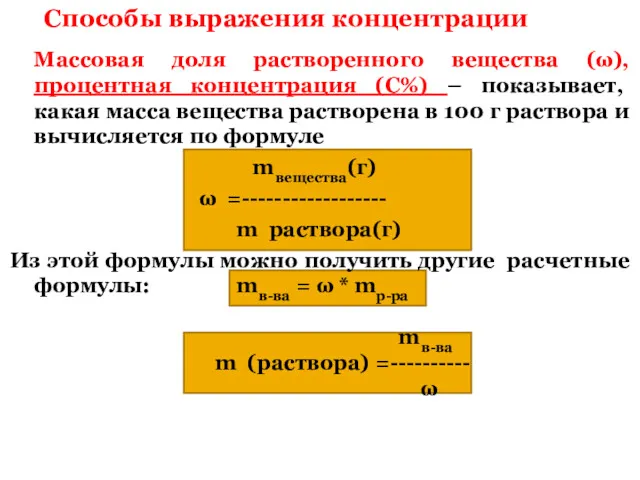
- 2. Массовая доля растворенного вещества (ω), процентная концентрация (С%) – показывает, какая масса вещества растворена в 100
- 3. Массу раствора можно выразить и через объём раствора и его плотность mв-ва = V * ρ
- 4. Вычислить массу серной кислоты содержащейся в 230мл серной кислоты, если массовая доля H2S04 в этом растворе
- 5. 1)Вычислите массу(г) хлорида калия, который содержится в 750мл. 10% -ного раствора с плотностью 1,063 г/мл. (
- 6. Кристаллогидраты Кристаллогидраты – это тоже растворы, где можно рассчитать массовую долю растворенного вещества. ZnSО4* 7Н2О –
- 7. Решение задач на кристаллогидраты Задача.В какой массе воды нужно растворить 125 г медного купороса СuSО4* 5Н2О,
- 9. Скачать презентацию





 Углекислый газ СО2
Углекислый газ СО2 Методы хроматографии. Ионообменная хроматография
Методы хроматографии. Ионообменная хроматография Спирти
Спирти Енергетичний стан поверхні. Сорбційні явища. Мезопористі матеріали
Енергетичний стан поверхні. Сорбційні явища. Мезопористі матеріали Основи, їх склад, назви, класифікація
Основи, їх склад, назви, класифікація Зависят ли свойства предельных одноатомных спиртов от их химического строения?
Зависят ли свойства предельных одноатомных спиртов от их химического строения? Фосфор
Фосфор Кислород O2
Кислород O2 Жесткость воды
Жесткость воды Азотная кислота
Азотная кислота Всероссийская олимпиада школьников по химии (региональный этап). Разбор заданий, 9 класс
Всероссийская олимпиада школьников по химии (региональный этап). Разбор заданий, 9 класс Непредельные углеводороды: этилен
Непредельные углеводороды: этилен Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду
Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду Гниение. Брожение
Гниение. Брожение Теория кристаллического поля
Теория кристаллического поля Вещества и их свойства
Вещества и их свойства Азотные удобрения
Азотные удобрения Непредельные углеводороды
Непредельные углеводороды Теория электрической диссоциации
Теория электрической диссоциации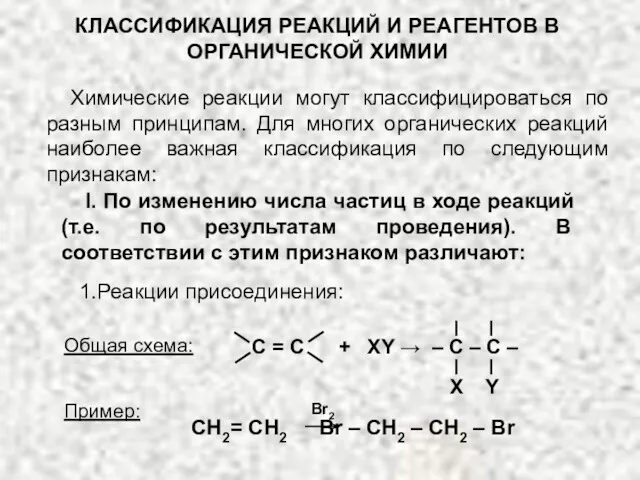 Классификация реакций и реагентов органической химии
Классификация реакций и реагентов органической химии Бор шикізатын қышқылдық ыдырату
Бор шикізатын қышқылдық ыдырату Органолептические и визуальные методы идентификация полимера
Органолептические и визуальные методы идентификация полимера Аминокислоты. Физические свойства
Аминокислоты. Физические свойства Введение в химическую технологию топлив и углеродных материалов
Введение в химическую технологию топлив и углеродных материалов Основания. Неорганические соединения
Основания. Неорганические соединения Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов
Положение в периодической системе Менделеева водорода, лантаноидов, актиноидов и искусственно полученных элементов Формы минералов и их агрегатов
Формы минералов и их агрегатов Основи. Властивості, застосування гідроксидів Натрію і Калію
Основи. Властивості, застосування гідроксидів Натрію і Калію