Содержание
- 2. План лекции 1. Фармацевтическая биоэтика а) Талидомид б) Биоэтика как наука 2. Ключевые вопросы биоэтики 3.
- 3. Актуальность темы Успешная работа по продвижении лекарственных препаратов на рынок много в чем зависит от профессионализма
- 4. Актуальность темы Такая подготовленность должна включать инструктаж про соответственные этичные аспекты поведения , учитывая критерии ВООЗ
- 5. Фармацевтическая биоэтика Ускорение научно-технического прогресса во второй половине XX в. еще более ярко высветило проблемы морально-нравственных
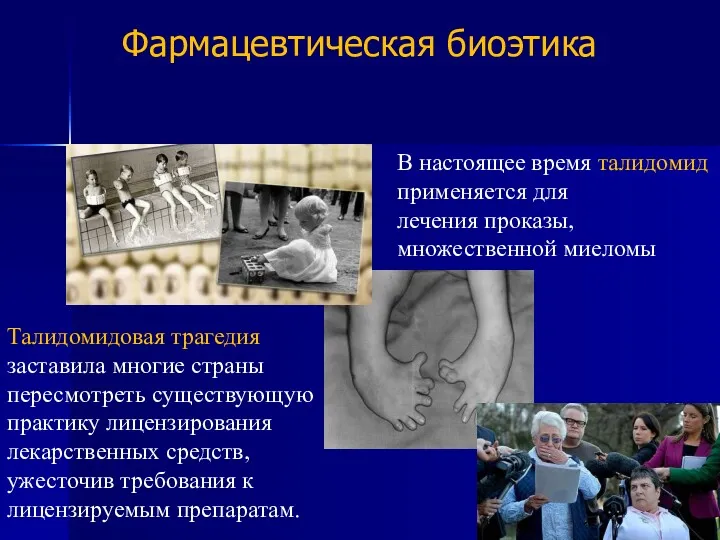
- 6. Талидомид — седативное снотворное лекарственное средство, обладающее тератогенностью. В период с 1956 по 1962 годы в
- 7. Талидомидовая трагедия заставила многие страны пересмотреть существующую практику лицензирования лекарственных средств, ужесточив требования к лицензируемым препаратам.
- 8. Зимняя олимпиада в Солт-Лейк Сити в 2002 г. преподнесла немало новых случаев использования лекарств с неблаговидными
- 9. Фармацевтическая биоэтика В ответ на сложившуюся ситуацию появилось новое направление в науке - биоэтика. Термин «биоэтика»
- 10. Фармацевтическая биоэтика Биоэ́тика (от др.-греч. βιός — жизнь и ἠθική —этика, наука о нравственности) — наука,
- 11. Фармацевтическая биоэтика Первый круг проблем биомедицинской этики связан с необходимостью проследить, как могут и должны проявлять
- 12. Фармацевтическая биоэтика Во-первых, это проблема активного включения в лечебную практику в качестве руководства к действию свода
- 13. Фармацевтическая биоэтика Во-вторых, это проблема установления однозначного трактования сущности и признаков Жизни и Смерти человека как
- 14. Фармацевтическая биоэтика Второй круг проблем биомедицинской этики связан со спецификой, развитием и современными достижениями медицины, которые
- 15. Фармацевтическая биоэтика проблема эвтаназии; проблемы реанимирования – принятия решения о его необходимости и длительности, проблемы трансплантации
- 16. Ключевые вопросы биоэтики моральные и философские проблемы аборта – ст. 50 Закона Украины «Основы законодательства Украины
- 17. Ключевые вопросы биоэтики Технология суррогатного материнства запрещена в некоторых странах (Германия), но разрешена на Украине и
- 18. Ключевые вопросы биоэтики В некоторых юрисдикциях разрешено лишь некоммерческое суррогатное материнство -Великобритания (допускается лишь оплата текущих
- 19. Ключевые вопросы биоэтики Правовое урегулирование отношений суррогатного материнства совершается положениями Семейного кодекса Украины, Приказом Министерства юстиции
- 20. Ключевые вопросы биоэтики Пионером в области легализации добровольной смерти стали Нидерланды. В 1984 году Верховный суд
- 21. Фармацевтическая биоэтика В 90х годах XX века началось становление фармацевтичес-кой биоэтики как одного из направлений биоэтики,
- 22. Фармацевтическая биоэтика Фармацевтическая биоэтика изучает: * моральные, правовые, социальные, экологические и юридические проблемы, возникающие при создании,
- 23. Фармацевтическая биоэтика * формы оказания фармацевтических научно-консультативных услуг, с целью защиты здоровья населения и отдельных лиц,
- 24. Фармацевтическая биоэтика в профессиональной деятельности в сфере обращения аптечных товаров, в первую очередь лекарств. Фармацевтическая биоэтика
- 25. Фармацевтическая биоэтика В 1996 году была проведена первая международная конференция "Фармацевтическая биоэтика", в этот год, можно
- 26. Биоэтические аспекты клинических испытаний лекарственных средств В Украине за последние пять лет проведено более 1000 клинических
- 27. Биоэтические аспекты клинических испытаний лекарственных средств Задачи, стоящие перед фармацевтической биоэтикой в Украине 1. Решение вопроса
- 28. Биоэтические аспекты клинических испытаний лекарственных средств Для оценки их качества в нашей стране до настоящего времени
- 29. Биоэтические аспекты клинических испытаний лекарственных средств Учитывая, что частота возникновения побочных эффектов многих лекарственных препаратов составляет
- 30. Биоэтические аспекты клинических испытаний лекарственных средств Возникает вопрос: этично ли результаты ограниченных клинических испытаний считать тестом,
- 31. Биоэтические аспекты клинических испытаний лекарственных средств 2. Решение этических проблем при проведении исследований биоэквивалентности
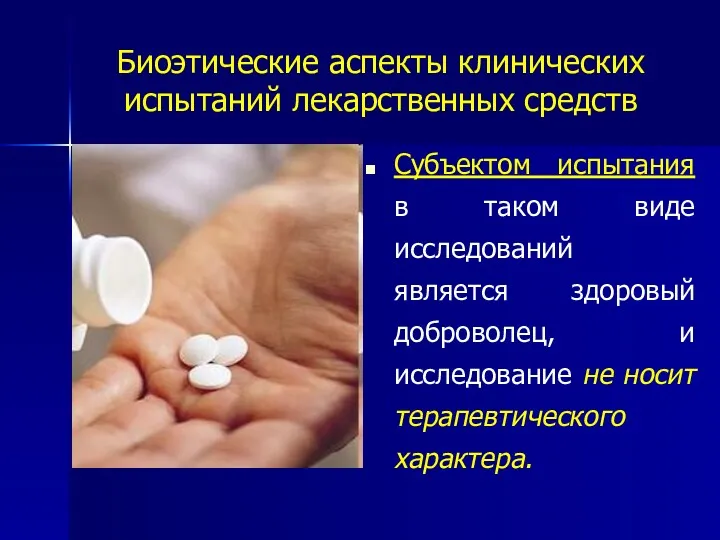
- 32. Биоэтические аспекты клинических испытаний лекарственных средств Субъектом испытания в таком виде исследований является здоровый доброволец, и
- 33. Биоэтические аспекты клинических испытаний лекарственных средств Особое внимание при рассмотрении материалов клинических испытаний этические комитеты должны
- 34. Биоэтические аспекты клинических испытаний лекарственных средств В соответствии с требованиями GCP суммы выплат должны быть пропорциональны
- 35. Биоэтические аспекты клинических испытаний лекарственных средств Если для привлечения в исследование здоровых добровольцев используются объявления, они
- 36. Биоэтические аспекты клинических испытаний лекарственных средств Этические комитеты (ЭК) — это независимые организации, в состав которых
- 37. Биоэтические аспекты клинических испытаний лекарственных средств Базовым документом для создания и функционирования национальных этических комитетов (НЭК)
- 38. Биоэтические аспекты клинических испытаний лекарственных средств Основные направления работы ЭК в соответствии с GCP : *
- 39. Биоэтические аспекты клинических испытаний лекарственных средств ХЕЛЬСИНСКАЯ ДЕКЛАРАЦИЯ ВСЕМИРНОЙ АССОЦИАЦИИ ВРАЧЕЙ Рекомендации для врачей по проведению
- 40. Биоэтические аспекты клинических испытаний лекарственных средств Следует подчеркнуть, что изложенные в Хельсинской декларации принципы являются только
- 41. Биоэтические аспекты клинических испытаний лекарственных средств В 1966 г. принята Международная Конвенция гражданских и политических прав
- 42. НАЦИОНАЛЬНОЕ ЗАКОНОДАТЕЛЬСТВО О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ В украинском законодательстве правовые и этические вопросы при проведении клинических испытаний
- 43. Биоэтические аспекты клинических испытаний лекарственных средств в статье 7 закона Украины «О лекарственных средствах», в частности,
- 44. Биоэтические аспекты клинических испытаний лекарственных средств Статья 8 закона Украины «О лекарственных средствах» полностью посвящена защите
- 45. Биоэтические аспекты клинических испытаний лекарственных средств Заказчик клинического исследования лекарственного средства обязан составить договор о страховании
- 46. Биоэтические аспекты клинических испытаний лекарственных средств Решение о приостановке клинического испытания лекарственного средства или отдельных его
- 47. Биоэтические аспекты клинических испытаний лекарственных средств В Украине в 1995 г. при Государственном фармакологическом комитете МЗ
- 48. Биоэтические аспекты клинических испытаний лекарственных средств Для решения комплекса биомедицинских проблем ГФЦ в 2000 г. были
- 49. ТРЕБОВАНИЯ GCP К ЭК Европейский форум GCP разработал рекомендации относительно состава ЭК. Они включают требование, чтобы
- 50. ТРЕБОВАНИЯ GCP К ЭК В состав ЭК должны быть включены также юрист, парамедик и хотя бы
- 51. ТРЕБОВАНИЯ GCP К ЭК Основными задачами Комиссии по вопросам этики являются: защита прав и интересов исследуемых,
- 52. ТРЕБОВАНИЯ GCP К ЭК До начала проведения клинического испытания лекарственного средства ЭК оценивает этические и нравственно-правовые
- 53. ТРЕБОВАНИЯ GCP К ЭК пригодность исследователя(лей) для проведения предложенного клинического испытания; соответствие исследовательского центра целям и
- 54. ТРЕБОВАНИЯ GCP К ЭК Во время проведения клинического испытания лекарственного средства Комиссия осуществляет контроль по защите
- 55. ТРЕБОВАНИЯ GCP К ЭК Варианты заключений Комиссии по рассмотренным материалам клинических исследований: Одобренное мнение (в странах
- 56. ТРЕБОВАНИЯ GCP К ЭК В процессе проведения клинических испытаний исследователь информирует Комиссию в следующих случаях: При
- 57. ТРЕБОВАНИЯ GCP К ЭК В Украине в настоящее время проводится активная работа по созданию местных этических
- 58. ЭТИКА ПРОВЕДЕНИЯ КЛИНИЧЕСКИХ ИСПЫТАНИЙ С УЧАСТИЕМ ДЕТЕЙ Согласно существующей в Украине практике, клинические испытания лекарственных средств
- 59. ЭТИКА ПРОВЕДЕНИЯ КЛИНИЧЕСКИХ ИСПЫТАНИЙ С УЧАСТИЕМ ДЕТЕЙ Изучение фармакокинетики оригинальных или сравнительной фармакокинетики генерических лекарств следует
- 60. ЭТИКА ПРОВЕДЕНИЯ КЛИНИЧЕСКИХ ИСПЫТАНИЙ С УЧАСТИЕМ ДЕТЕЙ Фармакокинетика многих лекарственных препаратов изменяется в зависимости от возраста
- 61. ЭТИКА ПРОВЕДЕНИЯ КЛИНИЧЕСКИХ ИСПЫТАНИЙ С УЧАСТИЕМ ДЕТЕЙ Прежде чем приступить к исследованию с привлечением детей, рекомендуется
- 62. ЭТИКА ПРОВЕДЕНИЯ КЛИНИЧЕСКИХ ИСПЫТАНИЙ С УЧАСТИЕМ ДЕТЕЙ Не следует привлекать к клиническим исследованиям детей, содержащихся в
- 64. Скачать презентацию


























































 Ликвор. Внутричерепная гипертензия
Ликвор. Внутричерепная гипертензия Емдеу сауықтыру мекемелерінін түрлері. Аурухана ішілік инфекция
Емдеу сауықтыру мекемелерінін түрлері. Аурухана ішілік инфекция Особенности оказания первой помощи при несчастных случаях. Тема 1
Особенности оказания первой помощи при несчастных случаях. Тема 1 Гигиена и антисептика рук в медицинском учреждении
Гигиена и антисептика рук в медицинском учреждении Особенности ЛФК (лечебная физкультура)
Особенности ЛФК (лечебная физкультура) Основы нейро- и микрохирургии
Основы нейро- и микрохирургии Обзор рекомендаций по диагностике и лечению внебольничного бактериального менингита у взрослых пациентов
Обзор рекомендаций по диагностике и лечению внебольничного бактериального менингита у взрослых пациентов Системные васкулиты
Системные васкулиты Тікелей емес әсер ететін адренергиялық заттар
Тікелей емес әсер ететін адренергиялық заттар Хроническая ревматическая болезнь сердца (ХРБС)
Хроническая ревматическая болезнь сердца (ХРБС) Личная гигиена тяжелобольного пациента. Профилактика пролежней
Личная гигиена тяжелобольного пациента. Профилактика пролежней Топографическая анатомия поясничной области
Топографическая анатомия поясничной области Ветеринарная гельминтология. Общие данные о гельминтах и вызываемых ими болезнях
Ветеринарная гельминтология. Общие данные о гельминтах и вызываемых ими болезнях Физическая реабилитация детей с врожденным вывихом бедра
Физическая реабилитация детей с врожденным вывихом бедра Диареегенные эшерихии
Диареегенные эшерихии Функциональная диспепсия. Современные принципы терапии
Функциональная диспепсия. Современные принципы терапии Хроническая сердечная недостаточность
Хроническая сердечная недостаточность Pharmacology of the respiratory system
Pharmacology of the respiratory system Психические расстройства при эпилепсии
Психические расстройства при эпилепсии Гострі інвазивні та секреторні діареї. Клініко-епідеміологічні особливості, диференціальний діагноз. Лікування
Гострі інвазивні та секреторні діареї. Клініко-епідеміологічні особливості, диференціальний діагноз. Лікування Стабилизатор мембран тучных клеток и антигистаминных лекарственных средств у детей
Стабилизатор мембран тучных клеток и антигистаминных лекарственных средств у детей Консервативное лечение перфоративной язвы желудка
Консервативное лечение перфоративной язвы желудка Формирование расписания приема врачей. Организация работы регистратуры
Формирование расписания приема врачей. Организация работы регистратуры Аккредитация медицинского персонала в 2023 году
Аккредитация медицинского персонала в 2023 году Траектория реабилитации пациента с заболеваниями сердечно-сосудистой системы
Траектория реабилитации пациента с заболеваниями сердечно-сосудистой системы Дифференциальная диагностика геморрагических высыпаний при системных васкулитах сосудов мелкого и среднего калибра
Дифференциальная диагностика геморрагических высыпаний при системных васкулитах сосудов мелкого и среднего калибра Инвазиялық ауруларда ет пен ет өнімдерін малдәрігерлік-санитарлық сараптау
Инвазиялық ауруларда ет пен ет өнімдерін малдәрігерлік-санитарлық сараптау Послеродовые гнойно-септические заболевания
Послеродовые гнойно-септические заболевания