Содержание
- 2. А Л Ь Д Е Г И Д Ы - органические вещества, молекулы которых содержат карбонильную
- 3. Классификация. 1. По характеру углеводородного радикала: предельные, непредельные, ароматические. 2. По числу альдегидных групп: моно-, диальдегиды
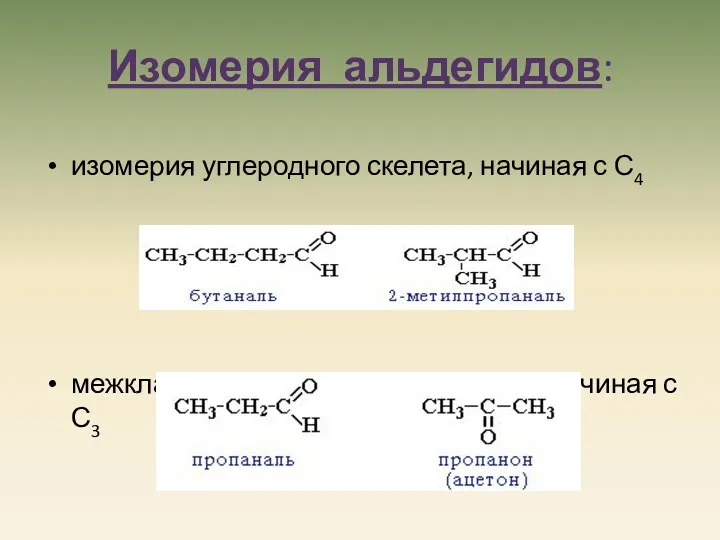
- 4. Изомерия альдегидов: изомерия углеродного скелета, начиная с С4 межклассовая изомерия с кетонами, начиная с С3
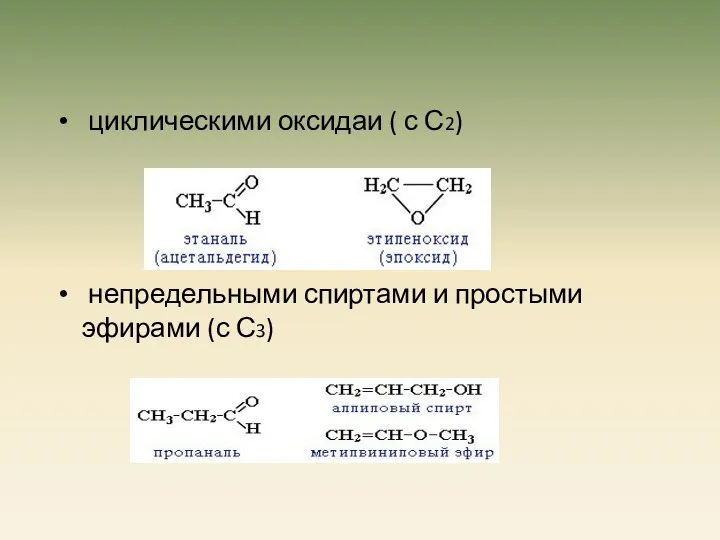
- 5. циклическими оксидаи ( с С2) непредельными спиртами и простыми эфирами (с С3)
- 6. Физические свойства. Метаналь (формальдегид) – газ, альдегиды С2-C5 – жидкости, высшие – твердые вещества. Низшие гомологи
- 7. Физически свойства некоторых альдегидов. Формальдегид – газ, с резким запахом, раздражает слизистые ткани и оказывает действие
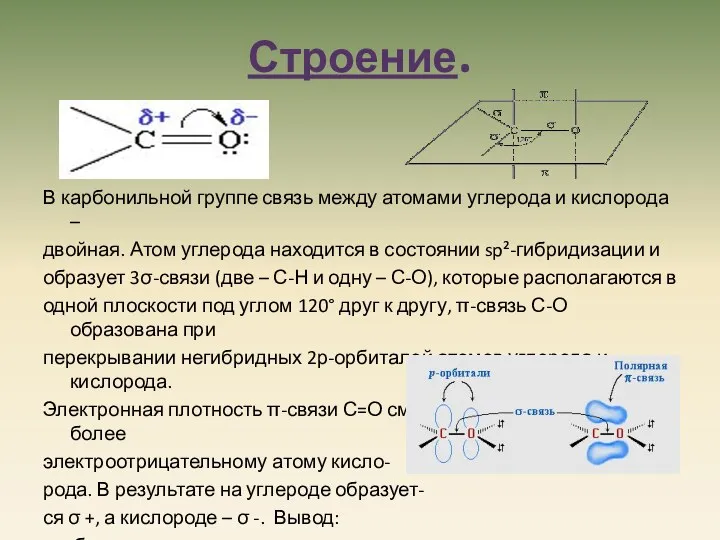
- 8. Строение. В карбонильной группе связь между атомами углерода и кислорода – двойная. Атом углерода находится в
- 9. Химические свойства. Наличие альдегидной группы в молекуле определяет характерные свойства альдегидов. Реакции присоединения. Гидрирование – реакции
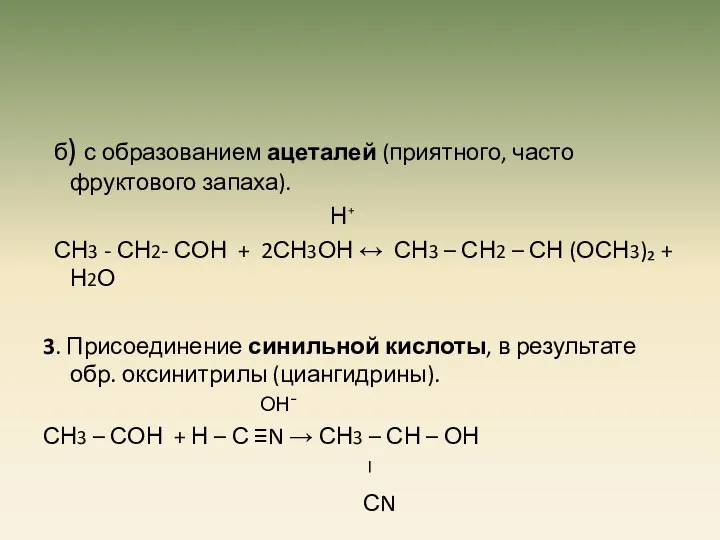
- 10. б) с образованием ацеталей (приятного, часто фруктового запаха). Н⁺ СН3 - СН2- СОН + 2СН3ОН ↔
- 11. 4. Присоединение гидросульфита натрия (это качественная реакция на карбонильную группу), в результате образ. гидросульфит натрия. СН3
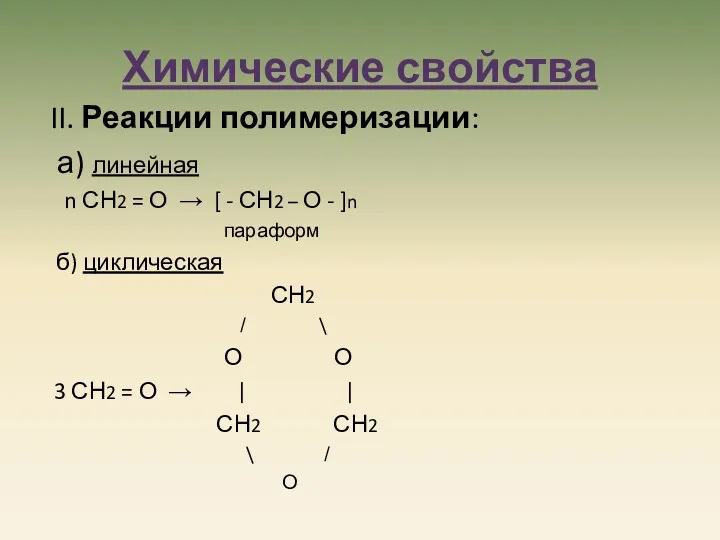
- 12. Химические свойства II. Реакции полимеризации: а) линейная n СН2 = О → [ - СН2 –
- 13. Химические свойства III. Реакции окисления: 1. аммиачным раствором оксида серебра (реакция «серебряного зеркала»). Это качественная реакция
- 14. 2. гидроксидом меди (II), в результате обр. осадок кирпично-красного цвета (качественная реакция). t° СН3 – СОН
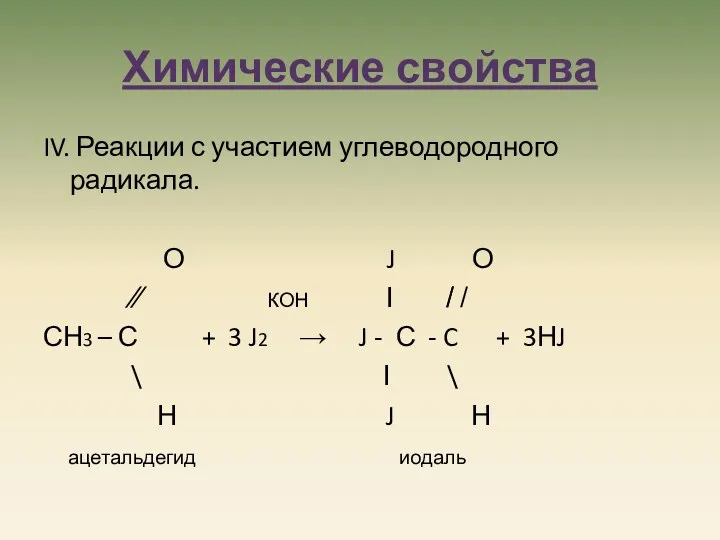
- 15. Химические свойства IV. Реакции с участием углеводородного радикала. О J О ∕∕ КОН Ι ̸̸ ̸
- 16. Химические свойства. V. Реакции с магнийорганическими соединениями. О ОМgBr первичный ΙΙ Ι Н2О спирт С +
- 17. Получение. 1. Окисление спиртов
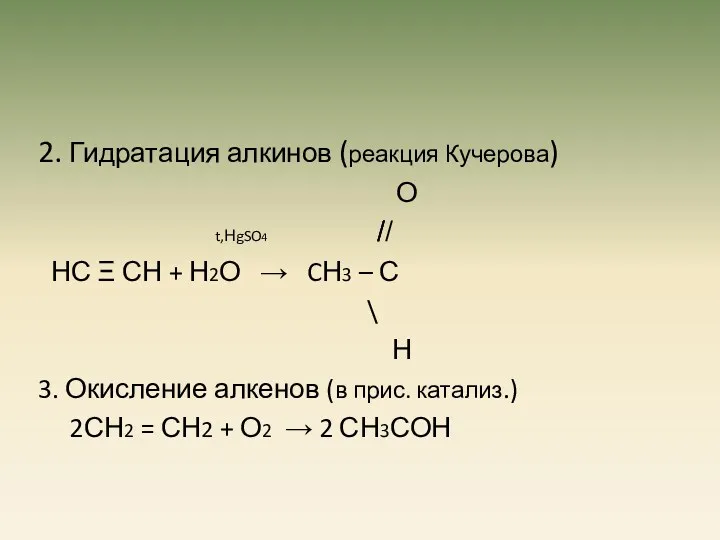
- 18. 2. Гидратация алкинов (реакция Кучерова) О t,НgSO4 ̸̸̸ ̸ НС Ξ СН + Н2О → CН3
- 19. Ацетальдегид Альдегиды. Применение. пластмасса Ацетатное волокно
- 21. Булочки ванильные, корицы аромат, Амаретто, шоколад Альдегидов вкус таят В землянике и кокосе И в жасмине
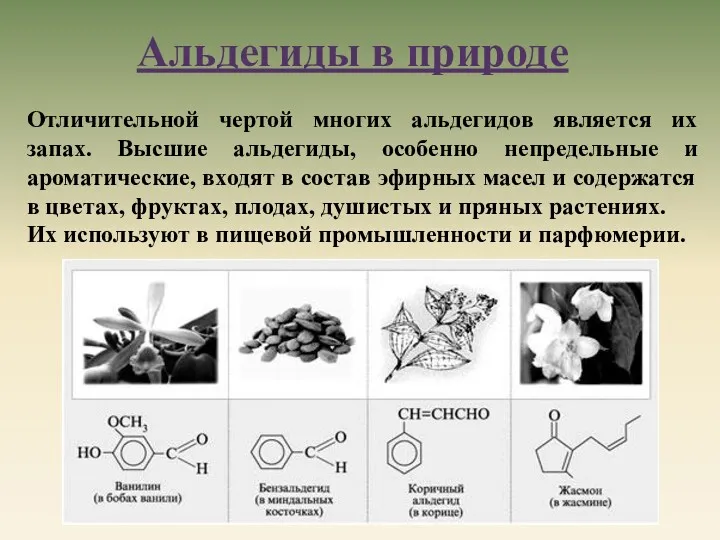
- 22. Отличительной чертой многих альдегидов является их запах. Высшие альдегиды, особенно непредельные и ароматические, входят в состав
- 23. В плодах ванили содержится ароматический альдегид, который придает им характерный запах. Ванилин применяется в парфюмерии, кондитерской
- 24. Фенилэтаналь Фенилэтаналь по сравнению с бензальдегидом лучше соответствует рецептору цветочного запаха. Фенилэтаналь пахнет гиацинтом. Альдегиды в
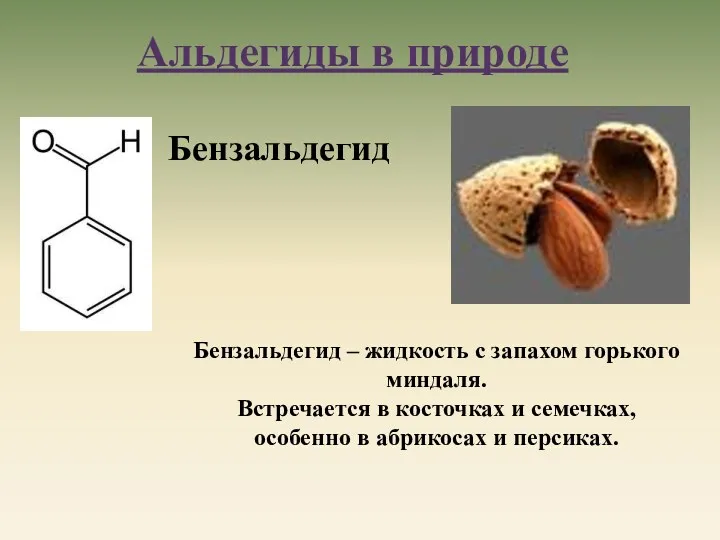
- 25. Бензальдегид Бензальдегид – жидкость с запахом горького миндаля. Встречается в косточках и семечках, особенно в абрикосах
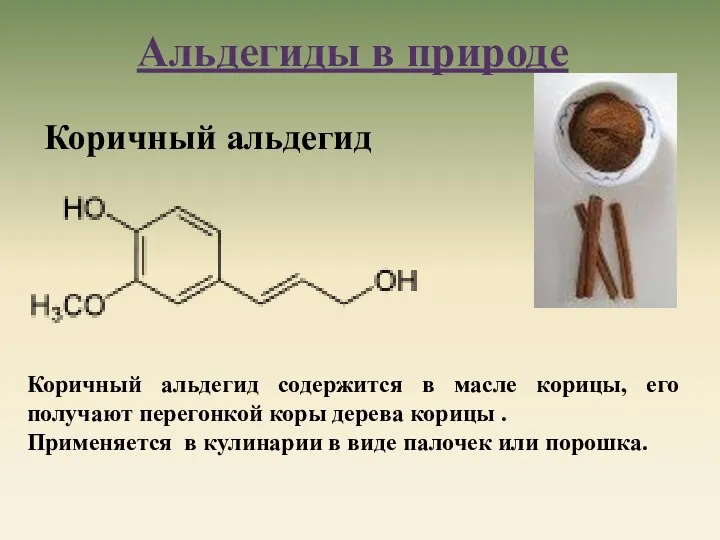
- 26. Коричный альдегид Коричный альдегид содержится в масле корицы, его получают перегонкой коры дерева корицы . Применяется
- 28. Скачать презентацию















 Таинственные острова математики
Таинственные острова математики Портфолио учителя начальных классов Дудиной Е. А.
Портфолио учителя начальных классов Дудиной Е. А. Приемы и техники массажа. Движение
Приемы и техники массажа. Движение ГСНТИ как информационная система
ГСНТИ как информационная система Характеристика детей, имеющих общее недоразвитие речи.
Характеристика детей, имеющих общее недоразвитие речи. Наша школьная жизнь
Наша школьная жизнь Презентация к дистанционному уроку Типы химических реакций на примере свойств воды. 8 класс
Презентация к дистанционному уроку Типы химических реакций на примере свойств воды. 8 класс Одночлен. 7 класс
Одночлен. 7 класс Презентация Методы и приемы обучения по речевому направлению в ДОУ
Презентация Методы и приемы обучения по речевому направлению в ДОУ Семейный кодекс РФ
Семейный кодекс РФ Artificial Intelligence
Artificial Intelligence Хлебобулочные изделия
Хлебобулочные изделия Токарный станок по дереву. Технология точения конических, фасонных и внутренних поверхностей
Токарный станок по дереву. Технология точения конических, фасонных и внутренних поверхностей Прямоугольный параллелепипед
Прямоугольный параллелепипед Климактерический период в жизни женщины
Климактерический период в жизни женщины Дидактическая игра Волшебный экран
Дидактическая игра Волшебный экран Элементы налогообложения
Элементы налогообложения Структура газообразных, жидких и твердых тел. 5 класс
Структура газообразных, жидких и твердых тел. 5 класс Зонирование территории: типы и рыночный эффект. Лекция 4
Зонирование территории: типы и рыночный эффект. Лекция 4 Архангельская губерния в XIX веке. Освоение Арктики
Архангельская губерния в XIX веке. Освоение Арктики Исход евреев из Египта
Исход евреев из Египта Вирусы и бактериофаги. Неклеточные формы жизни
Вирусы и бактериофаги. Неклеточные формы жизни Визитная карточка МБДОУ № 23 г. Коврова Муниципальное дошкольное образовательное учреждение детский сад № 23 Радуга г. Коврова
Визитная карточка МБДОУ № 23 г. Коврова Муниципальное дошкольное образовательное учреждение детский сад № 23 Радуга г. Коврова Воскресная школа сегодня и завтра
Воскресная школа сегодня и завтра Инвестиция
Инвестиция Социальное государство
Социальное государство Архангельск в годы Великой отечественной войны
Архангельск в годы Великой отечественной войны Буква, строка, текст. Искусство шрифта. (8 класс)
Буква, строка, текст. Искусство шрифта. (8 класс)