Слайд 2

ПЕРМАНГАНАТОМЕТРИЯ – метод объемного
(титриметрического) химического
анализа, основанный на применении
стандартного
(имеющего строго
определенную концентрацию) раствора
перманганата калия KMnO4.
Слайд 3

Наибольшее распространение в
аналитической практике получил
перманганатометрический метод
определения в кислых
средах:
восстановление МnО4- до Мn2+
проходит быстро и стехиометрично:
МnО4- + 8Н+ + 5 е- → Мn2+ + 4Н2О.
Слайд 4

При титровании в сильно кислых
средах чаще всего
используют серную кислоту
Количественно
восстановление
перманганата в
щелочной среде до манганата
протекает
в присутствии соли бария.
Слайд 5

Перманганатометрически в щелоч-
ной среде, как правило, определяют
органические соединения:
формиаты, формальдегид,
муравьиную, коричную, винную,
лимонную
кислоты, гидразин, ацетон и др.
Слайд 6

Признаком окончания титрования служит
бледно-розовая окраска избытка
титранта КМnО4(одна капля 0,004 моль/л
раствора титранта
придает заметную
окраску 100 мл раствора).
Слайд 7

К достоинствам перманганатометрического метода относят: 1) возможность титрования раствором КМnО4 в
любой среде (кислой, нейтральной, щелочной);
2) применимость растворов перманганата калия в кислой среде для определения многих веществ, которые не взаимодействуют с более слабыми окислителями
3) стехиометричность и достаточно высокую
скорость большинства окислительно-восстанови-
тельных реакций с участием МnО4- при оптимальновыбранных условиях ; 4) возможность титрования без индикатора;
5) доступность перманганата калия.
Слайд 8
Метод перманганатометрии имеет ряд недостатков:
1) титрант КМnО4 готовят как вторичный
стандарт,
поскольку исходный реагент – перманганат калия – трудно
получить в химически чистом состоянии; 2) реакции с
участием МnО4- возможны в определенных условиях
(рН, температура и т.д.); 3) титрование раствором КМnО4 не
рекомендуется проводить в присутствии С1-, что затрудняет
определение некоторых веществ, поскольку
НС1 часто применяют для растворения минеральных
объектов.







 Системный блок ПК
Системный блок ПК Тест с подсказками для закрепления знаний по теме Кислоты (8 класс)
Тест с подсказками для закрепления знаний по теме Кислоты (8 класс) Взаимодействие генов и их множественное действие
Взаимодействие генов и их множественное действие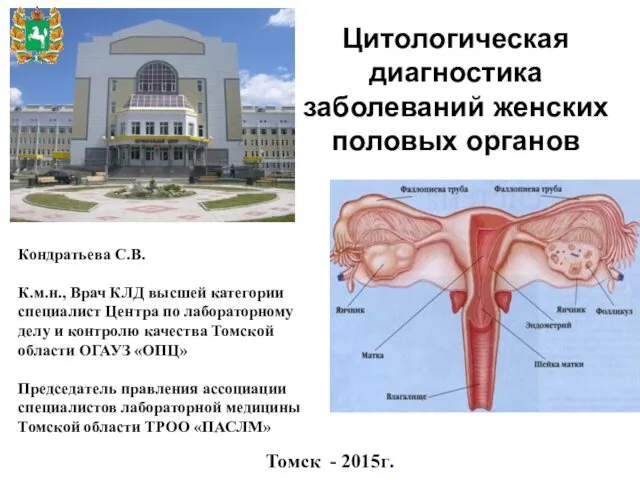 Цитологическая диагностика заболеваний женских половых органов
Цитологическая диагностика заболеваний женских половых органов Алканы, алкены, алкины
Алканы, алкены, алкины Електрозбереження в родині
Електрозбереження в родині Робототехника. Системы дистанционного управления. Технологические основы и направления роботизации
Робототехника. Системы дистанционного управления. Технологические основы и направления роботизации L_1_2_Sistema_Nats_bezopasn
L_1_2_Sistema_Nats_bezopasn Сказка Звездочки
Сказка Звездочки Деятельность саморегулируемых организаций по повышению качества работы кадастровых инженеров
Деятельность саморегулируемых организаций по повышению качества работы кадастровых инженеров A Case Bronchitis
A Case Bronchitis Основы SOA. Сервис-ориентированная архитектура
Основы SOA. Сервис-ориентированная архитектура Красота музыки Испании
Красота музыки Испании материалы к урокам 1 класс УМК Школа 2100
материалы к урокам 1 класс УМК Школа 2100 Презентация к классному часу Огонь - наш друг или враг...
Презентация к классному часу Огонь - наш друг или враг... Обморок- это временная потеря сознания, обусловленная внезапным снижением мозгового кровотока
Обморок- это временная потеря сознания, обусловленная внезапным снижением мозгового кровотока Кто нас защищает?
Кто нас защищает? Организация ЭВМ и вычислительных систем. ЛЕКЦИЯ 2. Вводная часть В3(продолжение)
Организация ЭВМ и вычислительных систем. ЛЕКЦИЯ 2. Вводная часть В3(продолжение) Решение заданий С2 при подготовке к ЕГЭ 2014
Решение заданий С2 при подготовке к ЕГЭ 2014 Хлеб.
Хлеб. Интегрированный урок математика+география
Интегрированный урок математика+география Мікропроцесорна техніка PSoC Creator 4.2 Designing with PSoC 3/5. (Лекція 7)
Мікропроцесорна техніка PSoC Creator 4.2 Designing with PSoC 3/5. (Лекція 7) Общие положения концепции жизненного цикла систем. Проектное управление – форма реализации концепции жизненного цикла систем
Общие положения концепции жизненного цикла систем. Проектное управление – форма реализации концепции жизненного цикла систем Подготовка природных газов к переработке
Подготовка природных газов к переработке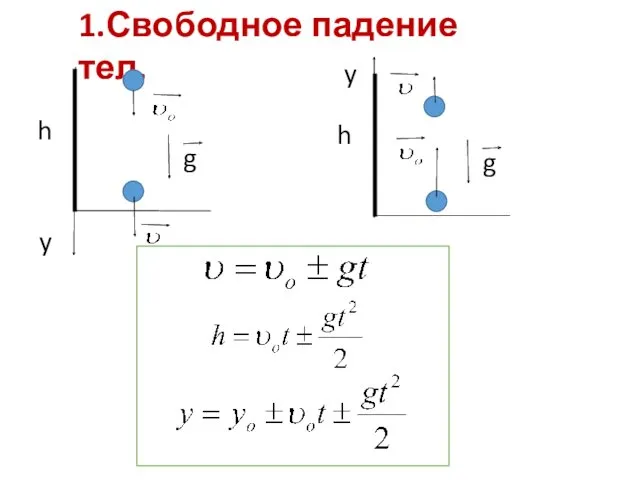 Свободное падение тел. Движение тела, брошенного под углом к горизонту
Свободное падение тел. Движение тела, брошенного под углом к горизонту Четырехугольник. Виды четырехугольника
Четырехугольник. Виды четырехугольника Презентация к уроку: Основания
Презентация к уроку: Основания Презентация
Презентация