Содержание
- 2. Ароматические амины. Анилин Производные аммиака в которых атом водорода замещен на аррильный или алкильный радикал Ароматические
- 3. История открытия Впервые анилин был получен в 1826 году при перегонке индиго с известью немецким химиком
- 4. Получение 1. Восстановление нитросоединений. В качестве восстановителей нитросоединений используют различные реагенты: H2/Pt,Pd,Ni; Sn/HCl; SnCl2/HCl; Fe/HCl; Fe/H2O
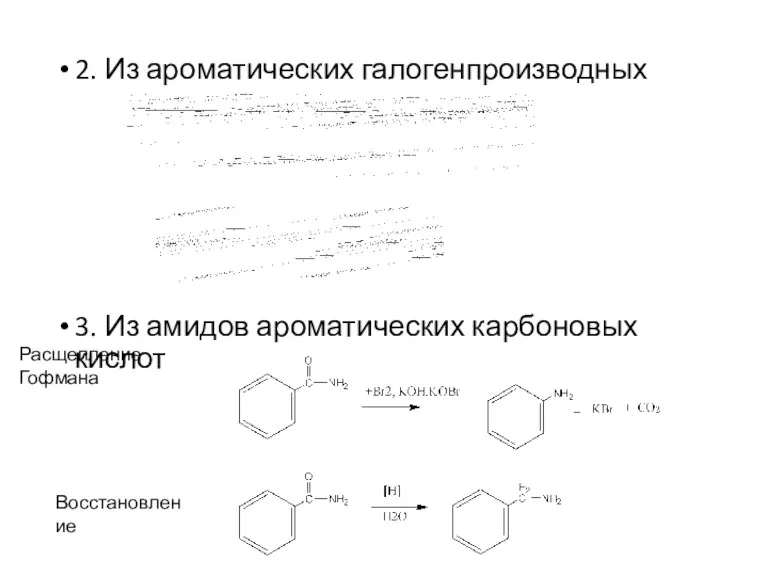
- 5. 2. Из ароматических галогенпроизводных 3. Из амидов ароматических карбоновых кислот Расщепление Гофмана Восстановление
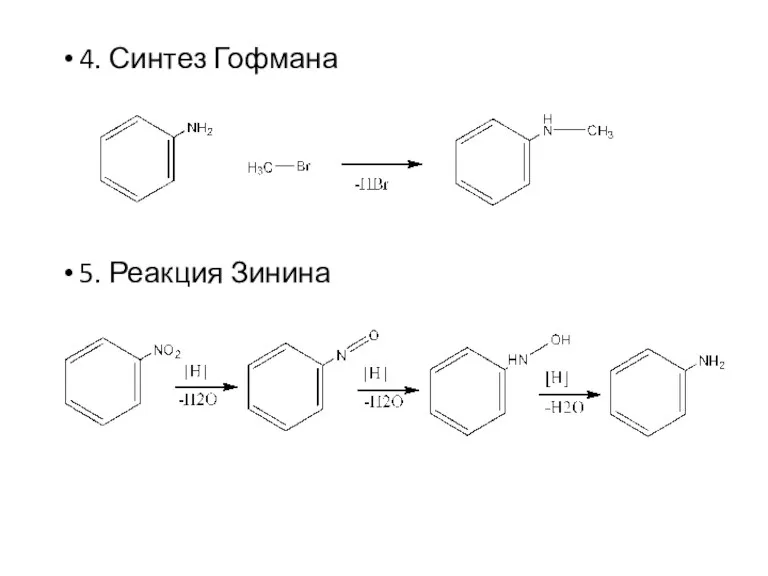
- 6. 4. Синтез Гофмана 5. Реакция Зинина
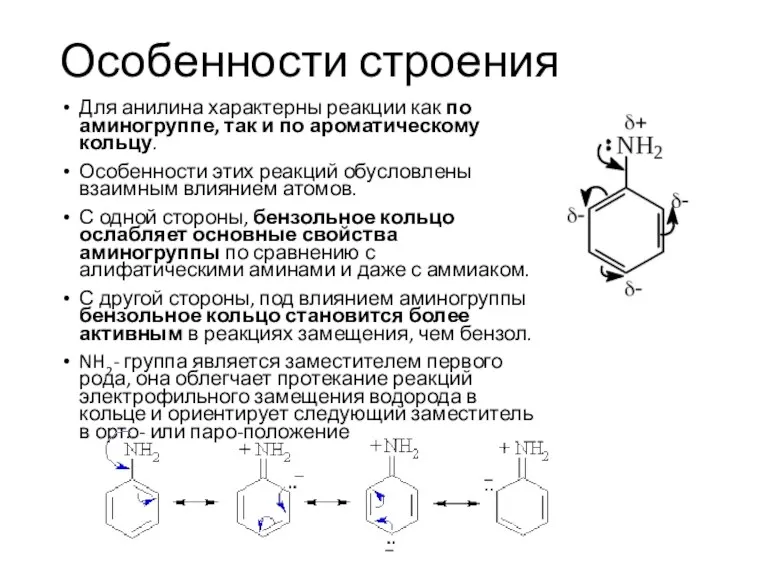
- 7. Особенности строения Для анилина характерны реакции как по аминогруппе, так и по ароматическому кольцу. Особенности этих
- 8. Химические свойства 1. Кислотно-основные свойства Ароматические амины менее сильные основания, чем аммиак и алкиламины. Делокализация неподеленной
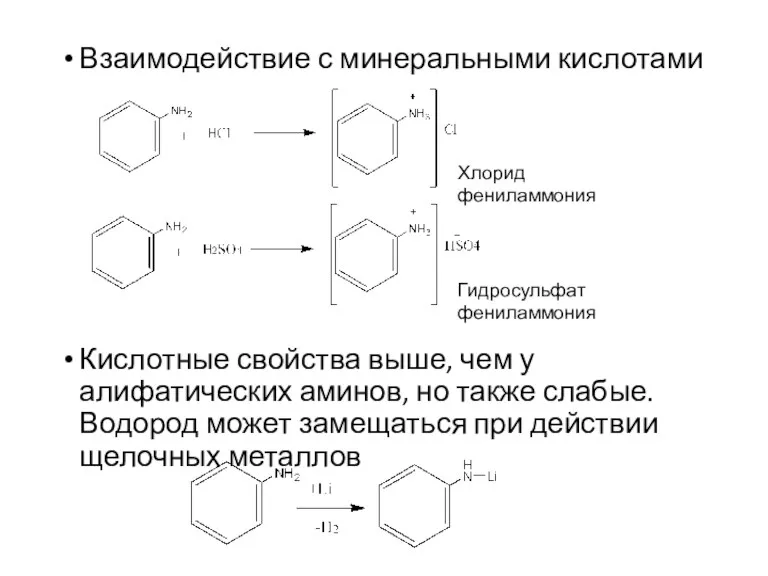
- 9. Взаимодействие с минеральными кислотами Кислотные свойства выше, чем у алифатических аминов, но также слабые. Водород может
- 10. 2. Реакции по амино-группе Алкилирование Арилирование Ацилирование Ацилирование карбоновыми кислотами и их производными (ангидридами, галогенангидридами, сложными
- 11. Конденсация с карбонильными соединениями Реакция с азотистой кислотой Реакция с азотистой кислотой – качественная реакция на
- 12. Вторичные ароматические амины нитрозируются с образованием N-нитрозоаминов. Ароматические N-нитрозоамины при действии минеральных кислот перегруппировываются в п-нитрозо-N-алкилариламины
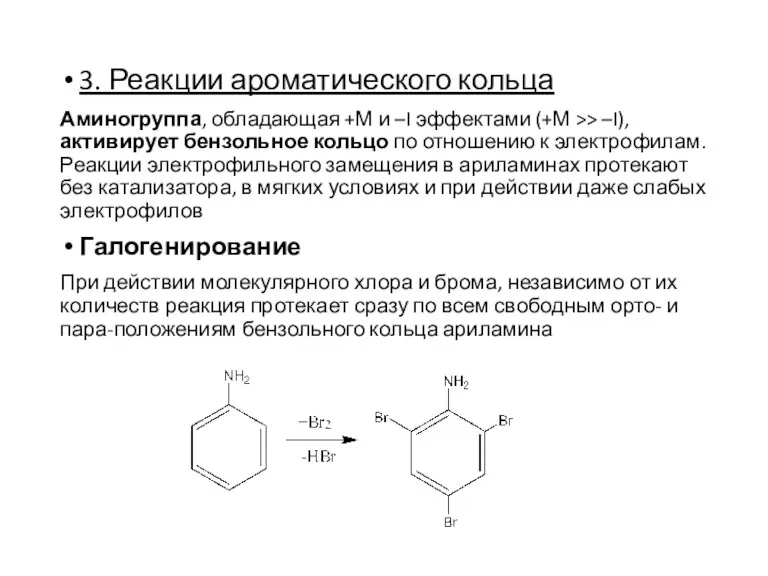
- 13. 3. Реакции ароматического кольца Аминогруппа, обладающая +М и –I эффектами (+М >> –I), активирует бензольное кольцо
- 14. Нитрование Первичные и вторичные ариламины легко окисляются азотной кислотой, поэтому для получения нитрозамещенных ариламинов требуется защита
- 15. Сульфирование Аминогруппа при действии конц. серной кислоты протонируется, а образующаяся аммониевая группа -NH3+ является электроноакцепторным заместителем,
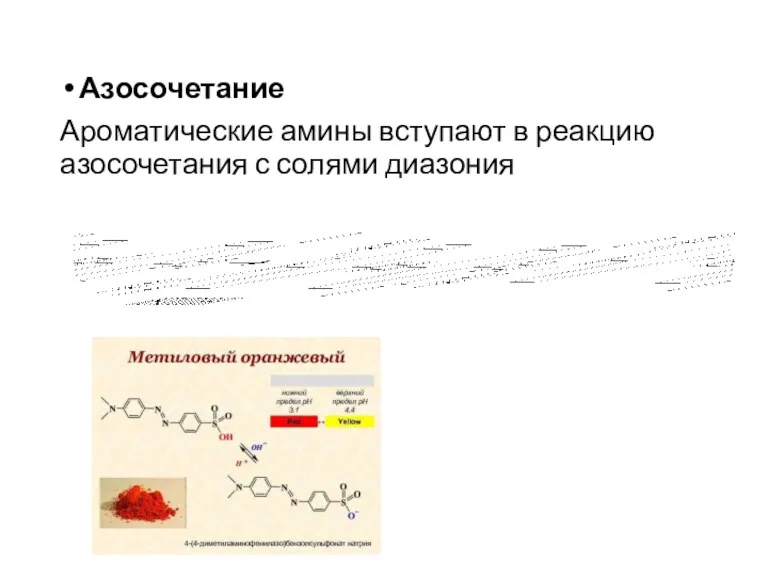
- 16. Азосочетание Ароматические амины вступают в реакцию азосочетания с солями диазония
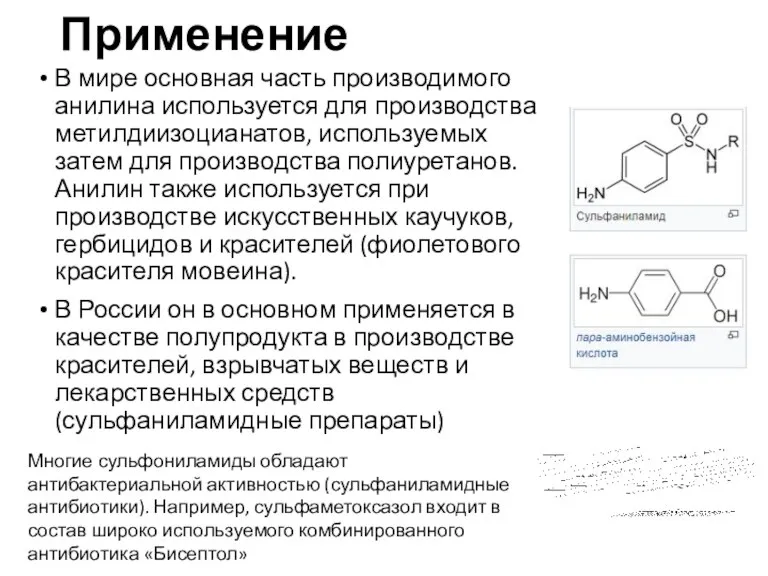
- 17. Применение В мире основная часть производимого анилина используется для производства метилдиизоцианатов, используемых затем для производства полиуретанов.
- 18. Токсикология Анилин ядовит. Оказывает негативное воздействие на центральную нервную систему. Кровеносный яд, вызывает кислородное голодание организма
- 19. Диазосоединения Диазосоединения представляют собой органические молекулы, содержащие два связанных между собой атома азота, причем один из
- 20. Примеры нейтральных (ковалентных) диазосоединений: В ароматическом ряду известны катионные формы диазосоединений (катионы диазония). Многие катионы арилдиазония
- 21. Получение Для получения ароматических солей диазония применяют реакцию диазотирования (П. Грисс), которая представляет собой взаимодействие первичных
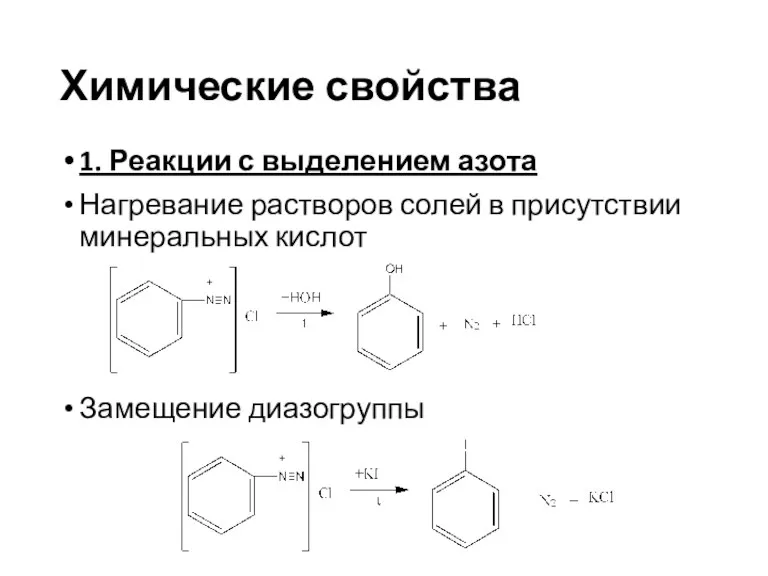
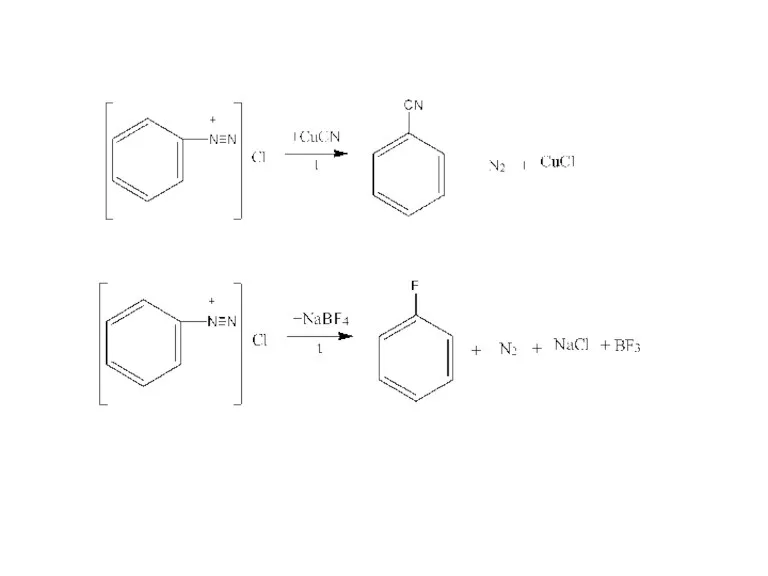
- 22. Химические свойства 1. Реакции с выделением азота Нагревание растворов солей в присутствии минеральных кислот Замещение диазогруппы
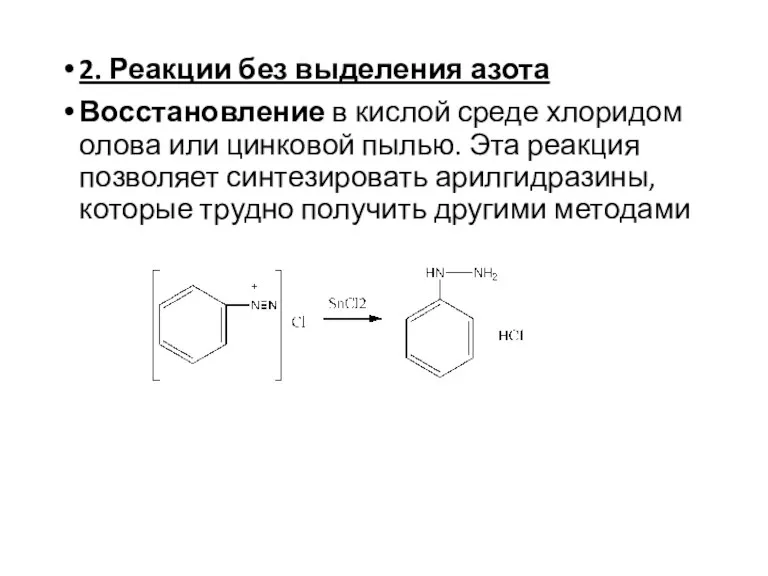
- 24. 2. Реакции без выделения азота Восстановление в кислой среде хлоридом олова или цинковой пылью. Эта реакция
- 25. Азосочетание Реакция азосочетания представляет собой электрофильное замещение атома водорода, когда в качестве электрофила выступает диазониевый ион
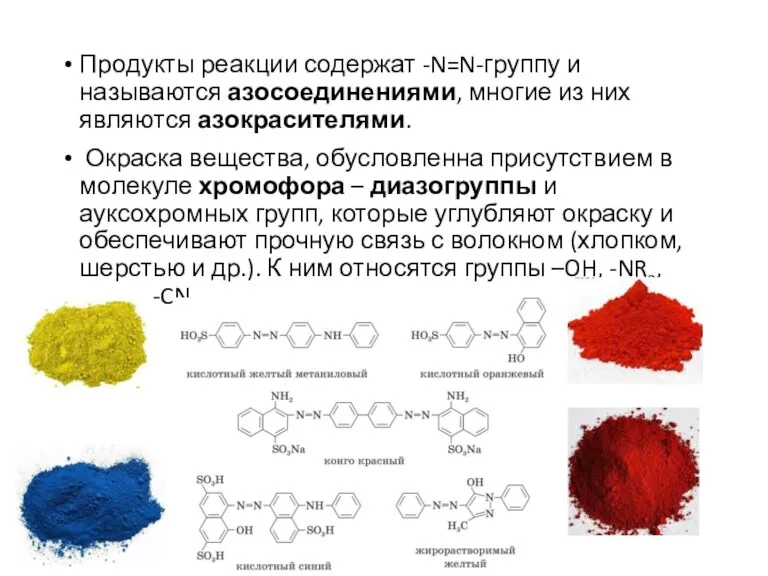
- 26. Продукты реакции содержат -N=N-группу и называются азосоединениями, многие из них являются азокрасителями. Окраска вещества, обусловленна присутствием
- 27. Нитроарены Нитроарены могут быть получены либо электрофильным замещением водорода, либо посредством нуклеофильного замещения функциональных групп (галогены,
- 28. Нитрогруппа, как сильный мезомерный акцептор, инициирует перераспределение электронной плотности в π-системе ароматического ядра. При этом наибольший
- 29. Восстановление нитробензола. В зависимости от условий ее проведения, позволяет получить целый ряд разнообразных продуктов При использовании
- 31. Скачать презентацию

















 B13. Задачи на концентрацию и сплавы
B13. Задачи на концентрацию и сплавы Строение и свойства металлов Физические и механические свойства металлов
Строение и свойства металлов Физические и механические свойства металлов Геохимия гидросферы
Геохимия гидросферы Химические реакции в растворах электролитов. Обобщение и систематизация знаний
Химические реакции в растворах электролитов. Обобщение и систематизация знаний Чистые вещества и смеси
Чистые вещества и смеси Амины
Амины Основы теории пространственного строения органических соединений. Конфигурации и конформации. Лекция 1
Основы теории пространственного строения органических соединений. Конфигурации и конформации. Лекция 1 Общие сведения об электрорадиоматериалах
Общие сведения об электрорадиоматериалах Organic compounds: nomenclature
Organic compounds: nomenclature Изотопный обмен
Изотопный обмен Электронный помощник по химии 8 класс
Электронный помощник по химии 8 класс Классификация органических соединений
Классификация органических соединений Типы химических реакций
Типы химических реакций Уральские горы. Самоцветы
Уральские горы. Самоцветы Углерод
Углерод Ионная химическая связь
Ионная химическая связь Вуглеводні. Підсумковий урок 9 клас
Вуглеводні. Підсумковий урок 9 клас Композиты и композиционные материалы
Композиты и композиционные материалы Щелочные металлы
Щелочные металлы Механизмы реакций органических соединений
Механизмы реакций органических соединений Пластмасса
Пластмасса Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады) Алканы. Углеводороды. Предельные (насыщенные, алканы)
Алканы. Углеводороды. Предельные (насыщенные, алканы) Углеводороды. Предельные нециклические (ациклические) углеводороды. Алканы
Углеводороды. Предельные нециклические (ациклические) углеводороды. Алканы Азот и его соединения
Азот и его соединения Водородная связь
Водородная связь Протолитические равновесия в растворах электролитах
Протолитические равновесия в растворах электролитах Полимеры. Каучук
Полимеры. Каучук