Содержание
- 2. Историческая справка Первоначально название «ароматические углеводороды» получили вещества, обладающие приятным запахом - например, фенилэтиловый спирт и
- 3. Физические свойства бензола При обычных условиях-бесцветная жидкость с характерным запахом, не смешивается с водой, является хорошим
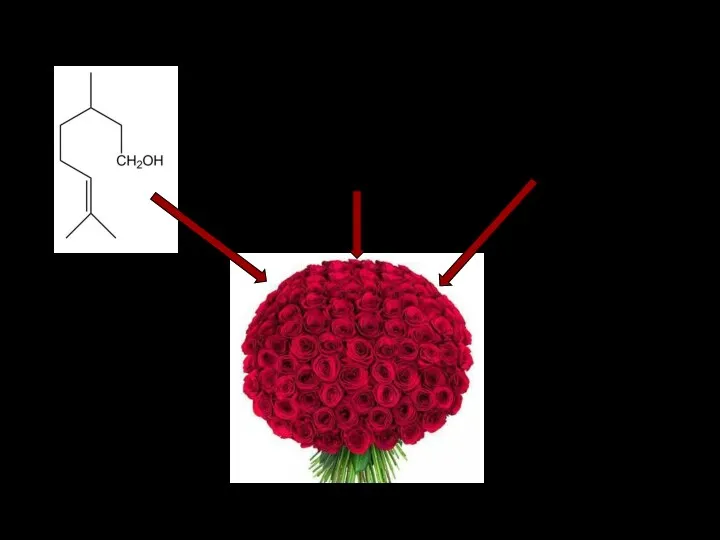
- 4. Фенилэтиловый спирт Гераниол Цитронеллол
- 5. Органические соединения, в состав которых входят одно или несколько бензольных колец, называются ароматическими углеводородами. Для гомологов
- 6. Бензол, электронное строение
- 7. Электронное строение молекулы бензола Общая формула моноциклических аренов СnH2n-6 (где n ≥ 6) показывает, что они
- 8. Бензол как бы состоит из 2-х альтернативных структур циклогексатриена-1,3,5. ⭤ Столь непредельное соединение не обесцвечивает бромную
- 9. s 2p sp2 Схема образования sp2-гибридных орбиталей атома углерода
- 10. Физическими методами установлено, что все атомы углерода и водорода в молекуле бензола лежат в одной плоскости
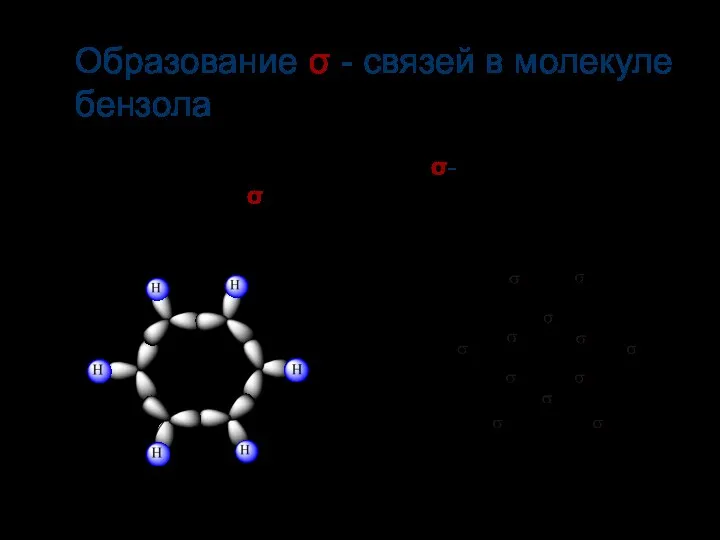
- 11. Каждый атом «С» образует три σ-связи (2 С-С и 1 С-Н σ-связи) Образование σ - связей
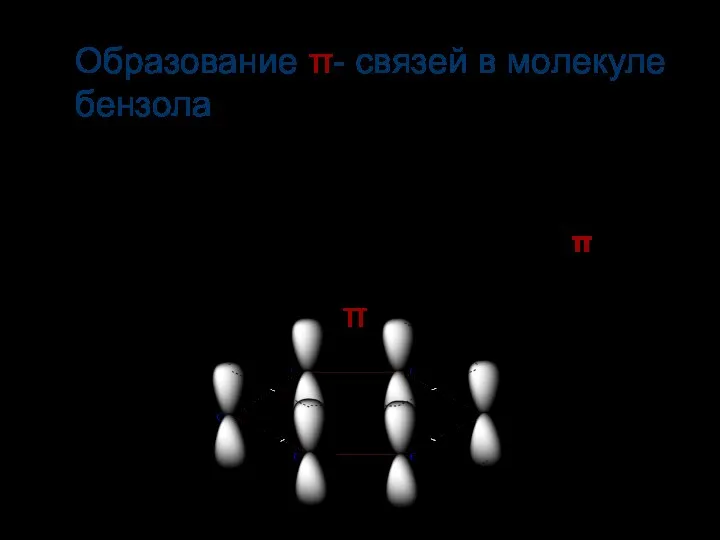
- 12. Образование π- связей в молекуле бензолa π Четвёртый негибридизированный р-электрон каждого атома «С» расположен перпендикулярно плоскости
- 13. Атомы углерода в бензоле находятся в sp2-гибридизации; Угол расположения 3-х гибридных орбиталей равен 120° и они
- 16. «HIC TUTA PERENNAT» переводится с латинского языка, как «здесь в безопасности пребывает». Римская богиня мудрости Миневра
- 17. Ароматичность. Критерии ароматичности
- 18. Критерий ароматичности – правила Хюккеля 1931 год Ароматические - плоские циклические сопряженные системы, содержащие 4n+2 делокализованных
- 19. Сравнение стабильности – теплота гидрирования
- 20. Сравнение стабильности – теплота гидрирования Циклооктатетраен не ароматичен!
- 21. Сравнение стабильности – теплота гидрирования Q=+96 кДж/моль Циклооктатетраен не ароматичен!
- 22. Сравнение стабильности – теплота гидрирования Q=+96 кДж/моль Q=+410 кДж/моль Циклооктатетраен не ароматичен!
- 23. Сравнение стабильности – теплота гидрирования Q=+96 кДж/моль Q=+410 кДж/моль Примерно в 4 раза больше. Циклооктатетраен не
- 24. Сравнение стабильности – теплота гидрирования непредельных циклогексанов
- 25. Q=+120 кДж/моль Q=+232 кДж/моль Q=+(340-360) кДж/моль Q=+208 кДж/моль
- 26. Q=+120 кДж/моль Q=+232 кДж/моль Q=+(340-360) кДж/моль Q=+208 кДж/моль
- 27. Q=+120 кДж/моль Q=+232 кДж/моль Q=+(340-360) кДж/моль Q=+208 кДж/моль
- 28. Q=+120 кДж/моль Q=+232 кДж/моль Q=+(340-360) кДж/моль Q=+208 кДж/моль
- 29. Q=+120 кДж/моль Q=+232 кДж/моль Q=+(340-360) кДж/моль Q=+208 кДж/моль
- 30. Q=+120 кДж/моль Q=+232 кДж/моль Q=+(340-360) кДж/моль Q=+208 кДж/моль
- 31. Q=+120 кДж/моль Q=+232 кДж/моль Q=+(340-360) кДж/моль Q=+208 кДж/моль
- 32. Химические свойства бензола
- 33. Химические свойства бензола Ароматическая связь определяет свойства бензола 6 π-электронная система является более устойчивой, чем обычные
- 34. I. Реакции присоединения Хлорирование Гексахлорциклогексан (гексахлоран-инсектицид) Гидрирование
- 35. Реакция сульфирования Сульфобензол; бензолсульфокислота II. Реакции замещения Реакция нитрования (нитруют смесью конц. кислот) Нитробензол
- 36. Реакция Зинина Водород в момент выделения: [H], а не H2 Из анилина далее азокрасители (рассмотрим позднее).
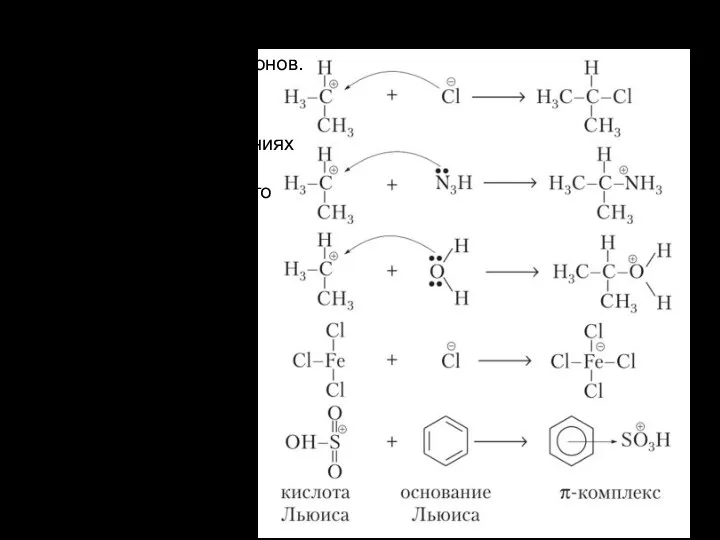
- 37. Кислоты Льюиса -акцепторы пары электронов. Для реакций SE в ароматических соединениях необходимы в качестве катализатора. Чаще
- 38. II. Реакции замещения Реакция галогенирования
- 39. Механизм реакции электрофильного замещения SE в ароматических соединениях
- 40. Механизм реакции электрофильного замещения SE в ароматических соединениях
- 41. Механизм реакции электрофильного замещения SE в ароматических соединениях δ− δ+
- 42. Реакции алкилирования (реакции Фриделя-Крафтса) 1. с галогеналканами 2. с алкенами 3. со спиртами II. Реакции замещения
- 43. Реакции алкилирования (реакции Фриделя-Крафтса) Изопропилбензол (кумол) II. Реакции замещения Но! Происходит изомеризация:
- 44. Реакции алкилирования (реакции Фриделя-Крафтса) II. Реакции замещения Но! Происходит изомеризация: Изопропилбензол (кумол)
- 45. Реакции алкилирования (реакции Фриделя-Крафтса). II. Реакции замещения За счёт чего происходит изомеризация
- 46. Реакции алкилирования (реакции Фриделя-Крафтса). II. Реакции замещения За счёт чего происходит изомеризация
- 47. Реакции алкилирования (реакции Фриделя-Крафтса). II. Реакции замещения За счёт чего происходит изомеризация Более стабильный катион
- 48. Реакции алкилирования (реакции Фриделя-Крафтса). II. Реакции замещения За счёт чего происходит изомеризация
- 49. Зачем нужен кумол
- 50. Как избежать изомеризации – реакция с ацилгалогенидами (хлорангидридами карбоновых кислот) Реакции алкилирования (реакции Фриделя-Крафтса). II. Реакции
- 51. Как избежать изомеризации – реакция с ацилгалогенидами (хлорангидридами карбоновых кислот) Реакции алкилирования (реакции Фриделя-Крафтса). II. Реакции
- 52. Реакции замещения с производными бензола Ориентационные эффекты заместителей
- 53. Номенклатура производных бензола 1,2-диметилбензол; орто-диметилбензол (о-диметилбензол)
- 54. Номенклатура производных бензола 1,2-диметилбензол; орто-диметилбензол (о-диметилбензол) 1,3-диметилбензол; мета-диметилбензол (м-диметилбензол)
- 55. Номенклатура производных бензола 1,2-диметилбензол; орто-диметилбензол (о-диметилбензол) 1,4-диметилбензол; пара-диметилбензол (п-диметилбензол) 1,3-диметилбензол; мета-диметилбензол (м-диметилбензол)
- 56. Наиболее характерными реакциями для ароматических углеводородов являются реакции электрофильного замещения SE. Химические свойства бензола
- 57. Наиболее характерными реакциями для ароматических углеводородов являются реакции электрофильного замещения SE. Химические свойства бензола Протекание реакции
- 58. Наиболее характерными реакциями для ароматических углеводородов являются реакции электрофильного замещения SE. Химические свойства бензола Протекание реакции
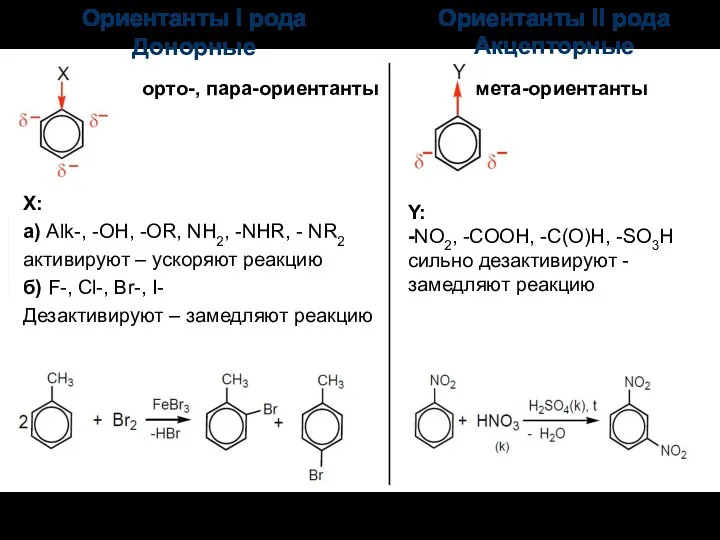
- 59. Ориентанты I рода Донорные Ориентанты II рода Акцепторные орто-, пара-ориентанты мета-ориентанты X: а) Alk-, -OH, -OR,
- 61. Скачать презентацию
























![Реакция Зинина Водород в момент выделения: [H], а не H2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/322125/slide-35.jpg)





















 Оксиды (1 этап изучения). 8 класс
Оксиды (1 этап изучения). 8 класс Кислотно-основное равновесие в процессах жизнедеятельности. Ионное произведение воды. Водородный показатель
Кислотно-основное равновесие в процессах жизнедеятельности. Ионное произведение воды. Водородный показатель 20230419_kolichestvo_veshchestva_mol
20230419_kolichestvo_veshchestva_mol Поверхностные явления
Поверхностные явления Углеводороды ациклические, циклические
Углеводороды ациклические, циклические Химия в сельском хозяйстве. Химизация сельского хозяйства и ее направления
Химия в сельском хозяйстве. Химизация сельского хозяйства и ее направления Синтетические методы получения лекарственных средств гетероциклического ряда антибиотики с четырехчленным азетидиновым ядром
Синтетические методы получения лекарственных средств гетероциклического ряда антибиотики с четырехчленным азетидиновым ядром Черная металлургия
Черная металлургия Органічна хімія, частина 1
Органічна хімія, частина 1 Тіршілік процесіне қатысатын гетерофункционалды қосылыстар
Тіршілік процесіне қатысатын гетерофункционалды қосылыстар Классификация моторных масел
Классификация моторных масел Физические и химические свойства воды
Физические и химические свойства воды Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Получение хлортетрациклина
Получение хлортетрациклина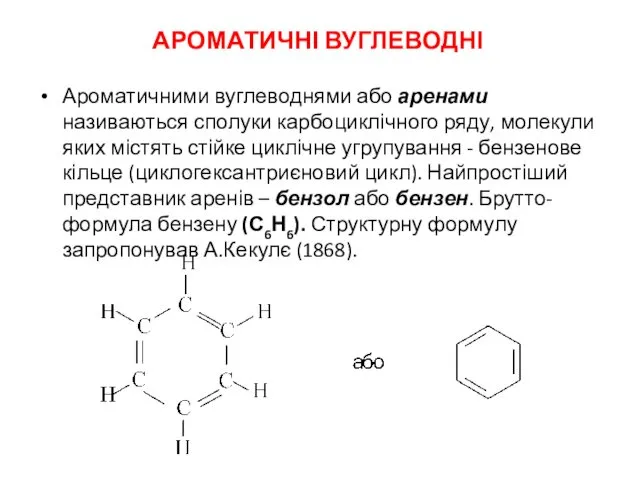 Ароматичні вуглеводні
Ароматичні вуглеводні Чистые вещества и смеси
Чистые вещества и смеси Массовая доля вещества в растворе
Массовая доля вещества в растворе Водородные и кислородные соединения неметаллов. Галогеноводороды. Соляная кислота
Водородные и кислородные соединения неметаллов. Галогеноводороды. Соляная кислота Химия пәні. Заттар және олардың қасиеттері
Химия пәні. Заттар және олардың қасиеттері Жескость воды
Жескость воды Классы органических соединений
Классы органических соединений Азотсодержащие соединения. Амины. Аминокислоты
Азотсодержащие соединения. Амины. Аминокислоты Пищевые добавки
Пищевые добавки Общая электронная теория восстановления и окисления металлов
Общая электронная теория восстановления и окисления металлов Минералы. Свойства минералов
Минералы. Свойства минералов Галогены. Положение галогенов в ПСХЭ
Галогены. Положение галогенов в ПСХЭ Кристаллические решетки
Кристаллические решетки Предмет органической химии. Органические вещества
Предмет органической химии. Органические вещества