Слайд 2

Цель урока :
Сформировать понятия о кристаллическом или аморфном состоянии твёрдых тел.
Ознакомить
с типами кристаллических решеток.
Рассмотреть влияние химической связи на свойства твёрдых тел.
Дать представление о законе постоянства состава веществ.
Слайд 3

Актуализация полученных знаний :
Химический диктант по теме : « Соли».
Слайд 4

Агрегатное состояние вещества :
Жидкое
Твёрдое
Газообразное
Слайд 5

Твёрдые вещества :
Аморфное состояние ( нет определённой температуры плавления, они размягчаются
постепенно и переходят в текучее состояние) Это пластмассы, смолы, пластилин, воск, шоколад, жевательная резинка.
Кристаллическое состояние ( имеют определённые температуры плавления, характерно правильное расположение частиц из которых они построены ( атомов, ионов, молекул). Эти частицы находятся в определённых точках пространства.
Слайд 6

Типы кристаллических решеток.
Слайд 7

Атомная кристаллическая решетка:
Слайд 8
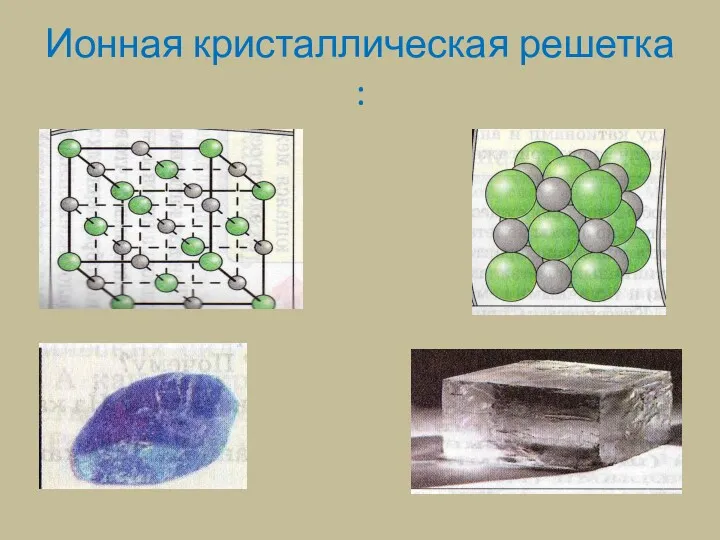
Ионная кристаллическая решетка :
Слайд 9

Молекулярная кристаллическая решетка:
Слайд 10

Закон постоянства состава веществ :
C + O2 = CO2 ↑
CaCO3 =
CaO + CO2 ↑
CaCO3 + 2 HCI = CaCI2 + CO2 ↑ + H2 O
Закон постоянства состава – гласит , что каждому веществу соответствует только одна химическая формула.









 Биогенді (s.p.d) элементтермен олардың қосылыстарының медициналық және биологиялық маңызы
Биогенді (s.p.d) элементтермен олардың қосылыстарының медициналық және биологиялық маңызы Кислоты, их состав и названия
Кислоты, их состав и названия Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Ароматические углеводороды
Ароматические углеводороды Гетерофазный катализ. (Лекция 20)
Гетерофазный катализ. (Лекция 20) Горение топлива
Горение топлива Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології
Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології Основные классы неорганических соединений
Основные классы неорганических соединений Соли, их классификация и свойства
Соли, их классификация и свойства Органічна хімія
Органічна хімія Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14
Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14 Жёсткость воды
Жёсткость воды Полисахариды: крахмал и целлюлоза
Полисахариды: крахмал и целлюлоза Растворы. Часть 2. Лекция №7
Растворы. Часть 2. Лекция №7 Химия атмосферы. Химические процессы в тропосфере
Химия атмосферы. Химические процессы в тропосфере Буферные системы
Буферные системы Белки. Строение
Белки. Строение Классификация химических элементов. Составитель. 8 класс
Классификация химических элементов. Составитель. 8 класс Минералы для ИЗБ
Минералы для ИЗБ Концентрация растворов. Массовая доля растворенного вещества. Урок 1
Концентрация растворов. Массовая доля растворенного вещества. Урок 1 Химический элемент медь
Химический элемент медь Кинетика химических реакций
Кинетика химических реакций Кремний и его соединения
Кремний и его соединения Галогены. Расположите галогены в порядке их открытия
Галогены. Расположите галогены в порядке их открытия Важнейшие реакции в органической химии
Важнейшие реакции в органической химии Технология производства аминоальдегидных смол
Технология производства аминоальдегидных смол Углерод. Физические и химические свойства
Углерод. Физические и химические свойства Гидролиз солей
Гидролиз солей