Содержание
- 2. ОСОБЕННОСТИ СТРОЕНИЯ и РЕАКЦИОННОЙ СПОСОБНОСТИ АРЕНОВ (Ar).
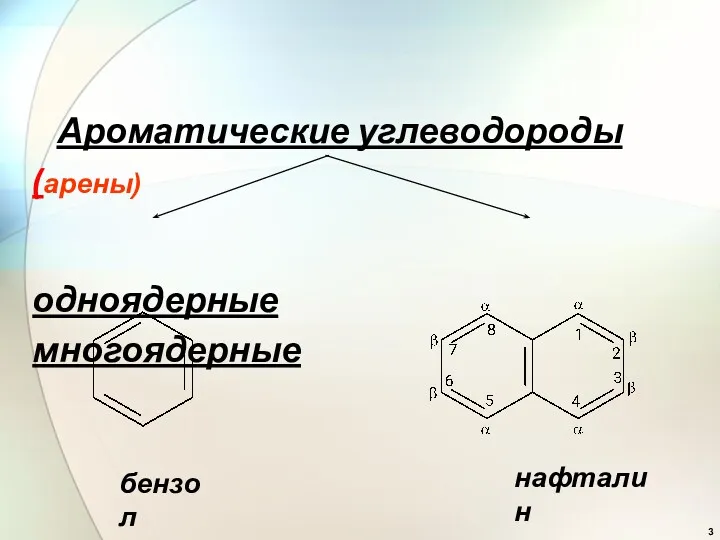
- 3. Ароматические углеводороды (арены) одноядерные многоядерные бензол нафталин
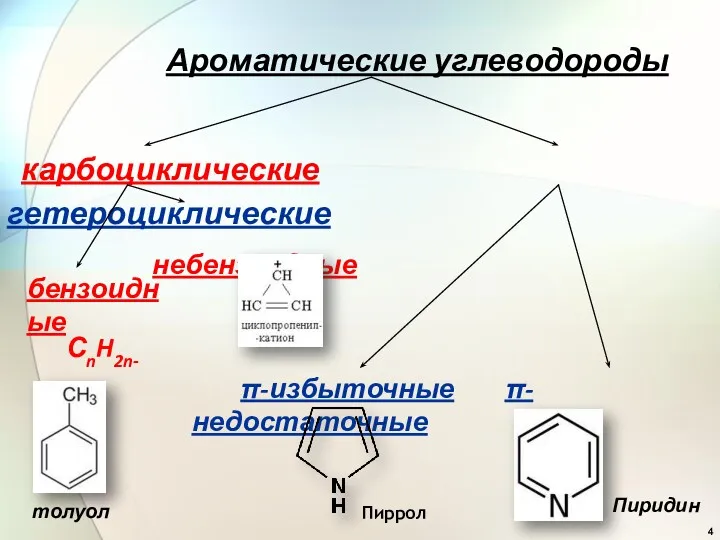
- 4. Ароматические углеводороды карбоциклические гетероциклические небензоидные бензоидные СnH2n-6 π-избыточные π-недостаточные толуол Пиррол Пиридин
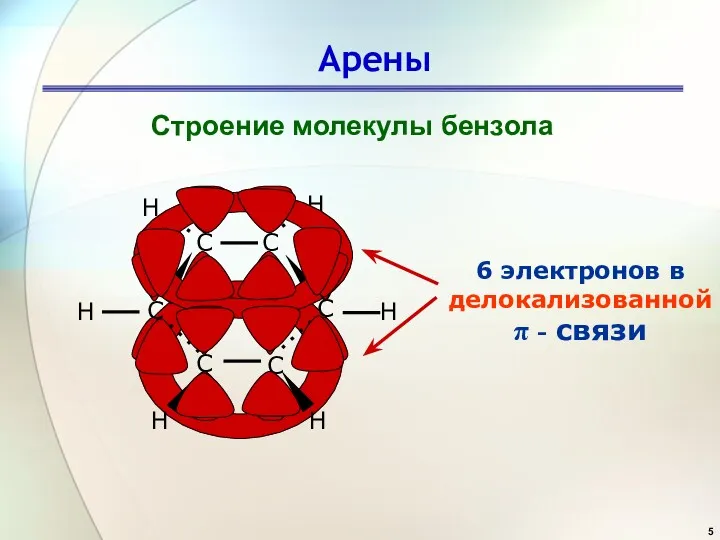
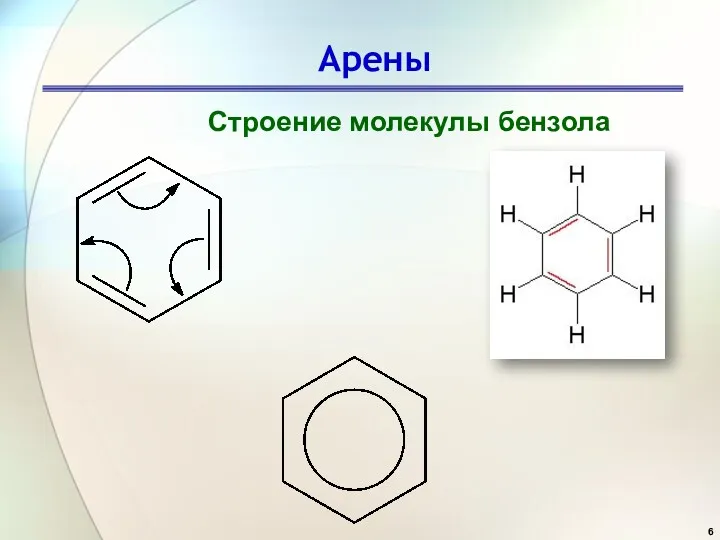
- 5. Арены Строение молекулы бензола 6 электронов в делокализованной π - связи
- 6. Арены Строение молекулы бензола
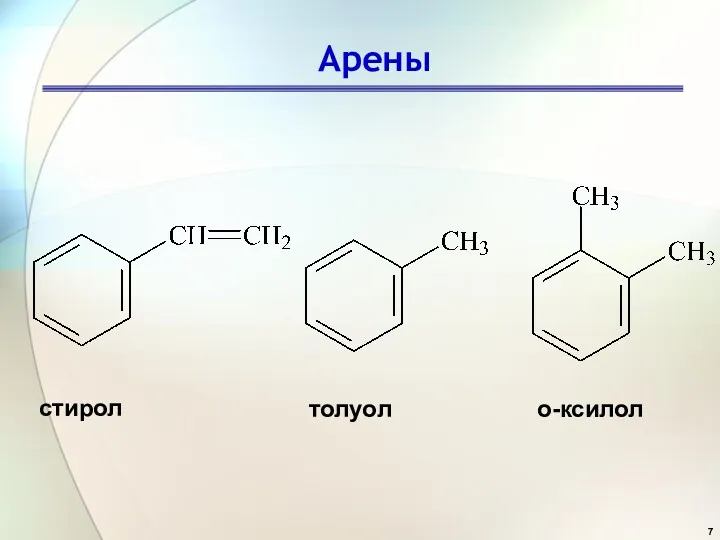
- 7. Арены стирол толуол о-ксилол
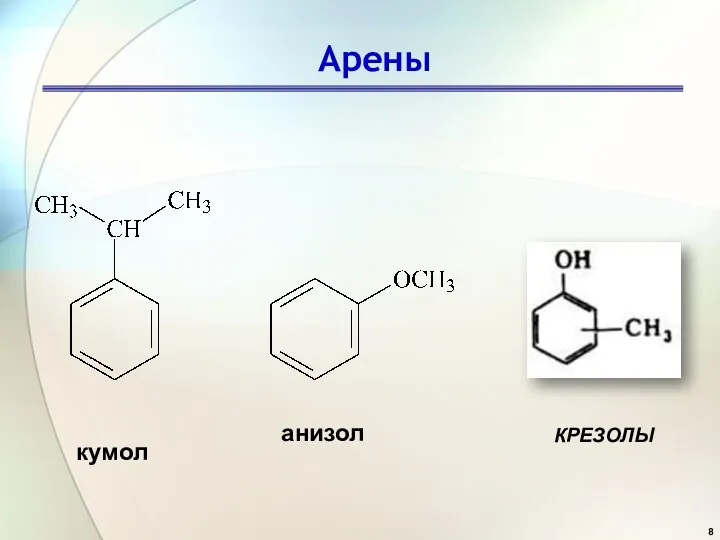
- 8. Арены кумол анизол КРЕЗОЛЫ
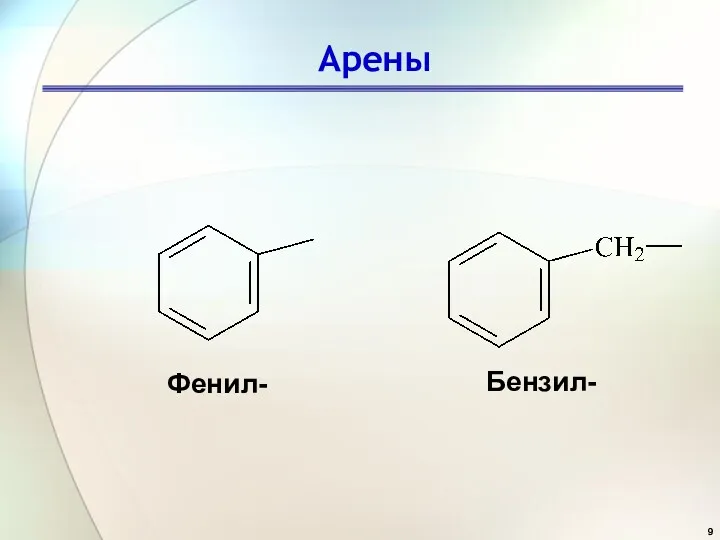
- 9. Арены Фенил- Бензил-
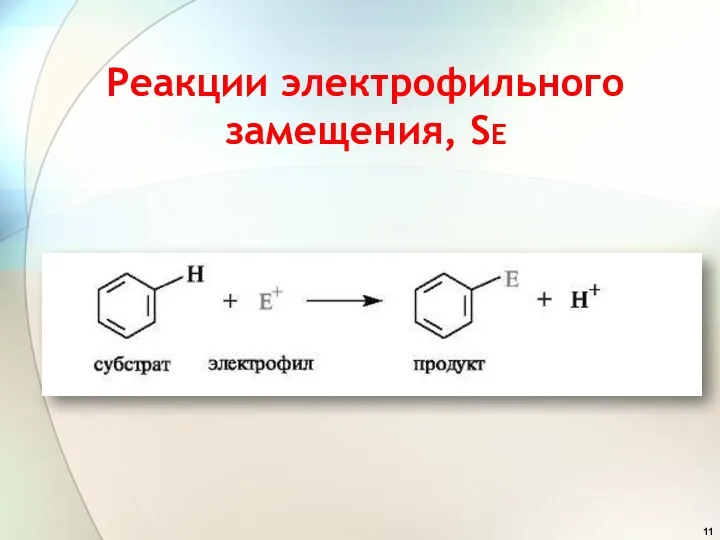
- 11. Реакции электрофильного замещения, SЕ
- 12. I. SЕ
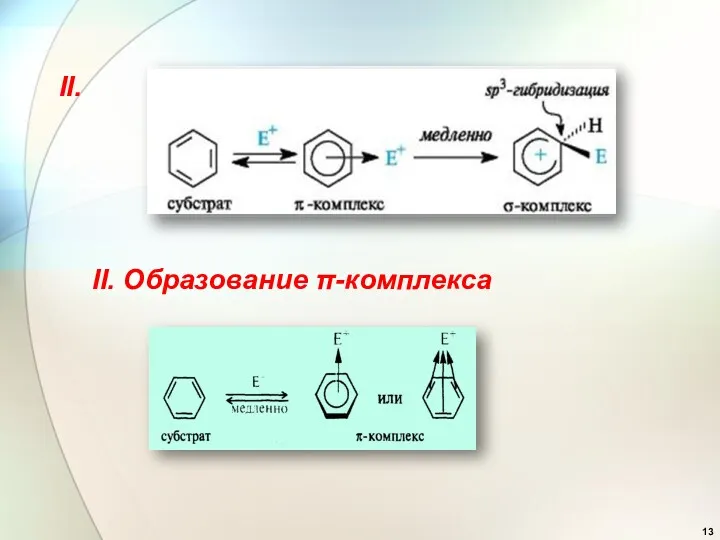
- 13. II. II. Образование π-комплекса
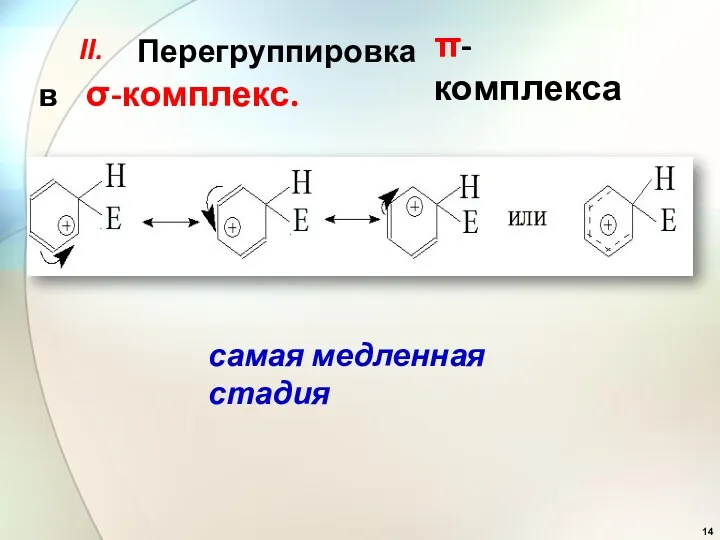
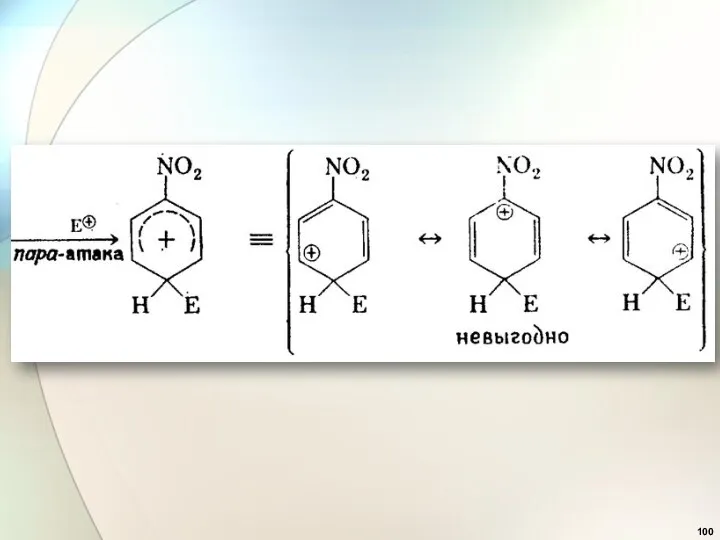
- 14. самая медленная стадия Перегруппировка в σ-комплекс. π-комплекса II.
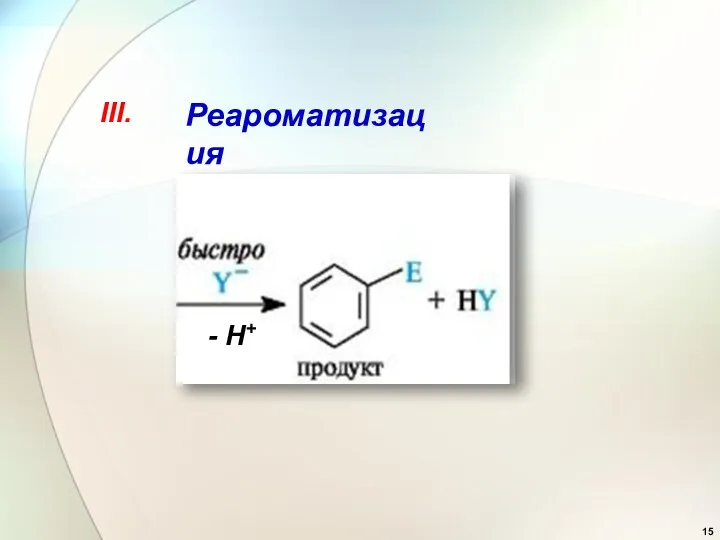
- 15. III. Реароматизация - Н+
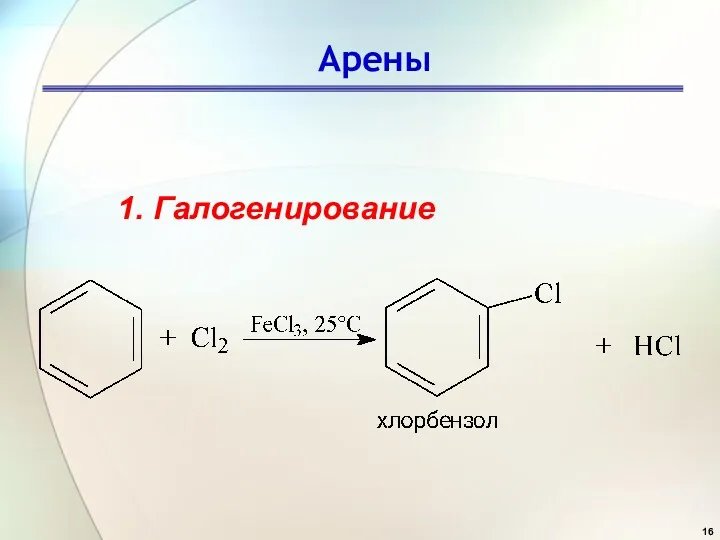
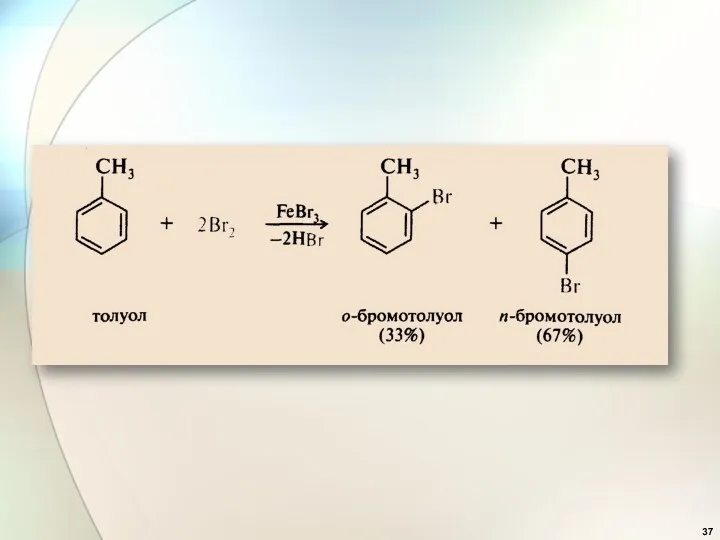
- 16. Арены 1. Галогенирование
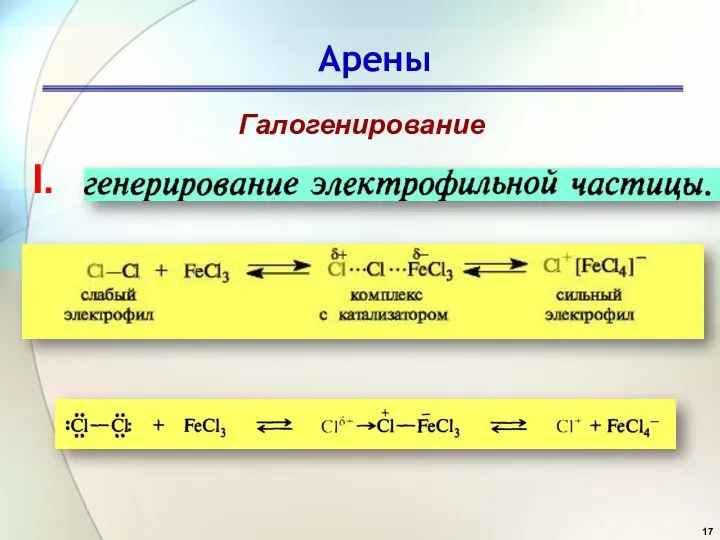
- 17. Арены Галогенирование I.
- 18. Для хлорирования в лабораторных условиях используют смесь HOCl с кислотой (хлор − газ!): Хлорноватистая кислота
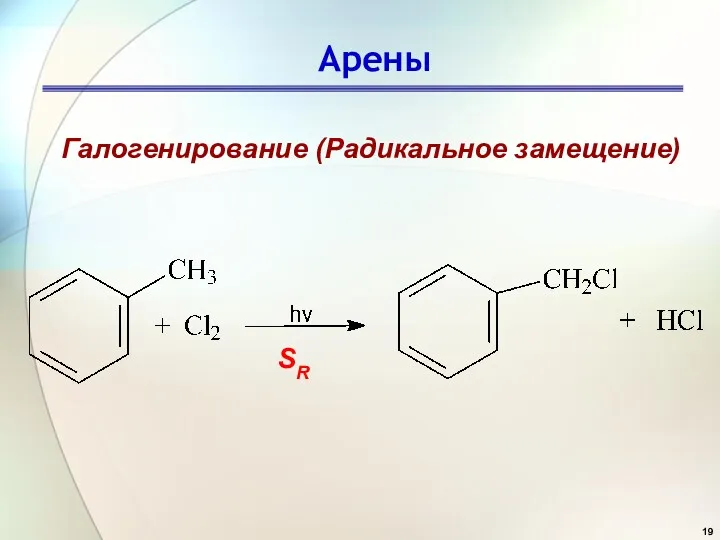
- 19. Арены Галогенирование (Радикальное замещение) SR
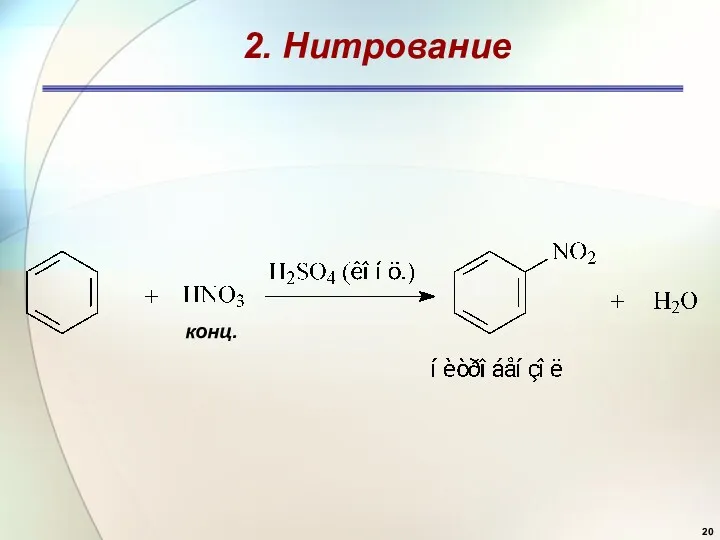
- 20. 2. Нитрование конц.
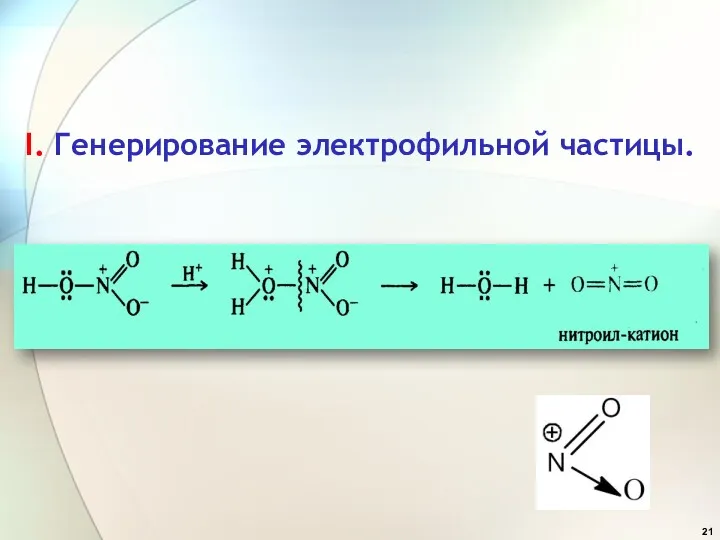
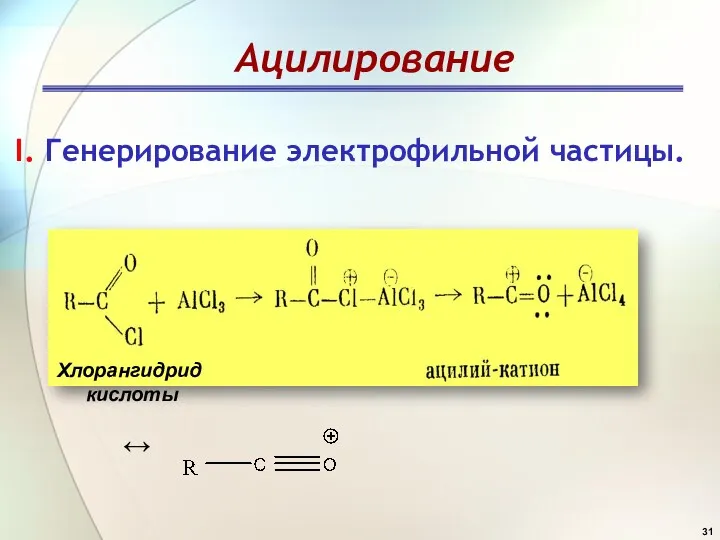
- 21. I. Генерирование электрофильной частицы.
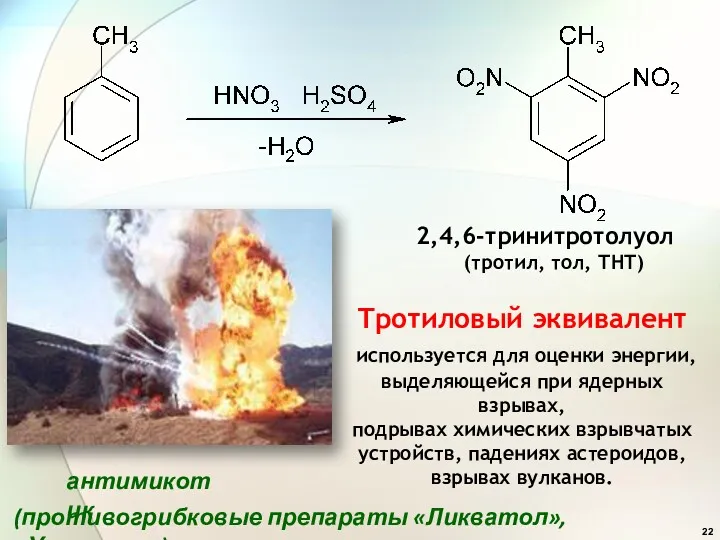
- 22. Тротиловый эквивалент используется для оценки энергии, выделяющейся при ядерных взрывах, подрывах химических взрывчатых устройств, падениях астероидов,
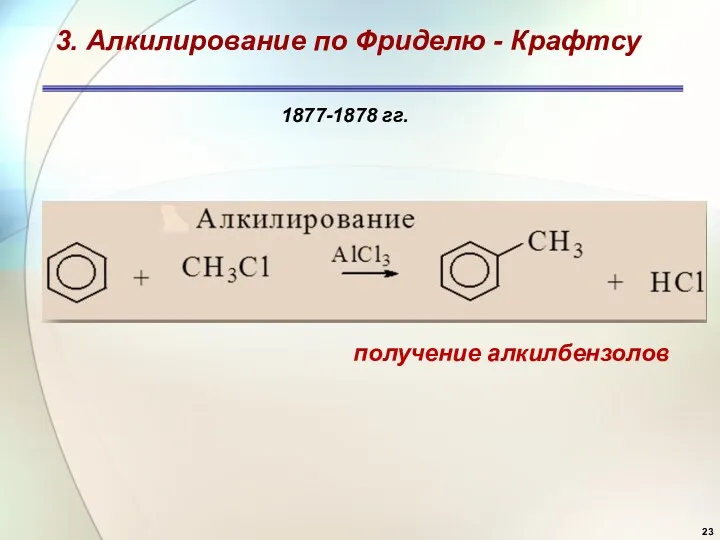
- 23. 3. Алкилирование по Фриделю - Крафтсу 1877-1878 гг. получение алкилбензолов
- 24. Реакция Фриделя—Крафтса Крафтс (Crafts) Джеймс Мейсон (8.3.1839 — 20.6.1917, США) Фридель (Friedel) Шарль (12.3.1832 — 20.4.1899,
- 25. + I. Генерирование электрофильной частицы.
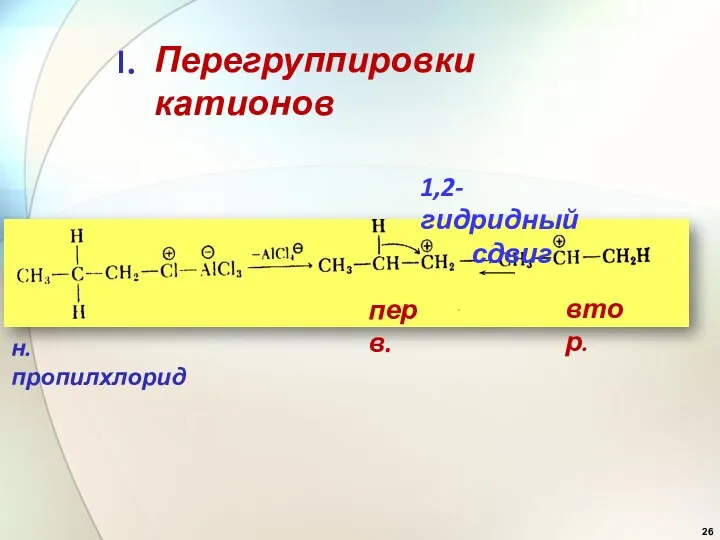
- 26. Перегруппировки катионов н.пропилхлорид I. перв. втор. 1,2-гидридный сдвиг
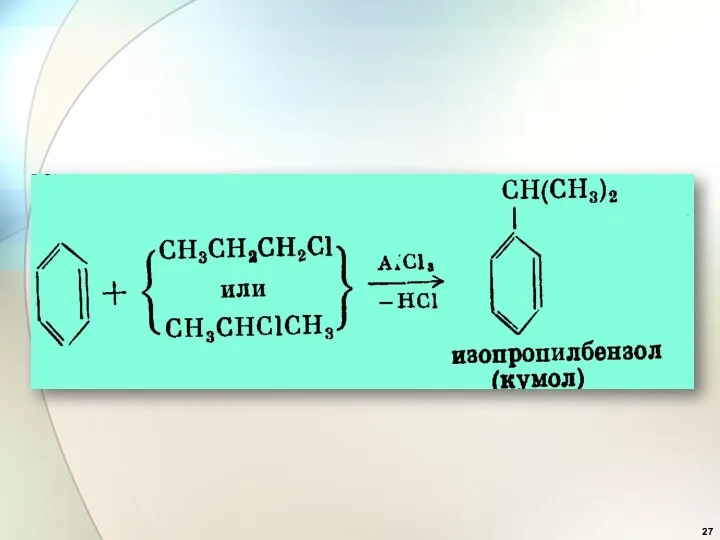
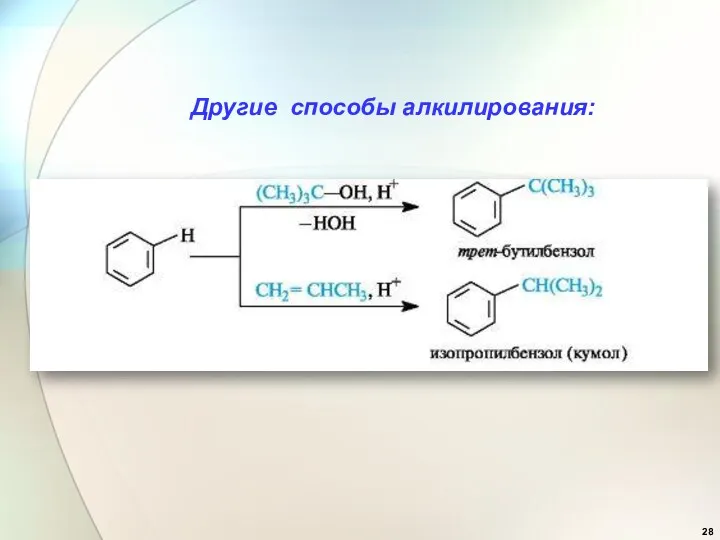
- 28. Другие способы алкилирования:
- 29. Полиалкилирование:
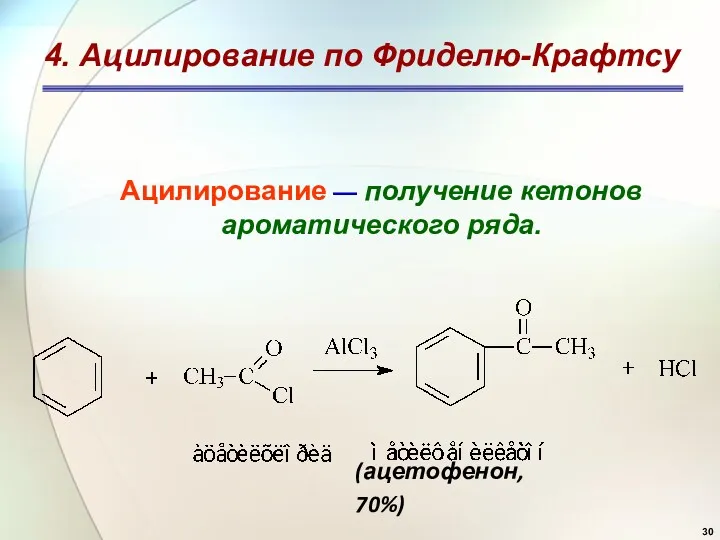
- 30. 4. Ацилирование по Фриделю-Крафтсу Ацилирование — получение кетонов ароматического ряда. (ацетофенон, 70%)
- 31. Ацилирование ↔ I. Генерирование электрофильной частицы. Хлорангидрид кислоты
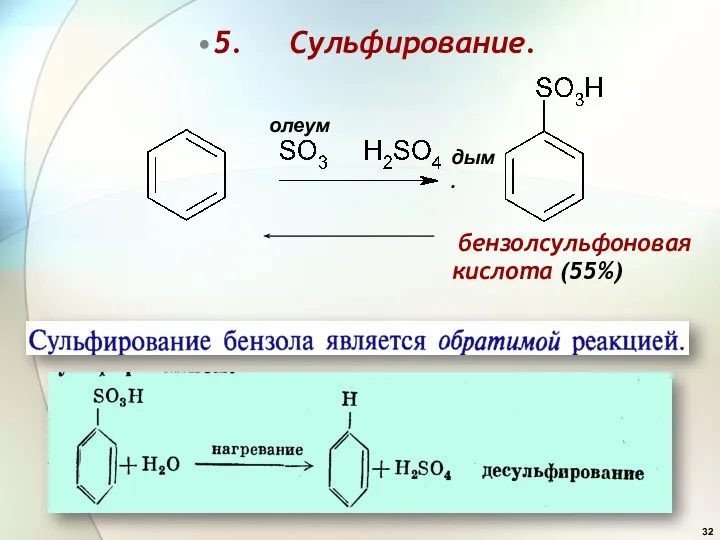
- 32. 5. Сульфирование. бензолсульфоновая кислота (55%) дым. олеум
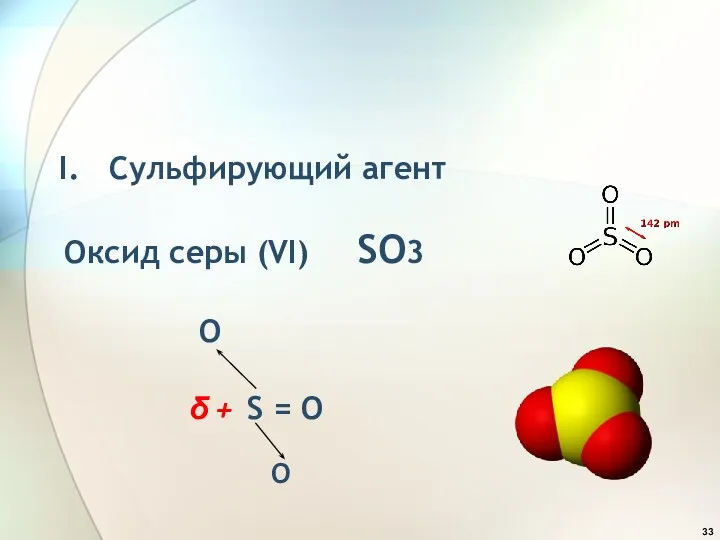
- 33. Сульфирующий агент Оксид серы (VI) SO3 O δ + S = O O
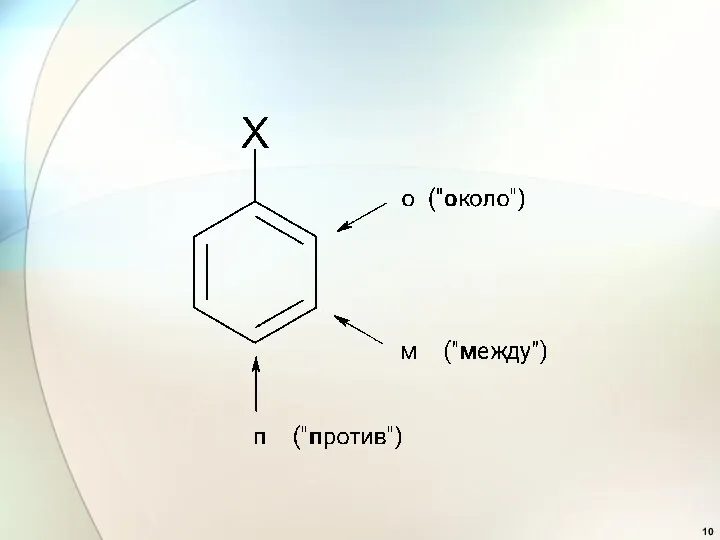
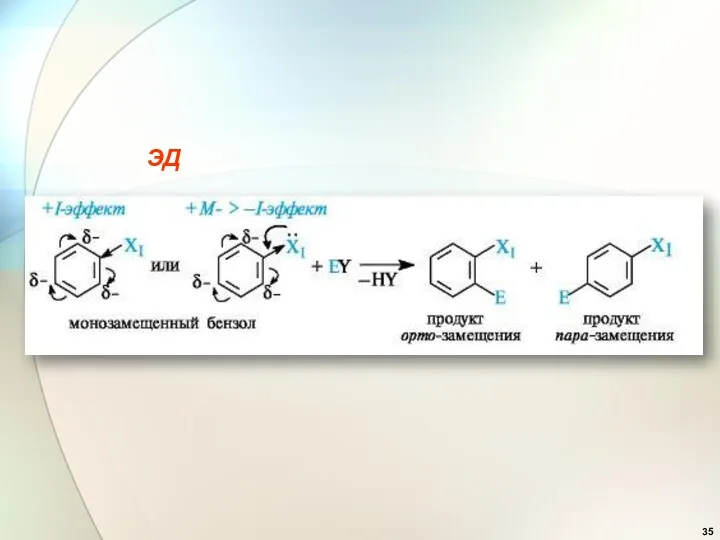
- 34. Ориентирующее действие заместителей в бензольном ядре.
- 35. ЭД
- 36. Эффекты заместителей при электрофильном замещении Заместители (ориентанты) первого рода (доноры): —ОН, —OR, —OCOR, —SH,- SR, —NH2,
- 38. 06.03.2015 фенол
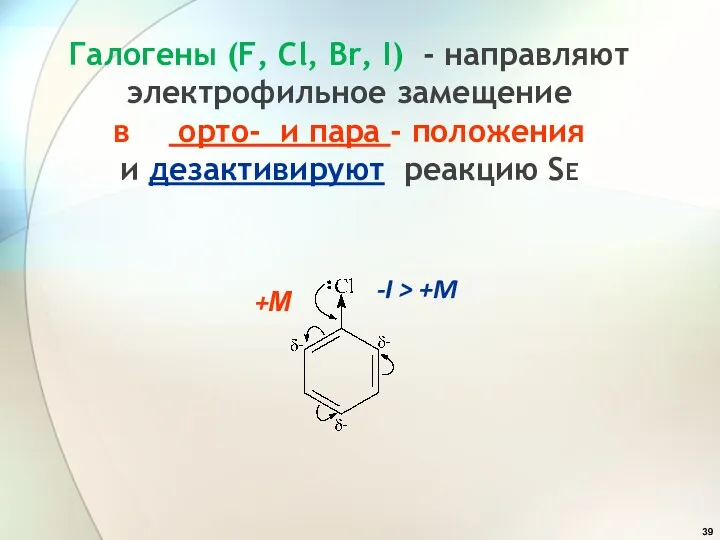
- 39. Галогены (F, Cl, Br, I) - направляют электрофильное замещение в орто- и пара - положения и
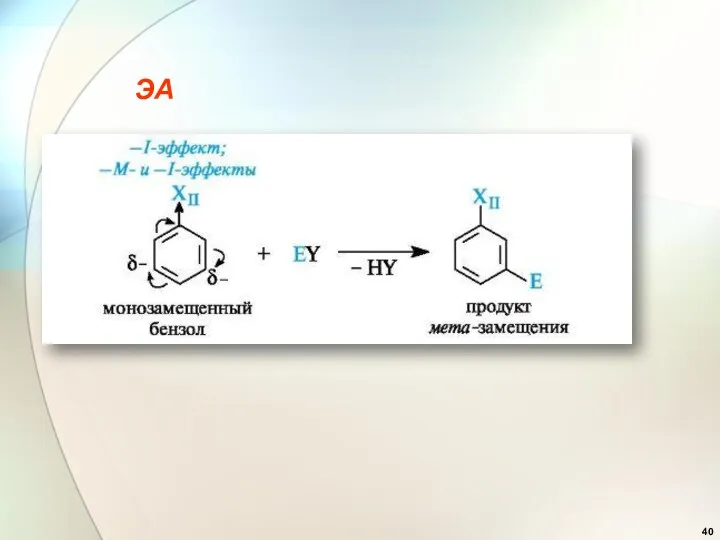
- 40. ЭА
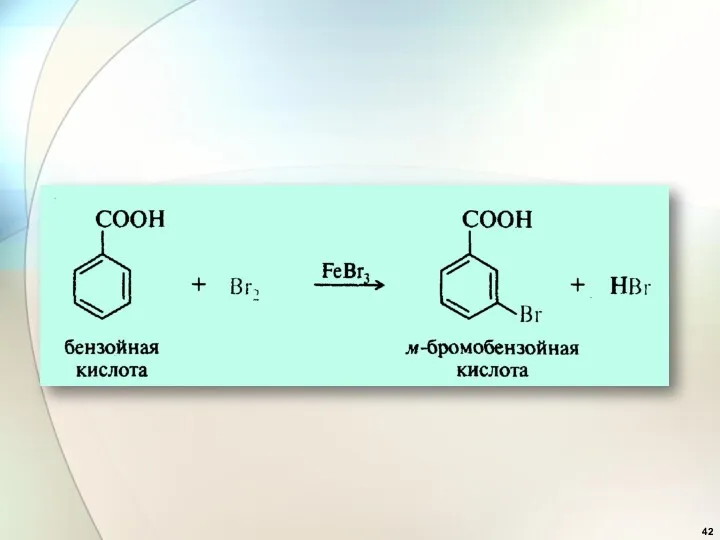
- 41. Эффекты заместителей при электрофильном замещении 2. Заместители (ориентанты) второго рода (акцепторы): —CN, —СООН, —SO3H, —СНО, —COR,
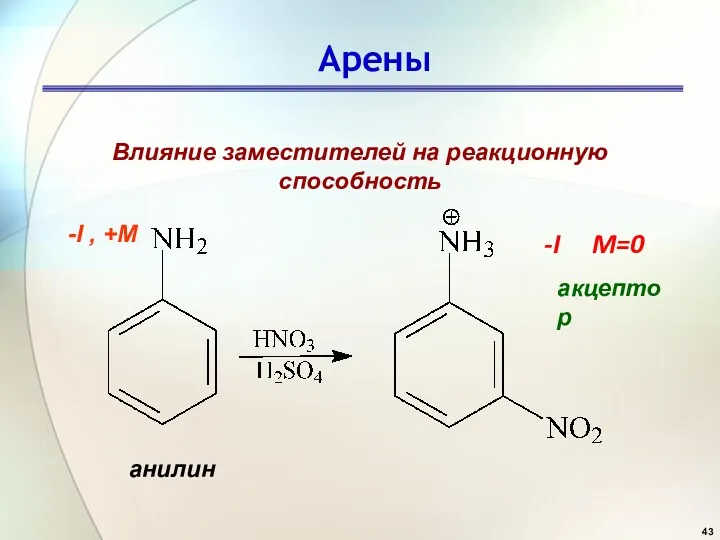
- 43. Арены Влияние заместителей на реакционную способность -I M=0 акцептор анилин -I , +M
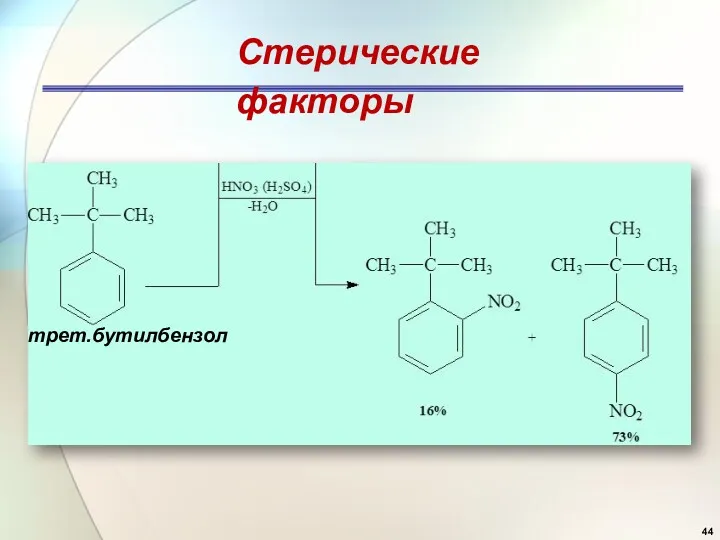
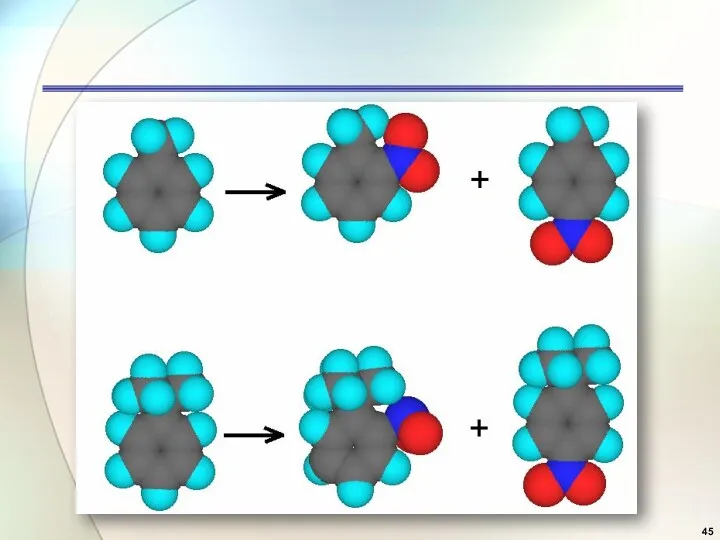
- 44. Стерические факторы трет.бутилбензол
- 46. Ориентация в бензольных кольцах, содержащих более одного заместителя Согласованная ориентация
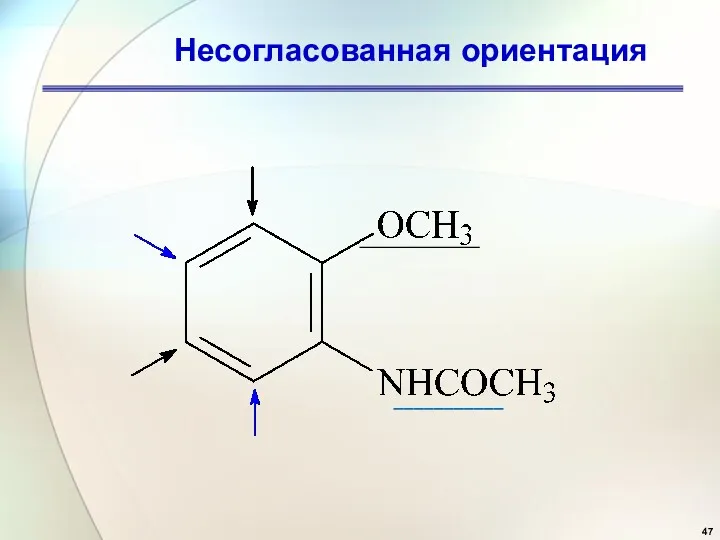
- 47. Несогласованная ориентация ___________
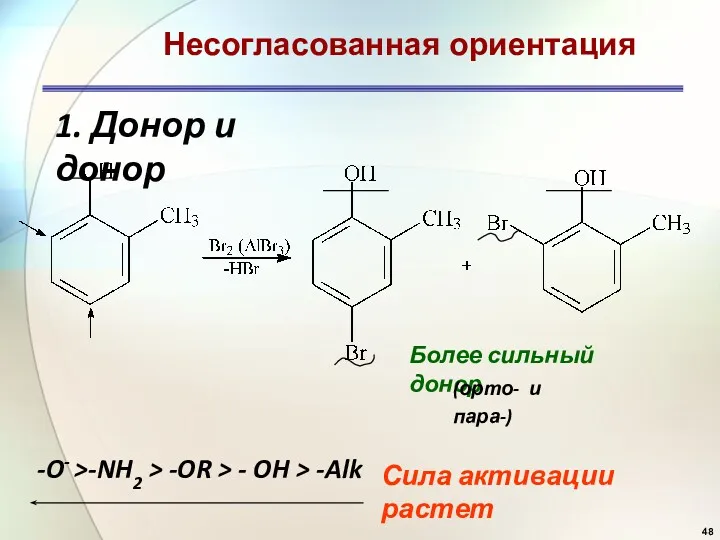
- 48. 1. Донор и донор Несогласованная ориентация Более сильный донор (орто- и пара-) -O- >-NH2 > -OR
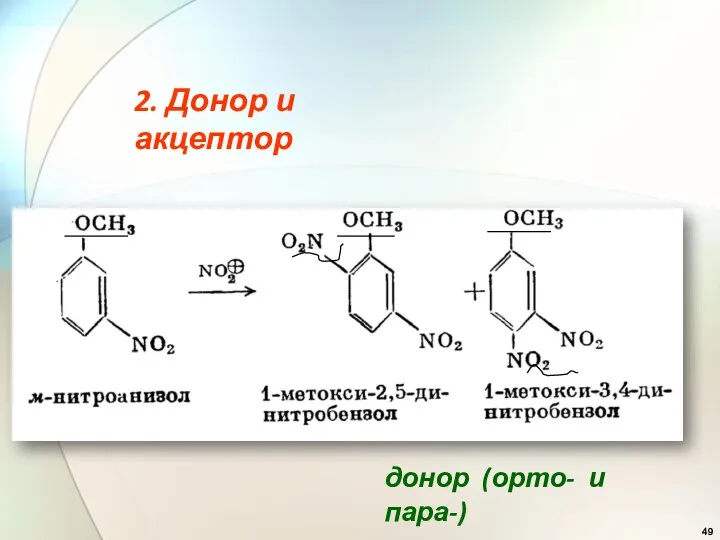
- 49. 2. Донор и акцептор донор (орто- и пара-)
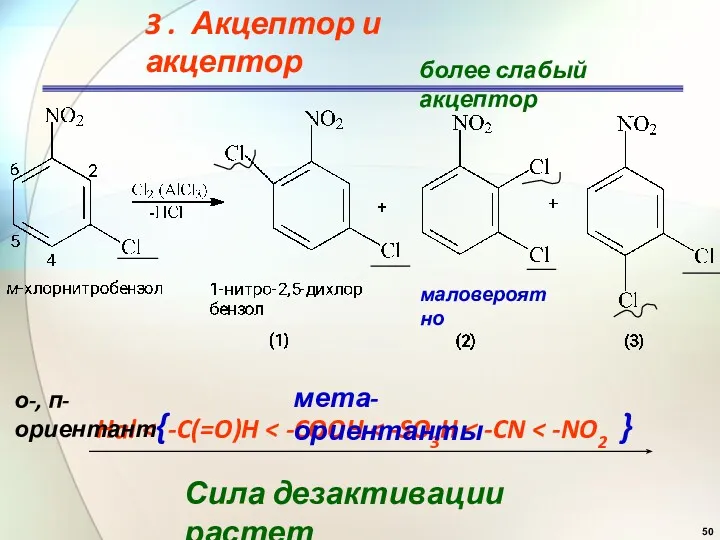
- 50. 3 . Акцептор и акцептор более слабый акцептор маловероятно Hal Сила дезактивации растет мета-ориентанты о-, п-ориентант
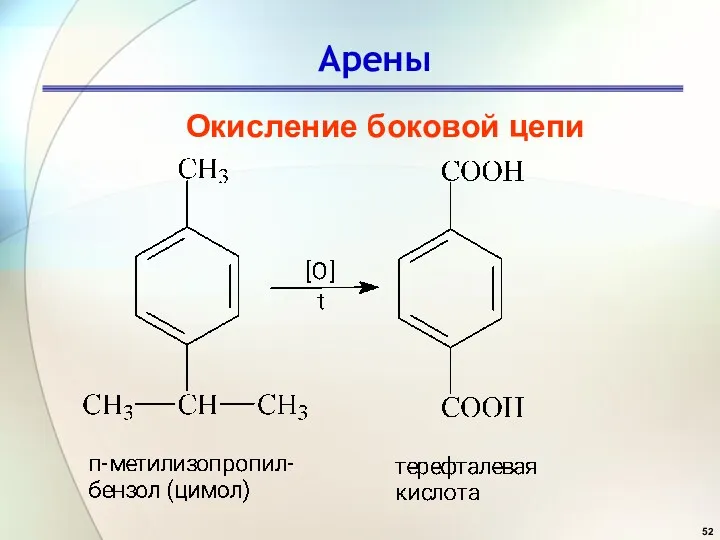
- 52. Арены Окисление боковой цепи
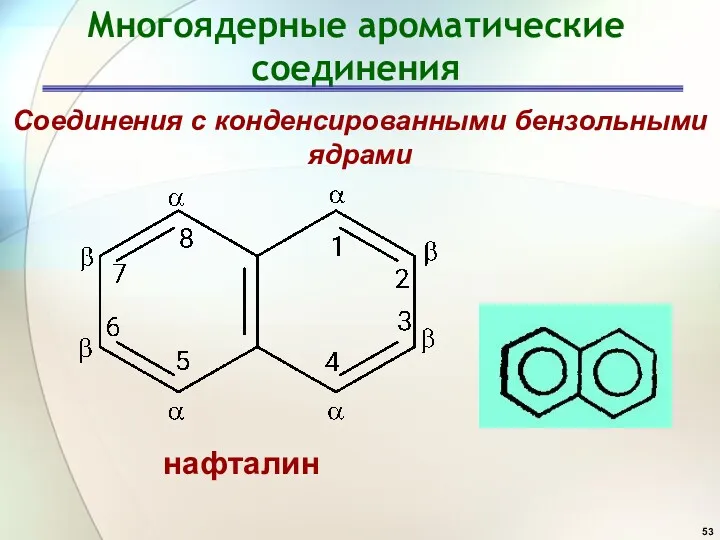
- 53. Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами нафталин
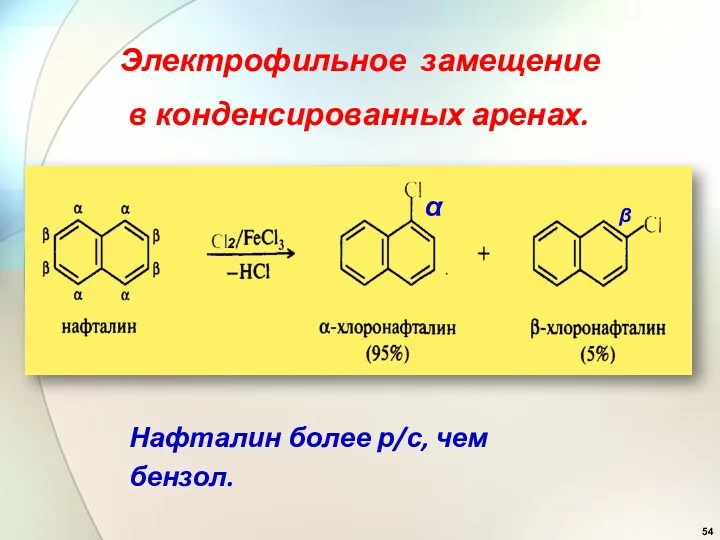
- 54. Электрофильное замещение в конденсированных аренах. Нафталин более р/с, чем бензол. α β 2
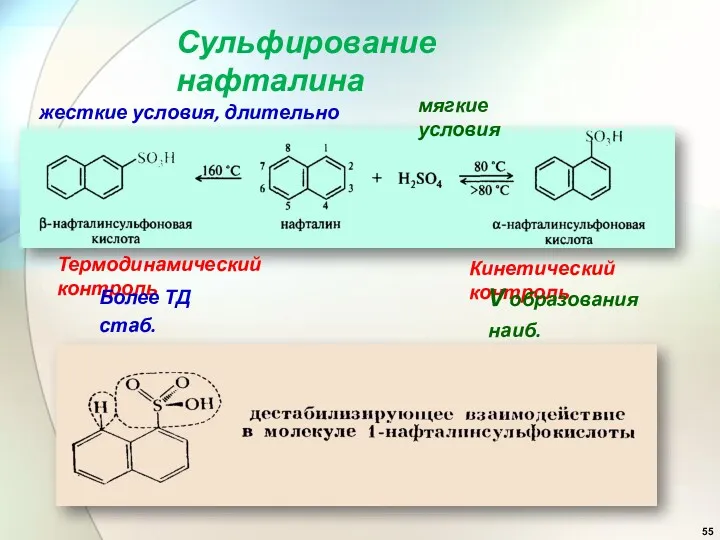
- 55. Кинетический контроль Термодинамический контроль мягкие условия жесткие условия, длительно V образования наиб. Более ТД стаб. Сульфирование
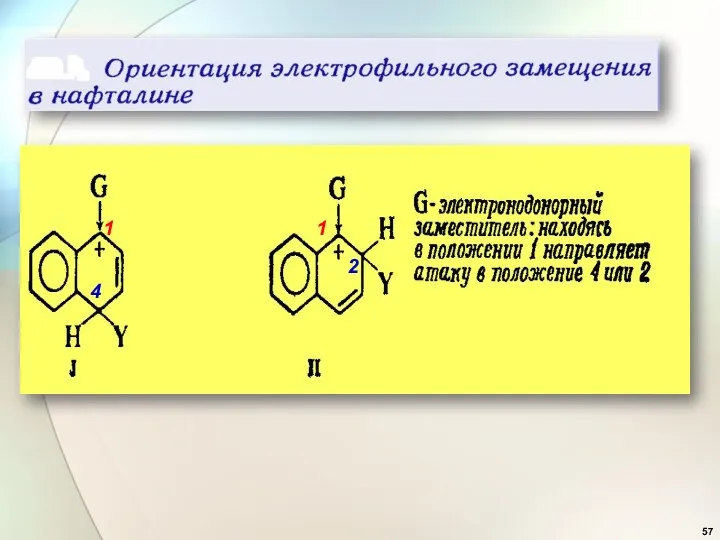
- 57. 4 2 1 1
- 58. 1 2
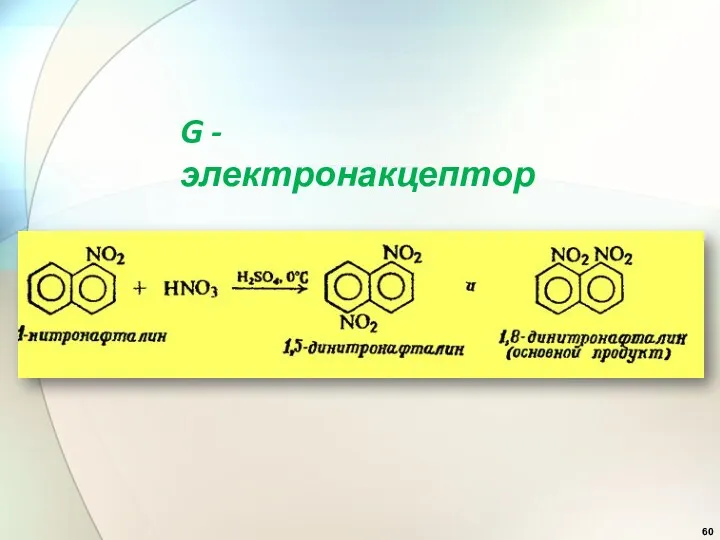
- 60. G - электронакцептор
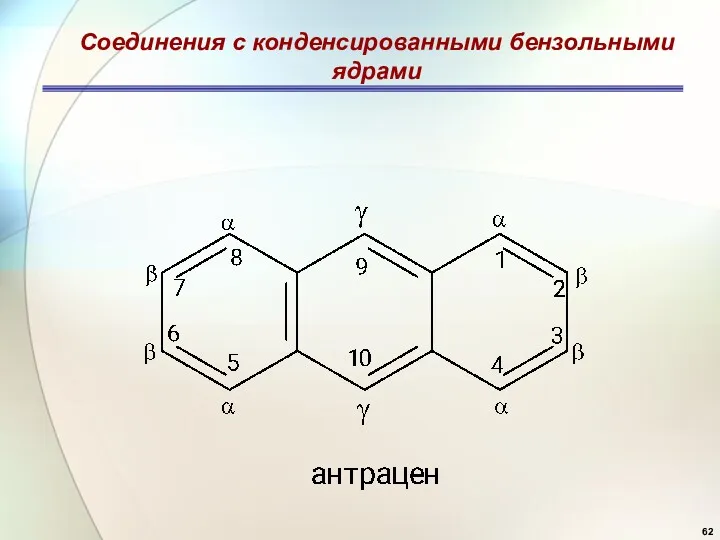
- 62. Соединения с конденсированными бензольными ядрами
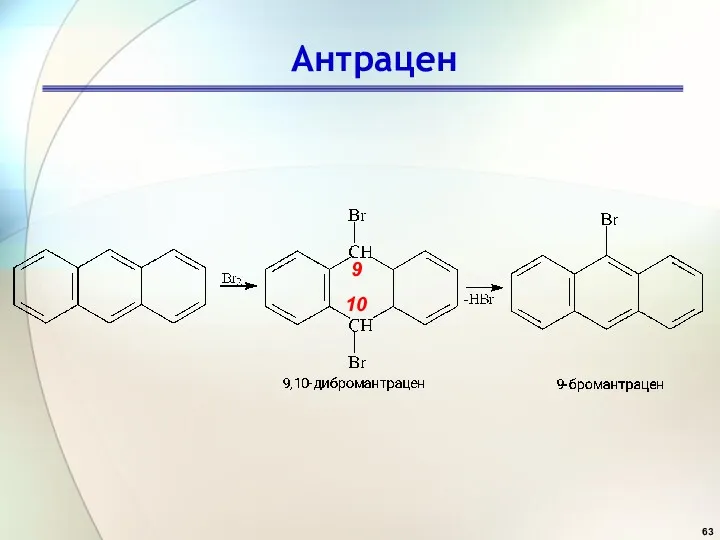
- 63. Антрацен 9 10
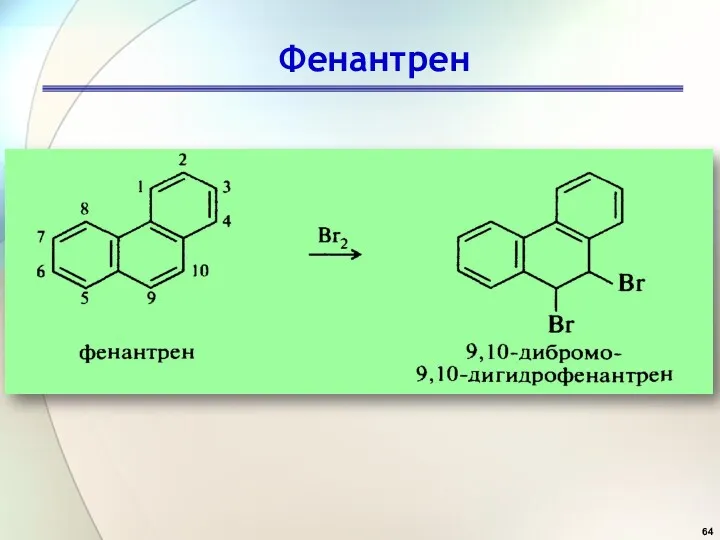
- 64. Фенантрен
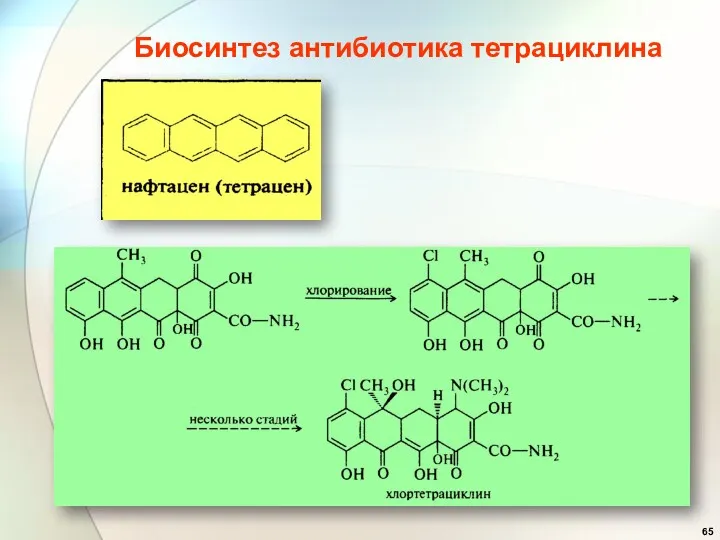
- 65. Биосинтез антибиотика тетрациклина
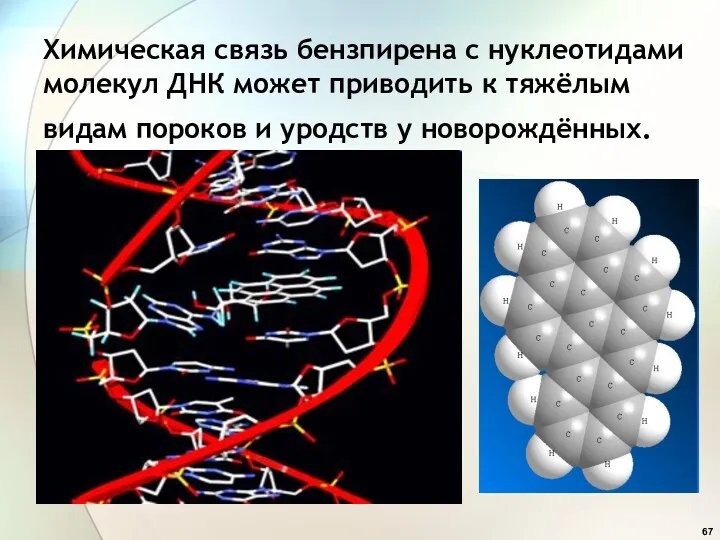
- 66. 06.03.2015 Физические и биологические свойства аренов. Бензпирен – мощный канцероген!
- 67. Химическая связь бензпирена с нуклеотидами молекул ДНК может приводить к тяжёлым видам пороков и уродств у
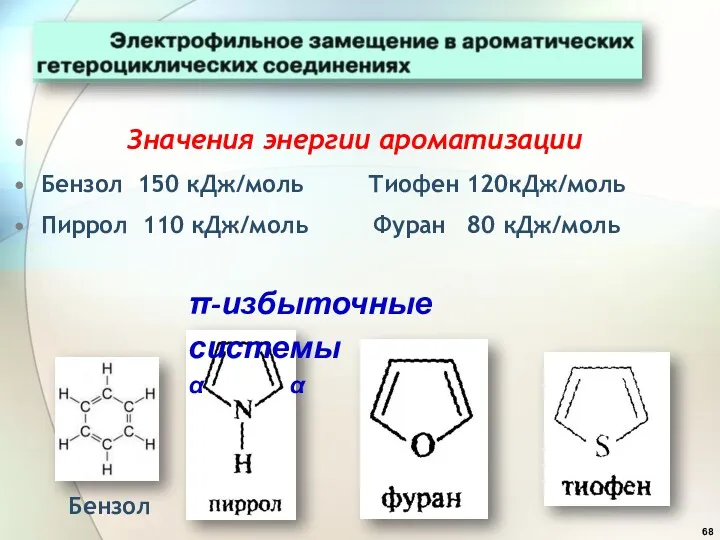
- 68. Значения энергии ароматизации Бензол 150 кДж/моль Тиофен 120кДж/моль Пиррол 110 кДж/моль Фуран 80 кДж/моль π-избыточные системы
- 69. Ацидофобность – нестабильность в сильнокислой среде пиррольных и фурановых ядер.
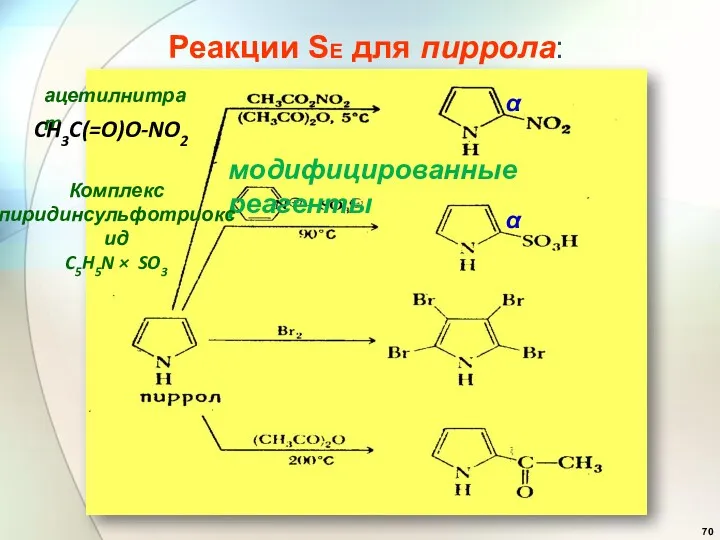
- 70. Реакции SE для пиррола: модифицированные реагенты α ацетилнитрат CH3C(=O)O-NO2 α Комплекс пиридинсульфотриоксид C5H5N × SO3
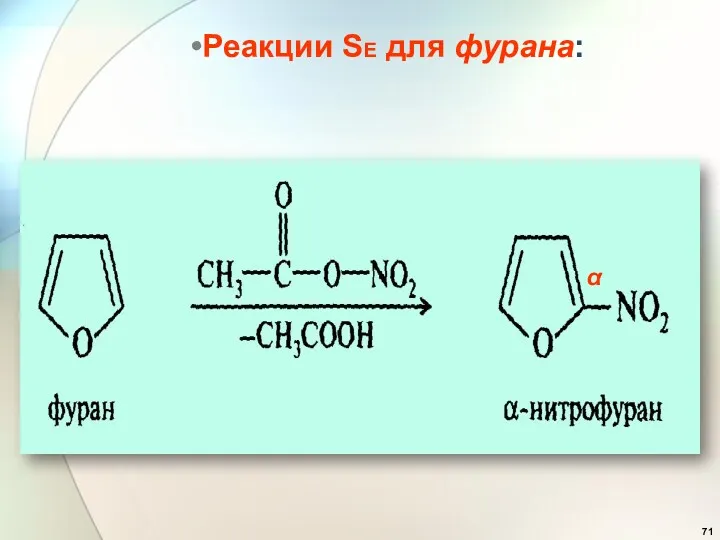
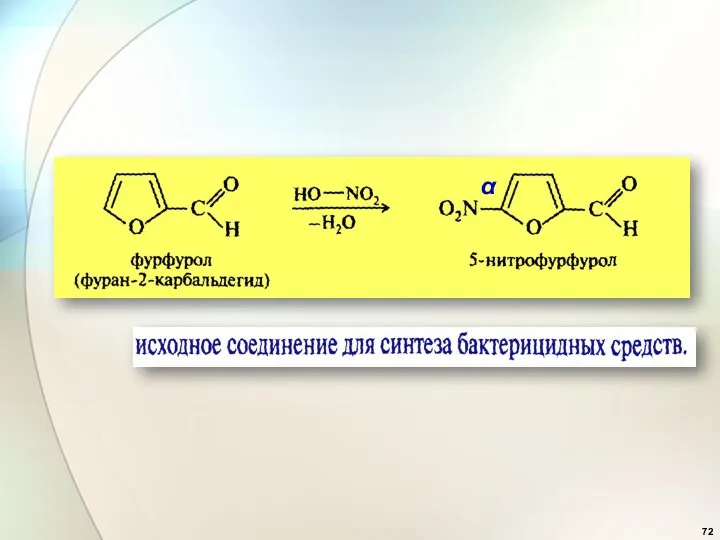
- 71. Реакции SE для фурана: α α
- 72. α
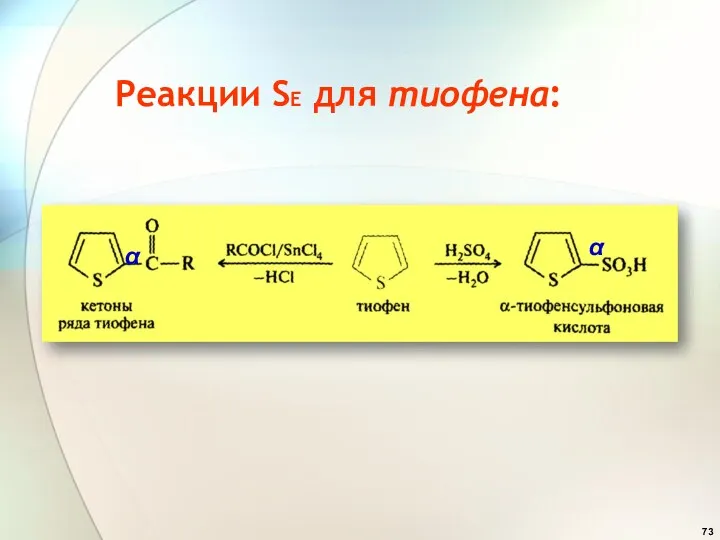
- 73. Реакции SE для тиофена: α α
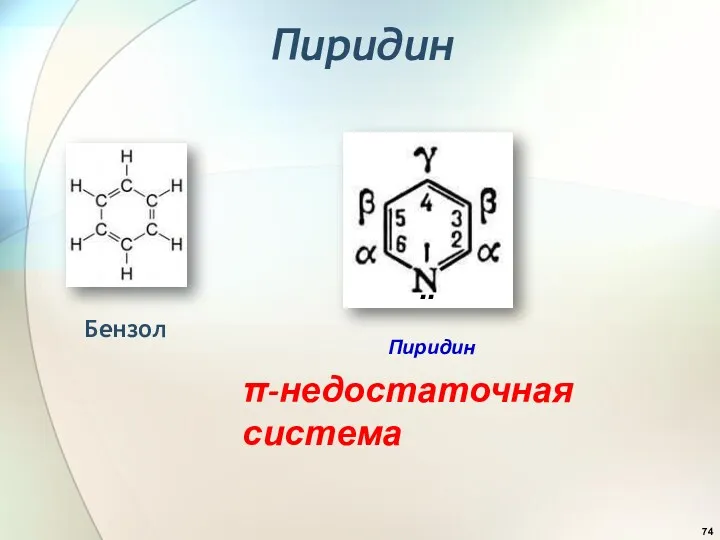
- 74. Пиридин π-недостаточная система Бензол .. Пиридин
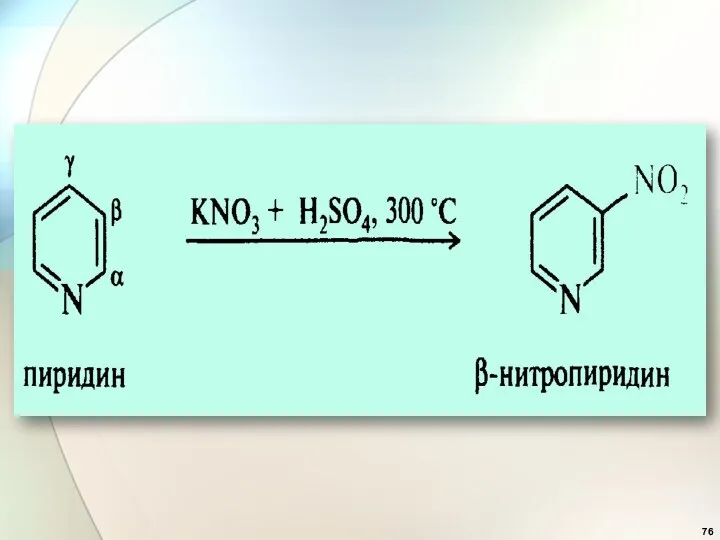
- 75. Реакции SE у пиридина β β β катион пиридиния катион пиридиния
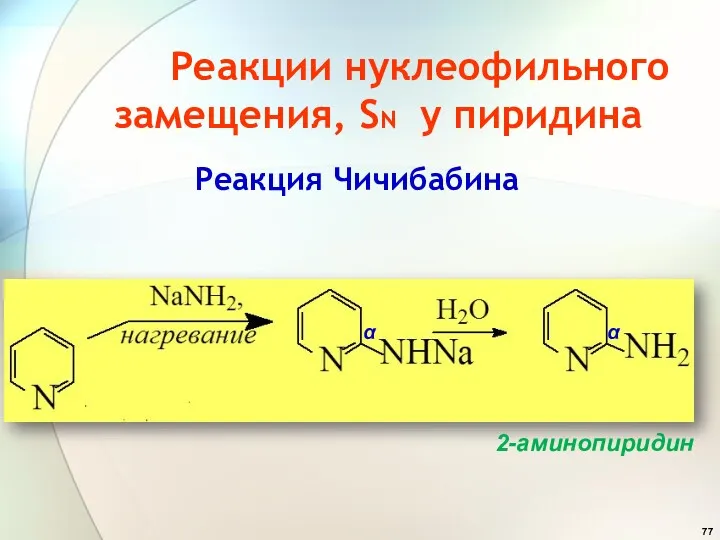
- 77. Реакции нуклеофильного замещения, SN у пиридина Реакция Чичибабина α α 2-аминопиридин
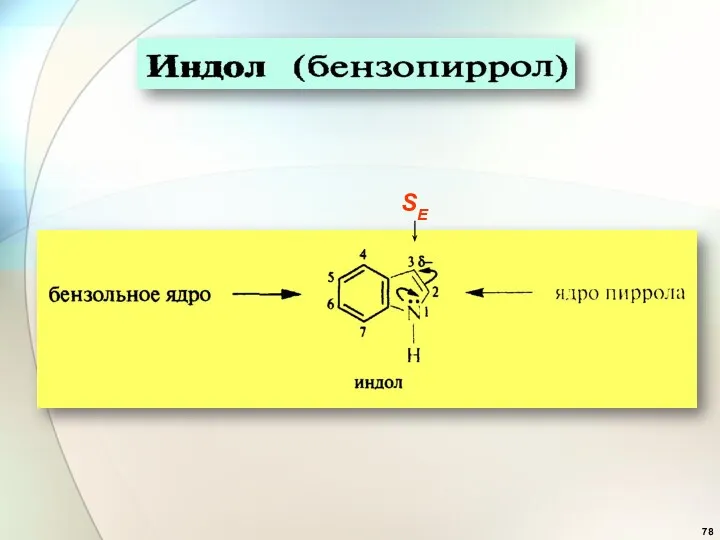
- 78. SE
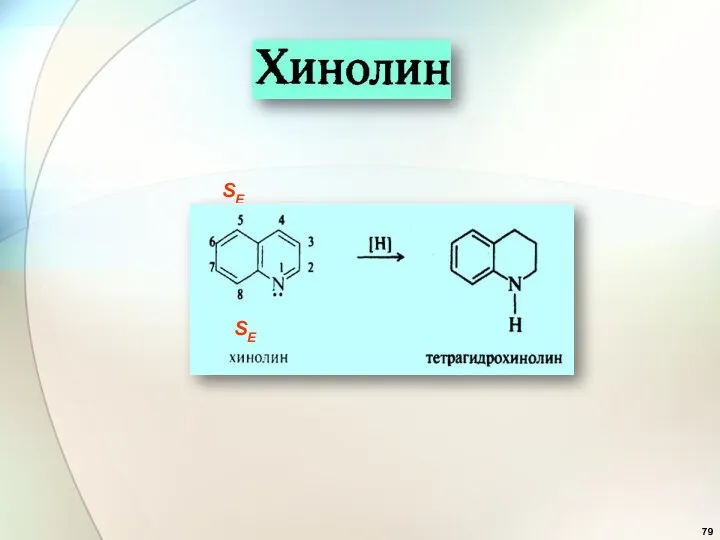
- 79. SE SE SE
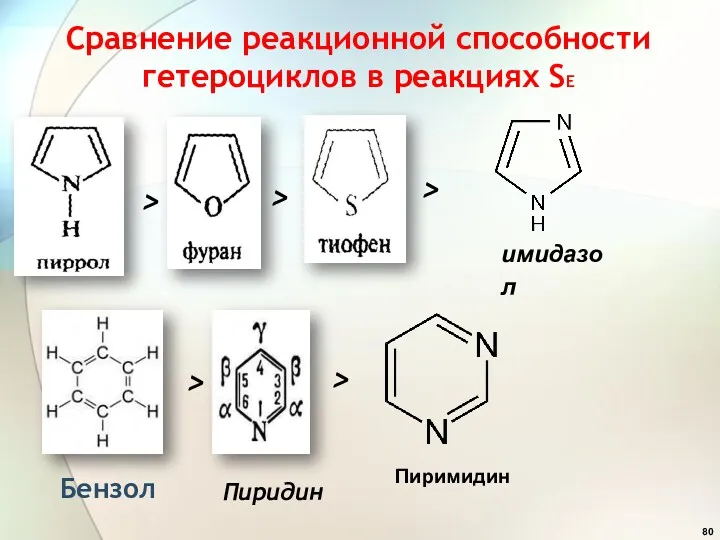
- 80. Сравнение реакционной способности гетероциклов в реакциях SE Бензол Пиридин Пиримидин > > > > > имидазол
- 81. 06.03.2015 Спасибо за Ваше внимание!
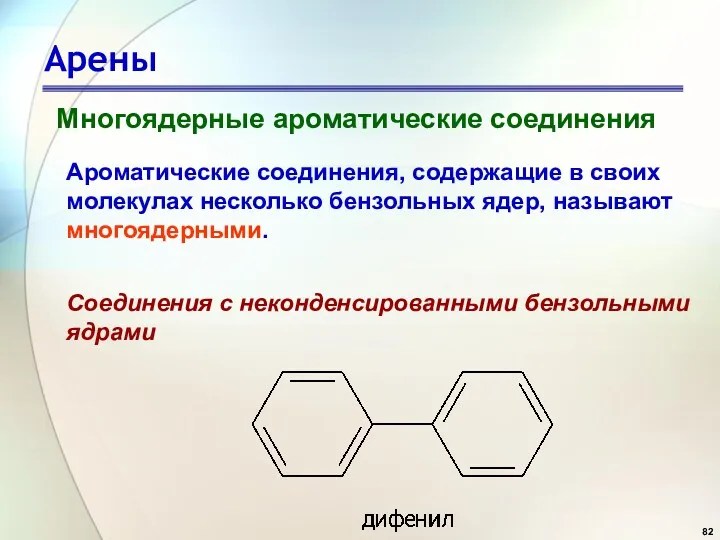
- 82. Арены Многоядерные ароматические соединения Ароматические соединения, содержащие в своих молекулах несколько бензольных ядер, называют многоядерными. Соединения
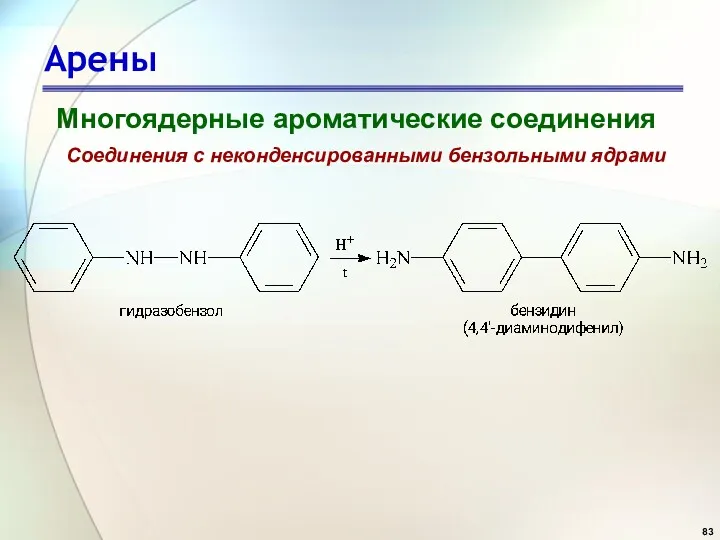
- 83. Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами
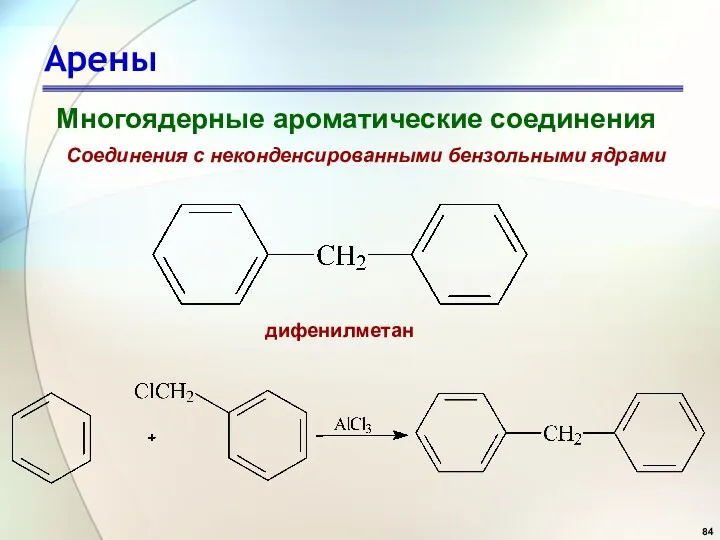
- 84. Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами дифенилметан
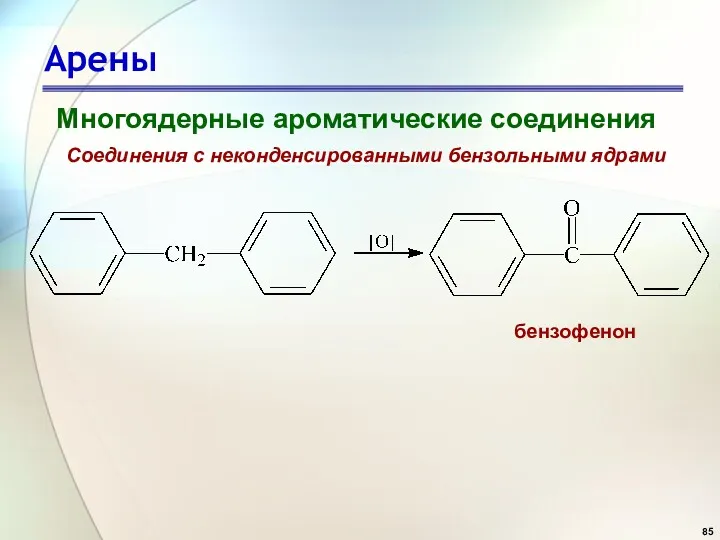
- 85. Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами бензофенон
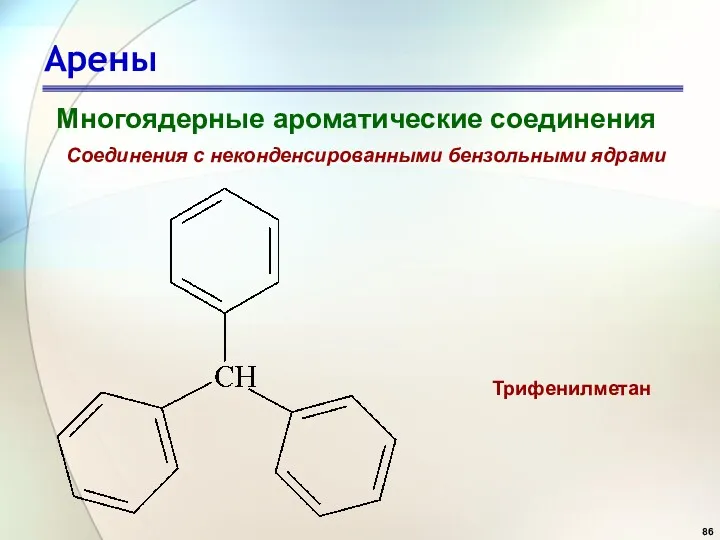
- 86. Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами Трифенилметан
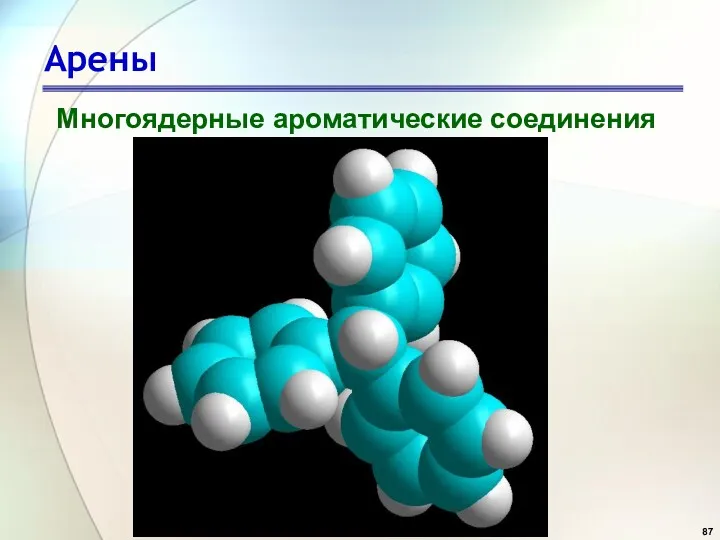
- 87. Арены Многоядерные ароматические соединения
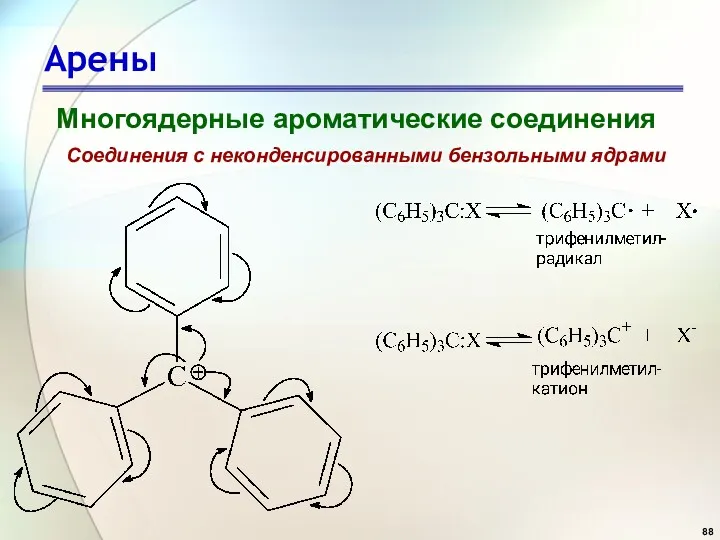
- 88. Арены Многоядерные ароматические соединения Соединения с неконденсированными бензольными ядрами
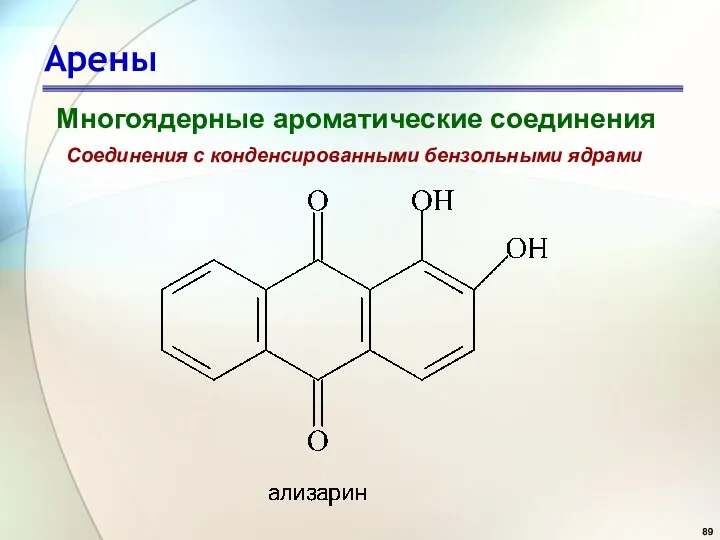
- 89. Арены Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами
- 90. Арены Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами а) Линейно конденсированные циклы: тетрацен пентацен гексацен
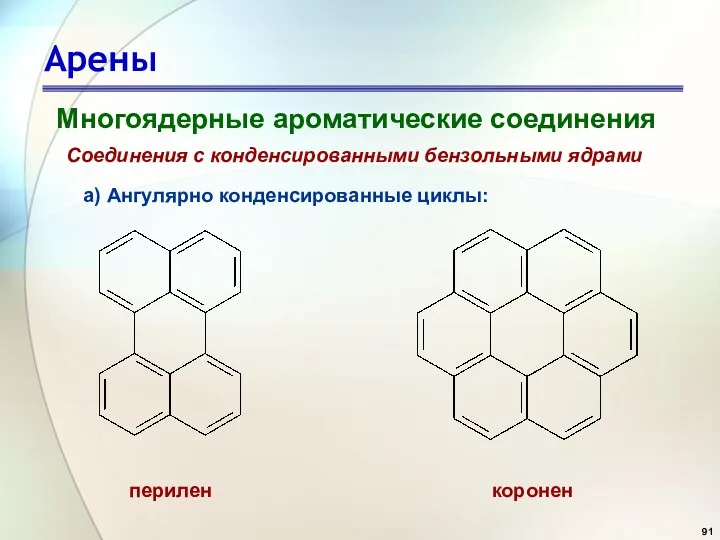
- 91. Арены Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами а) Ангулярно конденсированные циклы: перилен коронен
- 92. Арены Многоядерные ароматические соединения Соединения с конденсированными бензольными ядрами а) Ангулярно конденсированные циклы:
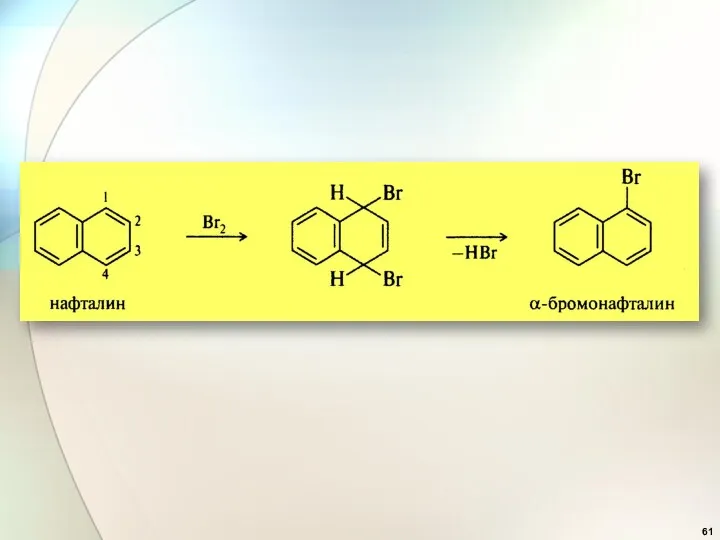
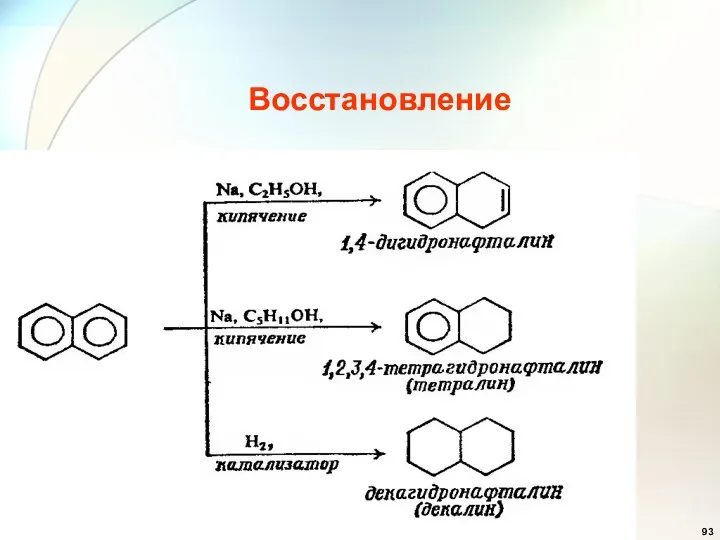
- 93. Восстановление
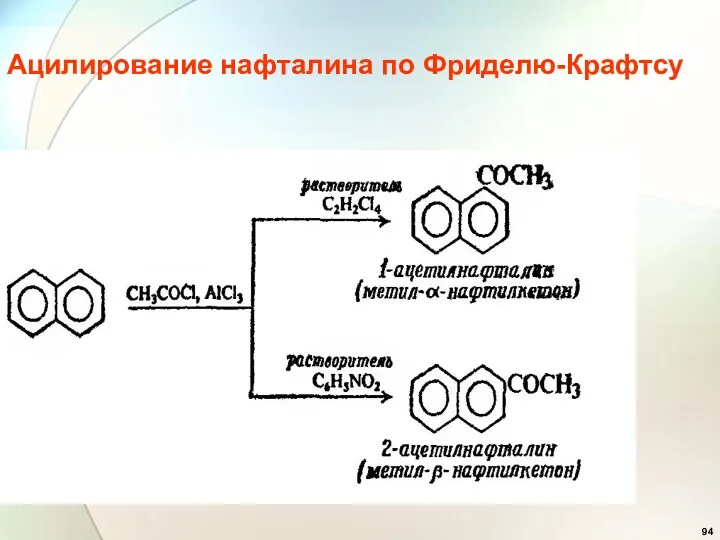
- 94. Ацилирование нафталина по Фриделю-Крафтсу
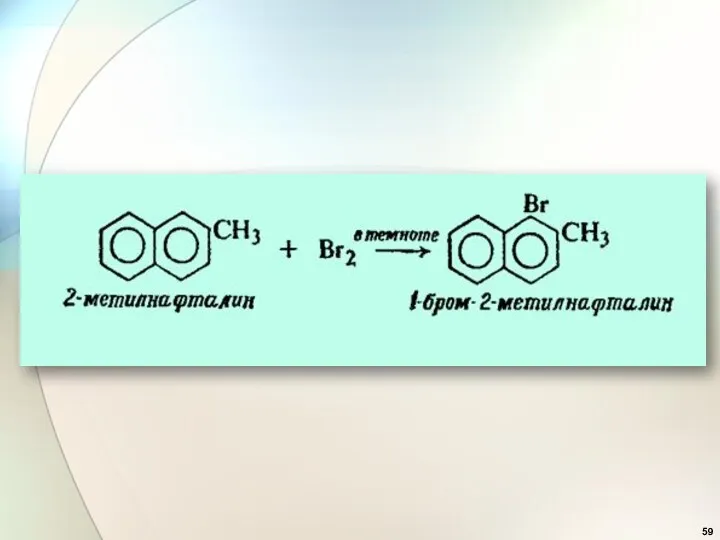
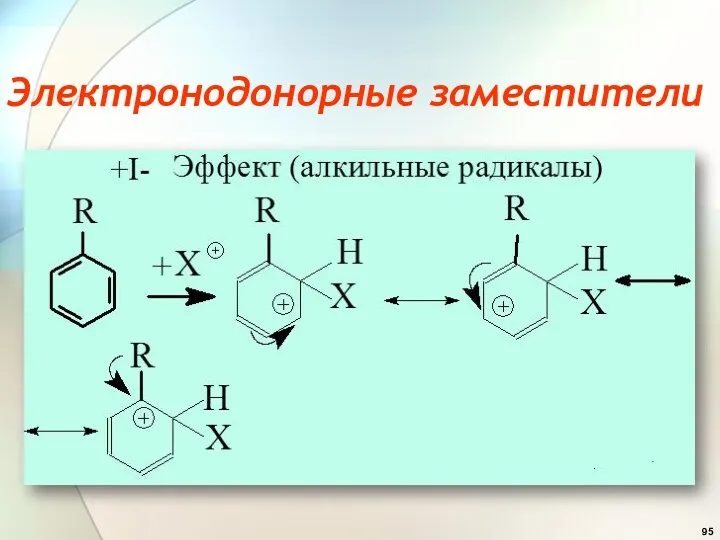
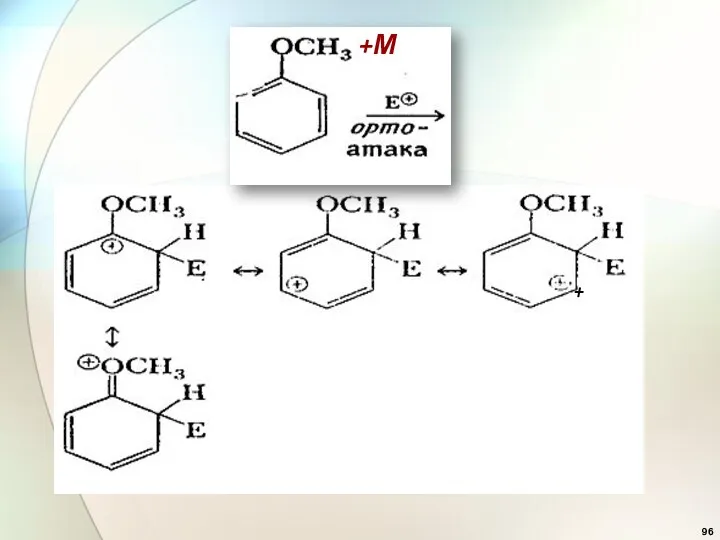
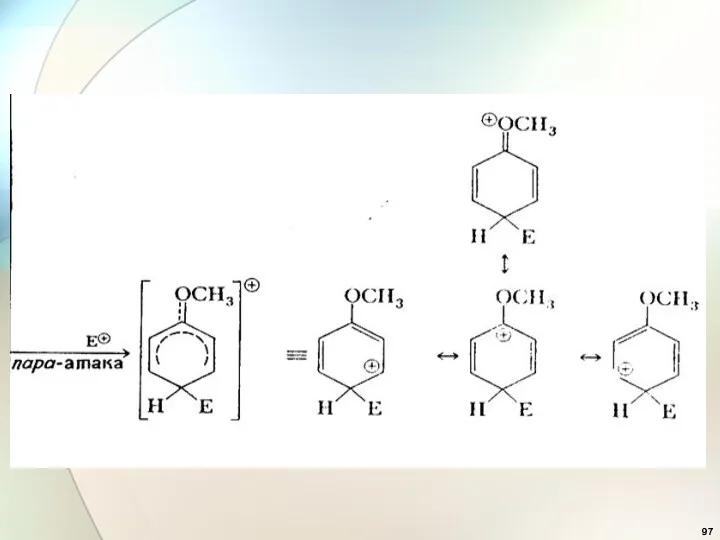
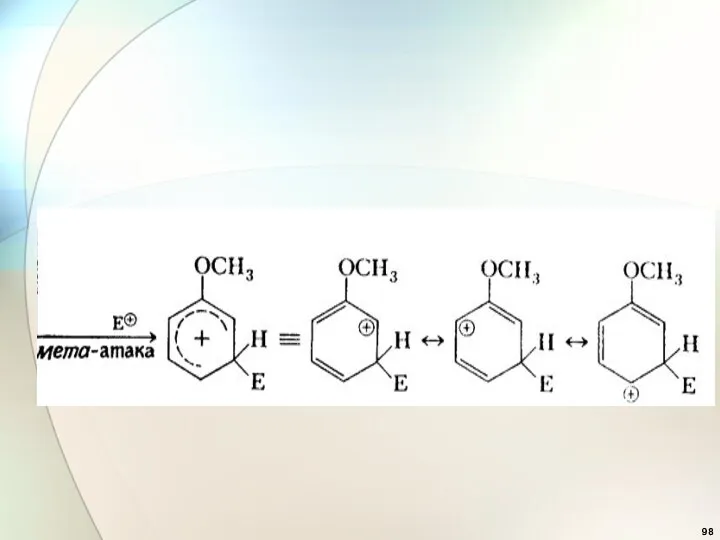
- 95. Электронодонорные заместители
- 96. + +М
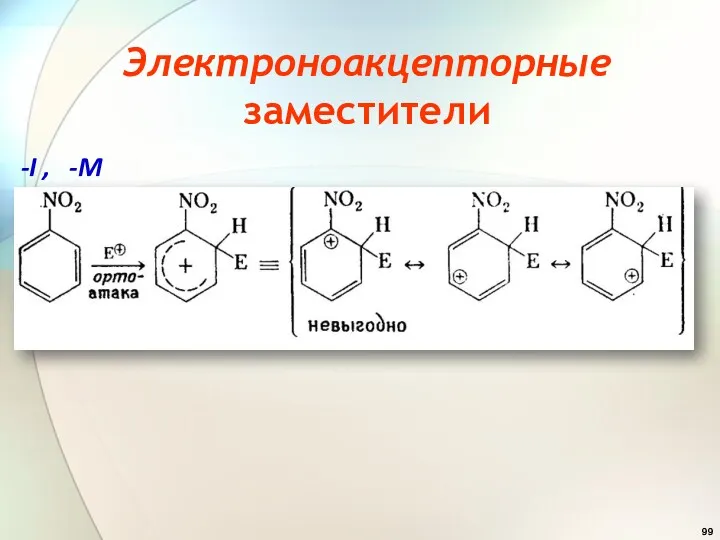
- 99. Электроноакцепторные заместители -I , -M
- 102. Скачать презентацию


















 Амины. Понятие об аминах. Анилин как органическое основание
Амины. Понятие об аминах. Анилин как органическое основание Cұйықтықтардағы электр тоғы
Cұйықтықтардағы электр тоғы Художественная обработка камня
Художественная обработка камня Фуллерендер құрылымдары және олардың түрлерi
Фуллерендер құрылымдары және олардың түрлерi Основы химической термодинамики и кинетики химических реакций
Основы химической термодинамики и кинетики химических реакций Реакции ионного обмена
Реакции ионного обмена Химическая кинетика
Химическая кинетика Основные понятия и законы химии
Основные понятия и законы химии Тағамның стериндері мен талшықтық құрамы
Тағамның стериндері мен талшықтық құрамы Предмет химии. Вещества
Предмет химии. Вещества Каучук и резина
Каучук и резина Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений
Особенности строения, реакционной способности и методы синтеза гидроксилсодержащих соединений Гидролиз солей
Гидролиз солей Природный газ и нефть
Природный газ и нефть Химия p-элементов
Химия p-элементов Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Комплексономертиялық титрлеу. Дәріс № 6
Комплексономертиялық титрлеу. Дәріс № 6 Игра Самый умный. Химия
Игра Самый умный. Химия Синтетикалық пиретроидтар. Инсектицидтердің тиомочевиндер, нейтротоксиндер, гормоналды, авермектиндер, карбаматтар
Синтетикалық пиретроидтар. Инсектицидтердің тиомочевиндер, нейтротоксиндер, гормоналды, авермектиндер, карбаматтар Введение в токсикологическую химию. Объекты химико-токсикологического исследования
Введение в токсикологическую химию. Объекты химико-токсикологического исследования Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Aqueous Solutions of Electrolytes
Aqueous Solutions of Electrolytes Основные классы неорганических соединений
Основные классы неорганических соединений Хімічні формули речовин
Хімічні формули речовин Общие классификации смазочных материалов
Общие классификации смазочных материалов Гидролиз неорганических солей
Гидролиз неорганических солей Химический элемент алюминий
Химический элемент алюминий Каменный уголь
Каменный уголь