Содержание
- 2. процесс более энергетически выгодный, чем электролиз расплавов при электролизе как на аноде, так и на катоде
- 3. Ряд напряжений металлов Li K Rb Ba Ca Na Mg Al| Mn Zn Cr Fe Cd
- 4. Li K Rb Ba Ca Na Mg Al | Mn Zn Cr Fe Cd Co Ni
- 5. Анодные процессы ПРОЦЕССЫ НА АНОДЕ: с растворимым анодом с нерастворимым анодом (поведение кислородсодержащих и бескислородных кислотных
- 6. Растворимый анод Электролиз растворов солей с анодом (Cu, Zn, Fe, Ag и др.): - не зависит
- 7. Нерастворимый анод Конкурирующие процессы при электролизе с инертным анодом (графит, платина) – два окислительных и восстановительных
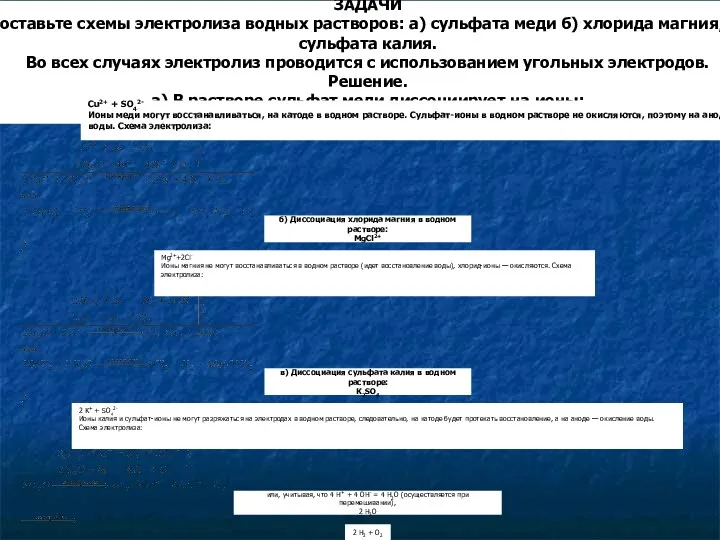
- 8. Пример 1. Разряжается анион соли и вода: а) электролиз раствора NaCl: К(-): 2H2O + 2e →
- 9. Пример 2. Разряжаются катион и анион соли: электролиз раствора CuCl2: К(-): Cu2+ + 2e → Cu0
- 10. Пример 3. Разряжаются катион соли и вода: а) электролиз раствора ZnSO4 К(-): Zn2+ + 2e →
- 11. Пример 4. Разряжается только вода: Электролиз раствора Na2SO4, KNO3 К(-): 2H2O + 2e→ H2 + 2OH-
- 12. Электролиз расплавов ХАРАКТЕРИСТИКА: энергетически ёмкий (электролиты плавятся при очень высоких температурах); при плавлении разрушаются кристаллические решётки;
- 13. Примеры электролиза расплавов NaCl K(-): Na ++ 1e → Na0 A(+): 2Cl- - 2e → Cl2
- 14. Применение электролиза получение щелочей, хлора, водорода, алюминия, магния, натрия, кадмия очистка металлов (меди, никеля, свинца) защита
- 15. ЗАДАЧА Электролиз 400 г 8,5%-ного раствора нитрата серебра продолжали до тех пор, пока масса раствора не
- 16. При электролизе образовавшегося раствора азотной кислоты разлагается вода: 2 H2O = 2 Н2↑ + O2↑. Потеря
- 17. Зависимость количества вещества, образовавшегося при электролизе, от времени и силы тока описывается: m = (Э /
- 20. Скачать презентацию
















 Карбоновые кислоты. Тест
Карбоновые кислоты. Тест Кремний и его соединения
Кремний и его соединения Водородная связь
Водородная связь Природные источники углеводородов, их переработка, применение и экологические проблемы
Природные источники углеводородов, их переработка, применение и экологические проблемы Металлы и их свойства. Способы получения
Металлы и их свойства. Способы получения Органическая химия. Вещества
Органическая химия. Вещества Магматизм. (Лекция 6)
Магматизм. (Лекция 6) Кислород
Кислород Спроби класифікації хімічних елементів
Спроби класифікації хімічних елементів Алкены (олефины, этиленовые углеводороды)
Алкены (олефины, этиленовые углеводороды) Прочность полимеров
Прочность полимеров Амфотерные органические и неорганические соединения
Амфотерные органические и неорганические соединения Буферные растворы
Буферные растворы Місце хімії серед наук про природу
Місце хімії серед наук про природу Химические волокна
Химические волокна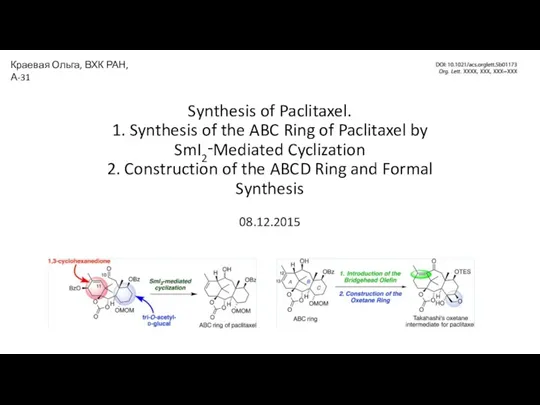 Synthesis of Paclitaxel
Synthesis of Paclitaxel Строение атома. 8 класс
Строение атома. 8 класс Лекция 3. Разновидности химических связей
Лекция 3. Разновидности химических связей Витамины. Ашылу тарихы
Витамины. Ашылу тарихы ГИА-9 Химия. А4
ГИА-9 Химия. А4 Массовая и объемная доли компонентов смеси (раствора)
Массовая и объемная доли компонентов смеси (раствора) Классификация органических соединений, углеводородов
Классификация органических соединений, углеводородов Рідкі кристали
Рідкі кристали Спирты
Спирты Химические уравнения
Химические уравнения Вещества молекулярного и немолекулярного строения
Вещества молекулярного и немолекулярного строения Применение алюминия и его сплава в машиностроении
Применение алюминия и его сплава в машиностроении Химическая связь. 8 класс
Химическая связь. 8 класс