1. Образование слоистых соединений
Слоистые соединения образуются за счет внедрения атомов и
молекул в межслоевое пространство. Атомы реагента могут быть связаны с атомами углерода ковалентными, координационными или ионными связями. В зависимости от типа связи слоистое соединение может сохранять электропроводность исходного графита или терять ее.
Непроводящие слоистые соединения с sp3-гибридными связями
Плоские слои изгибаются, π-электронное облако исчезает, электропроводность теряется
Получают при обработке графита смесью HNO3 и H2SO4, дымящей H2SO4 или др. сильными окислителями
Сn окис-ль СnOmHx (оксид графита)
Получают при обработке графита прямым воздействием газообразного F2:
Сn + 1/2F2 (СF)n (фторид графита)
2. Электропроводящие слоистые соединения с sp2-гибридными связями
Атомы включаются между слоями углеродных атомов без разрушения плоской системы. Металлоценовые соединения получаются нагреванием графита в присутствии Ме.
















 Тепловой эффект химических реакций
Тепловой эффект химических реакций Крохмаль. Структурна формула крохмалю
Крохмаль. Структурна формула крохмалю Сполуки неметалічних елементів з гідрогеном. Амоніак та хлороводень
Сполуки неметалічних елементів з гідрогеном. Амоніак та хлороводень Анализ качества лекарственных веществ, определяемых методом комплексонометрии
Анализ качества лекарственных веществ, определяемых методом комплексонометрии Электрохимические накопители энергии
Электрохимические накопители энергии Пластмаси та їх роль у сучасному виробництві
Пластмаси та їх роль у сучасному виробництві Химическое равновесие. Принцип Ле Шателье
Химическое равновесие. Принцип Ле Шателье Периодический закон и периодическая система Д.И. Менделеева
Периодический закон и периодическая система Д.И. Менделеева Дослідження методів очищення висококольорових поверхневих вод
Дослідження методів очищення висококольорових поверхневих вод Белки. 9 класс
Белки. 9 класс Химические свойства соляной кислоты
Химические свойства соляной кислоты Исследование снежного покрова
Исследование снежного покрова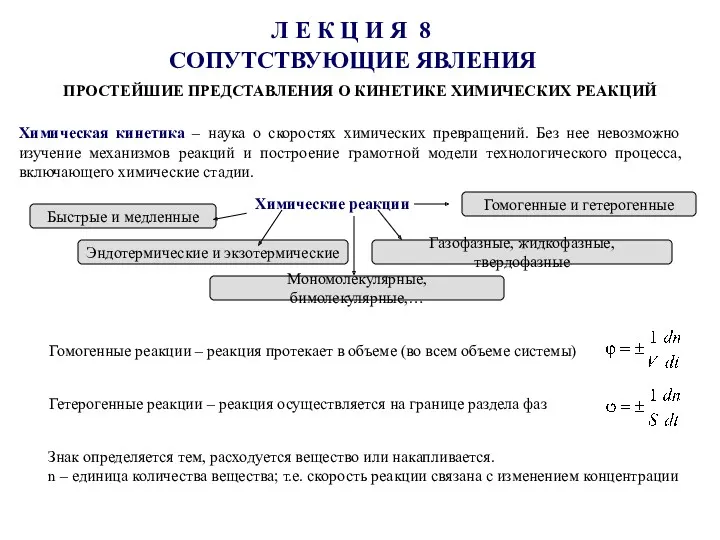 Простейшие представления о кинетике химических реакций
Простейшие представления о кинетике химических реакций Строение атома
Строение атома Азотная кислота и ее свойства
Азотная кислота и ее свойства Физические и химические явления. Условия течения и признаки химических реакций
Физические и химические явления. Условия течения и признаки химических реакций Plastic is one of the challenges of the 21st century
Plastic is one of the challenges of the 21st century Методы исследования взаимодействий с участием белков (Co-IP, equilibrium microdialysis, ITC, MST, SPR, BLI, QСM)
Методы исследования взаимодействий с участием белков (Co-IP, equilibrium microdialysis, ITC, MST, SPR, BLI, QСM) Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Взаємодія води з кислотними оксидами
Взаємодія води з кислотними оксидами Ароматические углеводороды. Процессы производства. Направления использования
Ароматические углеводороды. Процессы производства. Направления использования Мұнай эмульсиясының құрамы және фаза аралық беттерінің құрылымы. Эмульсия инверсиясы
Мұнай эмульсиясының құрамы және фаза аралық беттерінің құрылымы. Эмульсия инверсиясы Платиновые металлы
Платиновые металлы Химия 20 века
Химия 20 века Карбонатна кислота. Солі карбонатної кислоти, їх поширення та застосування
Карбонатна кислота. Солі карбонатної кислоти, їх поширення та застосування Относительная атомная масса. Знаки химических элементов
Относительная атомная масса. Знаки химических элементов Контрольная работа. Разбор. 9 класс
Контрольная работа. Разбор. 9 класс Классы органических соединений
Классы органических соединений