Содержание
- 2. В химии при письме вместо названий используют формулы веществ. Как вы думаете, почему?
- 3. Формулы веществ записывать быстрее, они занимают мало место и несут много информации. Наша задача сегодня –
- 4. Химическая формула - это условная запись состава вещества с помощью химических знаков и индексов
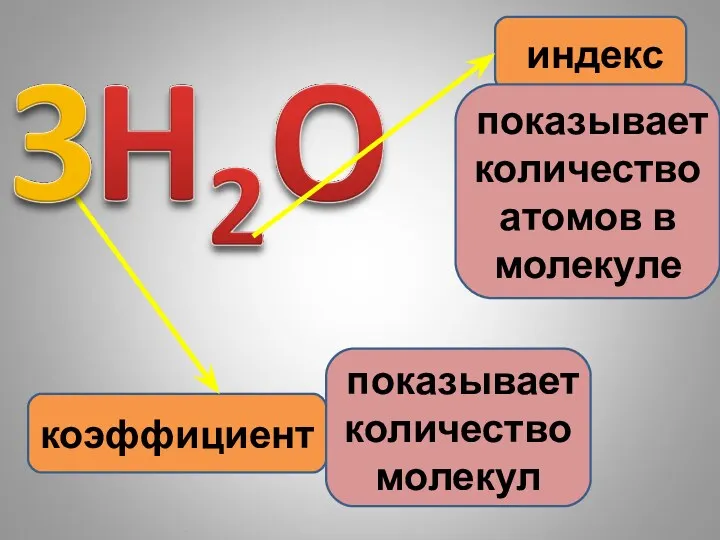
- 5. химические знаки индекс показывает количество атомов в молекуле
- 6. Информация, которую содержат химические формулы: 1) 1 молекула
- 7. 1) 1 молекула Как быть, если нам нужно указать не одну молекулу, а несколько: 2, 3
- 8. коэффициент индекс показывает количество атомов в молекуле показывает количество молекул
- 9. 1. В записи 5SO3 коэффициент равен: б) 15; в) 3; г) коэффициент отсутствует. 2. В записи
- 10. 3. В записи СO2коэффициент равен: б) 3; в) 2; г) коэффициент отсутствует. а) 1; 3. В
- 11. Информация, которую содержат химические формулы: 1) 1 молекула 2) Название вещества 3) Качественный состав
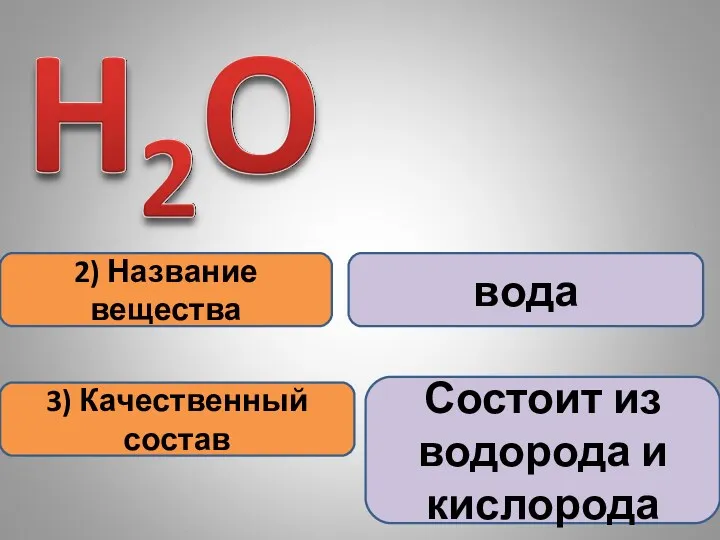
- 12. 2) Название вещества 3) Качественный состав вода Состоит из водорода и кислорода
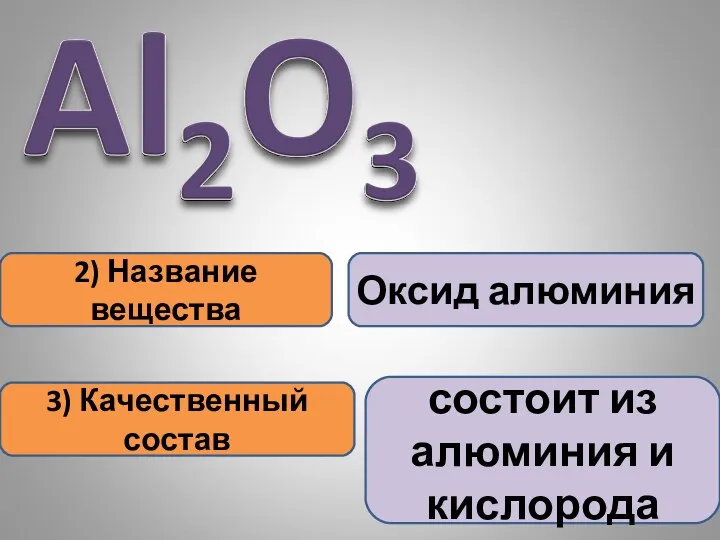
- 13. 2) Название вещества 3) Качественный состав Оксид алюминия состоит из алюминия и кислорода
- 14. Информация, которую содержат химические формулы: 1) 1 молекула 2) Название вещества 3) Качественный состав 4) Количественный
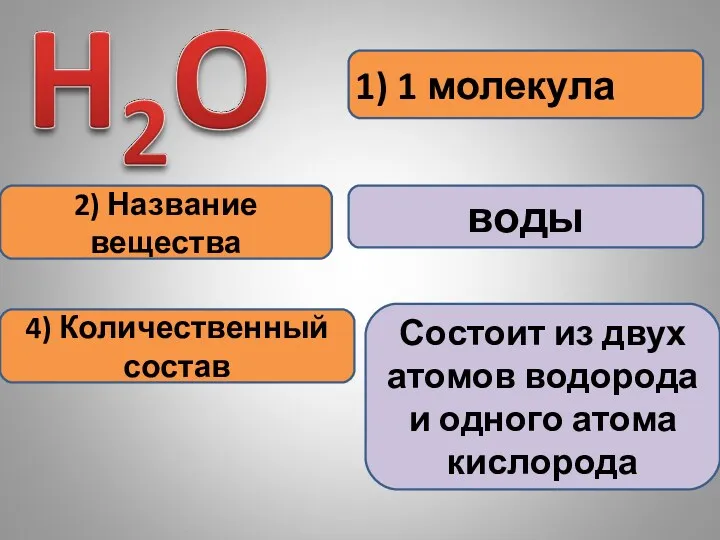
- 15. 1) 1 молекула 2) Название вещества воды 4) Количественный состав Состоит из двух атомов водорода и
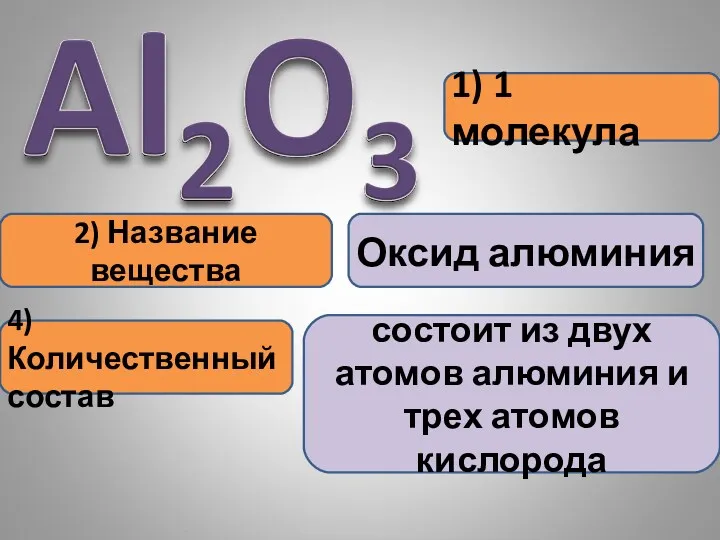
- 16. 1) 1 молекула 2) Название вещества Оксид алюминия 4) Количественный состав состоит из двух атомов алюминия
- 17. Информация, которую содержат химические формулы: 1) 1 молекула 2) Название вещества 3) Качественный состав 4) Количественный
- 18. Мr(Н2О)= Чтобы найти относительную молекулярную массу вещества, надо сложить относительные атомные массы элементов Аr(О)= 16 Аr(Н)=
- 19. Мr(СО2)=12 + 2*16= 44 Найдите относительную молекулярную массу углекислого газа
- 20. Найдите относительные молекуляр-ные массы следующих веществ: 1) кислорода О2 2) аммиака NH3 3) Оксида алюминия Аl2О3
- 21. Рассчитайте Мr (H2) = Mr (СаСl2) = Mr (CaCO3) = Мr (Ca(OH)2)= Mr (СН3СООН)= Мr (Ca3(PO4)2)=
- 23. Мы знаем, что вещества состоят из , а молекулы из молекул атомов. Чтобы атомы оставались вместе,
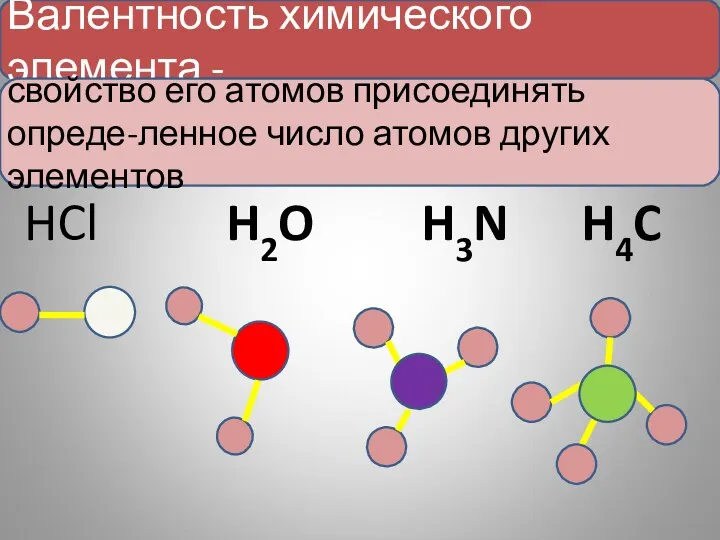
- 24. Валентность химического элемента - свойство его атомов присоединять опреде-ленное число атомов других элементов HCl H3N H2O
- 25. Как же можно узнать валентность элемента? Очень просто! Из таблицы Менделеева! Валентность элемента совпадает с номером
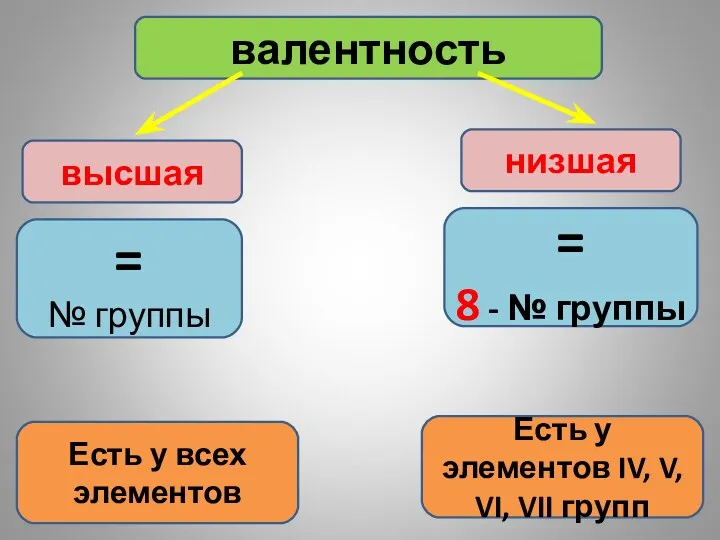
- 26. валентность = № группы высшая = 8 - № группы низшая Есть у всех элементов Есть
- 27. Как узнать, когда элемент обладает высшей валентностью, а когда низшей? Для этого вводят еще одно свойство
- 28. Договорились, что при составлении формул элемент с большей электро-отрицательностью надо записывать справа, а с меньшей -
- 29. 1.Рядом записываем знаки химических элементов. 2.Определяем валентность элементов: У элемента, который записан слева – она высшая
- 31. Скачать презентацию




















 Ртуть и цинк
Ртуть и цинк Драгоценные камни
Драгоценные камни Соли, их классификация и свойства
Соли, их классификация и свойства Степень окисления. Определение степени окисления в соединениях
Степень окисления. Определение степени окисления в соединениях Теория электролитической диссоциации
Теория электролитической диссоциации Химия и биологическая роль элементов VIIА-группы
Химия и биологическая роль элементов VIIА-группы Студенттің өзіндік жұмысы
Студенттің өзіндік жұмысы Составление уравнений химических реакций. Закон сохранения массы веществ
Составление уравнений химических реакций. Закон сохранения массы веществ Водород
Водород Соединения кальция. Жесткость воды и способы её устранения
Соединения кальция. Жесткость воды и способы её устранения Алкени (етиленові вуглеводні, олефіни)
Алкени (етиленові вуглеводні, олефіни) Коррозия металлов
Коррозия металлов Строение, свойства и применение алкенов
Строение, свойства и применение алкенов Дистилляция в химической промышленности
Дистилляция в химической промышленности Хлорид натрия (NaCI)
Хлорид натрия (NaCI) Кислород. Озон. Получение кислорода
Кислород. Озон. Получение кислорода Өндірілетін және тиелетін өнімнің сапасын бақылау, оларға қойылатын талаптар
Өндірілетін және тиелетін өнімнің сапасын бақылау, оларға қойылатын талаптар 20230802_stroenie_atoma_avtosohranennyy_2
20230802_stroenie_atoma_avtosohranennyy_2 Хімічні властивості алкенів
Хімічні властивості алкенів Биоразлагаемые ПАВ. Лекция 2
Биоразлагаемые ПАВ. Лекция 2 Принципы наноармирования волокнистых композитов
Принципы наноармирования волокнистых композитов Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Альдегиды и кетоны
Альдегиды и кетоны Искусственная и синтетическая резина
Искусственная и синтетическая резина Мұнай құрамындағы тұздың мөлшерін анықтау
Мұнай құрамындағы тұздың мөлшерін анықтау Неомыляемые липиды. Изопреноиды
Неомыляемые липиды. Изопреноиды Задачи на избыток-недостаток
Задачи на избыток-недостаток Синтетический каучук и его применение
Синтетический каучук и его применение