Содержание
- 2. Химическое соединение имеет постоянную химическую формулу! Н2О и Н2О2 Два разных вещества! Краткое повторение
- 3. Химическое соединение имеет постоянную химическую формулу! Химическая формула составляется по правилам валентности для молекулярных веществ. Н
- 4. Химическое соединение имеет постоянную химическую формулу! Химическая формула составляется по правилам валентности для молекулярных веществ Индексы
- 5. Химическое соединение имеет постоянную химическую формулу! Химическая формула составляется по правилам валентности для молекулярных веществ Индексы
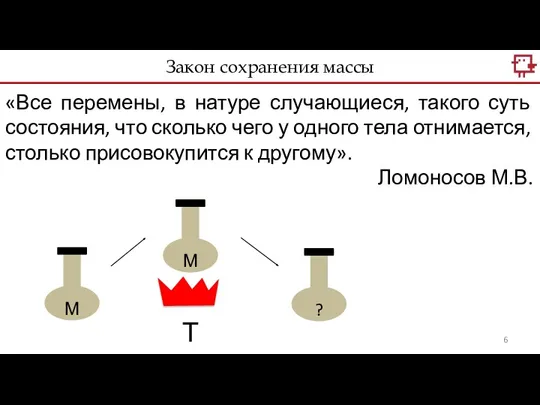
- 6. Закон сохранения массы «Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного
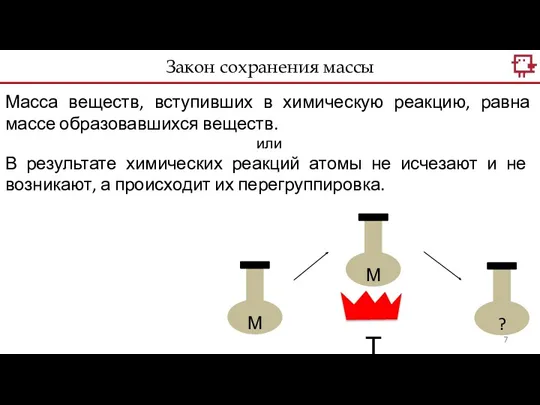
- 7. Закон сохранения массы Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ. или В результате
- 8. Закон сохранения массы Этот закон крайне важен, т.е. приняв такое положение можно проводить количественные расчеты. Задача.
- 9. Химическое уравнение Химическое уравнение – условная запись химической реакции посредством химических знаков и формул. Химическое уравнение
- 10. Химическое уравнение Для составления уравнения реакции нужно выполнить следующие шаги: В левой части уравнения пишут формулы
- 11. Химическое уравнение Для составления уравнения реакции нужно выполнить следующие шаги: В левой части уравнения пишут формулы
- 12. Химическое уравнение Для составления уравнения реакции нужно выполнить следующие шаги: В левой части уравнения пишут формулы
- 13. Химическое уравнение Существует ряд дополнительных значков: t – над стреловой или равно, означает нагревание – около
- 14. Эм…. А как понять, что получиться в результате реакции?!?!?!
- 15. Типы химических реакций Разложения Соединения Замещения Обмена Реакций разложения называется такая химическая реакция, в которой из
- 16. Типы химических реакций Разложения Соединения Замещения Обмена Реакций разложения называется такая химическая реакция, в которой из
- 17. Типы химических реакций Разложения Соединения Замещения Обмена Реакций разложения называется такая химическая реакция, в которой из
- 18. Типы химических реакций Разложения Соединения Замещения Обмена Реакций разложения называется такая химическая реакция, в которой из
- 19. Типы химических реакций Разложения Соединения Замещения Обмена Реакций разложения называется такая химическая реакция, в которой из
- 21. Скачать презентацию
















 Жиры
Жиры Хром и его соединения
Хром и его соединения Открытие Периодического закона
Открытие Периодического закона Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов
Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов Основные виды и понятия курса органической химии в старшей школе
Основные виды и понятия курса органической химии в старшей школе Химические свойства металлов
Химические свойства металлов Алкены. Химические свойства этилена
Алкены. Химические свойства этилена Кислородные соединения азота
Кислородные соединения азота Углеводородное топливо, его виды и назначения
Углеводородное топливо, его виды и назначения Відкриття та походження хімічних елементів
Відкриття та походження хімічних елементів Общая характеристика галогенов
Общая характеристика галогенов Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Классы неорганических веществ. Лекция №4
Классы неорганических веществ. Лекция №4 Неметаллы. Особенности строения атомов неметаллов
Неметаллы. Особенности строения атомов неметаллов Алкани. Ізомерія та номенклатура алканів
Алкани. Ізомерія та номенклатура алканів Окислительно – восстановительные реакции
Окислительно – восстановительные реакции Глицерин. Свойства и применение
Глицерин. Свойства и применение КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ
КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ Методы количественного определения. Химические методы анализа
Методы количественного определения. Химические методы анализа Элементы VII группы периодической таблицы Д.И. Менделеева
Элементы VII группы периодической таблицы Д.И. Менделеева Redox Reactions
Redox Reactions Термический анализ
Термический анализ Растворы электролитов. Ионизация воды и шкала рН
Растворы электролитов. Ионизация воды и шкала рН Колдовство волшебницы ОВ: окислительные или восстановительные превращения
Колдовство волшебницы ОВ: окислительные или восстановительные превращения Мотивирующие цитаты великих людей
Мотивирующие цитаты великих людей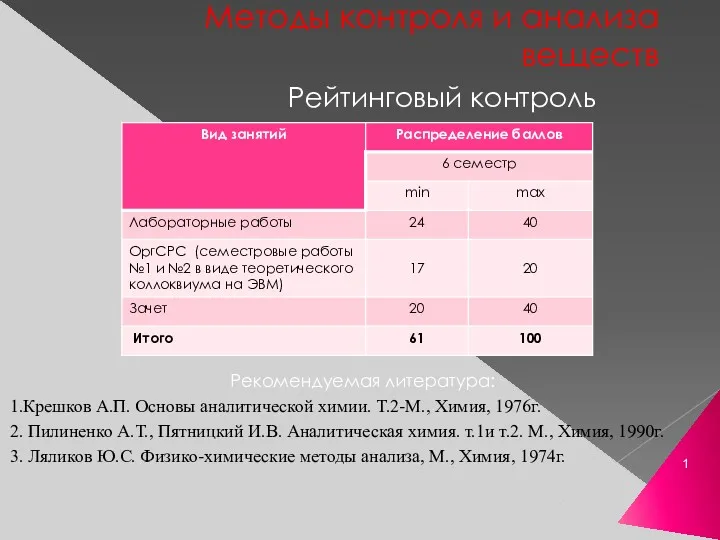 Методы контроля и анализа веществ
Методы контроля и анализа веществ Карбоновые кислоты
Карбоновые кислоты Анализ лекарственных форм
Анализ лекарственных форм