Содержание
- 2. Задание 1. Выпишите из предложенного перечня формул веществ только формулы кислот. На отметку «4» и «
- 4. Na2CO3 Cu(OH)2 FeO AlCl3 MgBr2 NaOH CO2 NiO Ca(OH)2 HCl H2SO4 H2SiO3
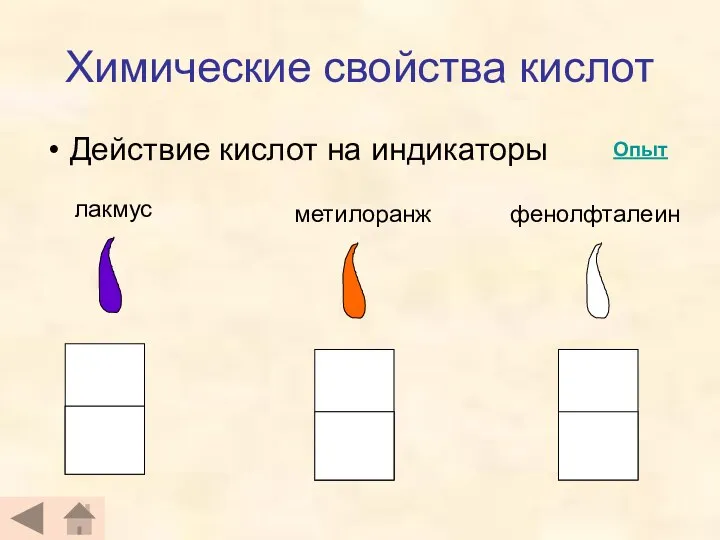
- 5. Химические свойства кислот Действие кислот на индикаторы лакмус метилоранж фенолфталеин Опыт
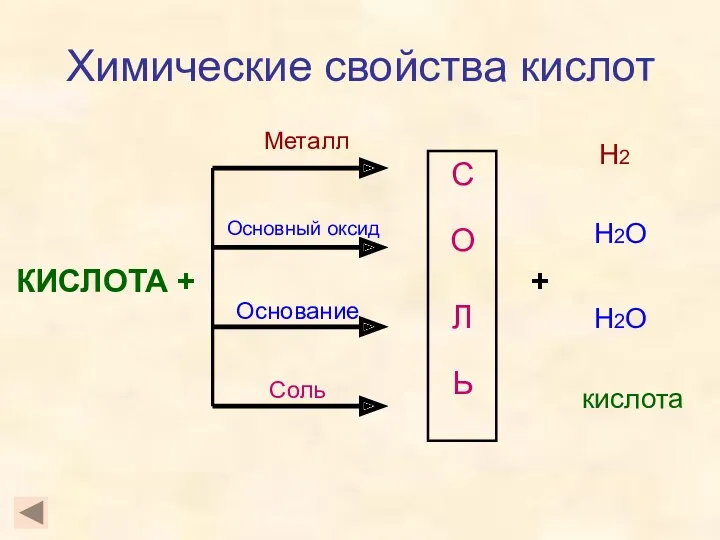
- 6. Химические свойства кислот КИСЛОТА + С О Л Ь Металл Основный оксид Основание Соль + Н2
- 7. Химические свойства кислот Кислота + металл = соль + водород Ряд активности металлов: Li K Ba
- 8. Химические свойства кислот Кислота + основный оксид = соль + вода
- 9. Кислота + основание = соль + вода Химические свойства кислот Реакция нейтрализации – это реакция обмена
- 10. Химические свойства кислот Кислота 1 + соль 1 = соль 2 + Кислота 2 Условия реакции:
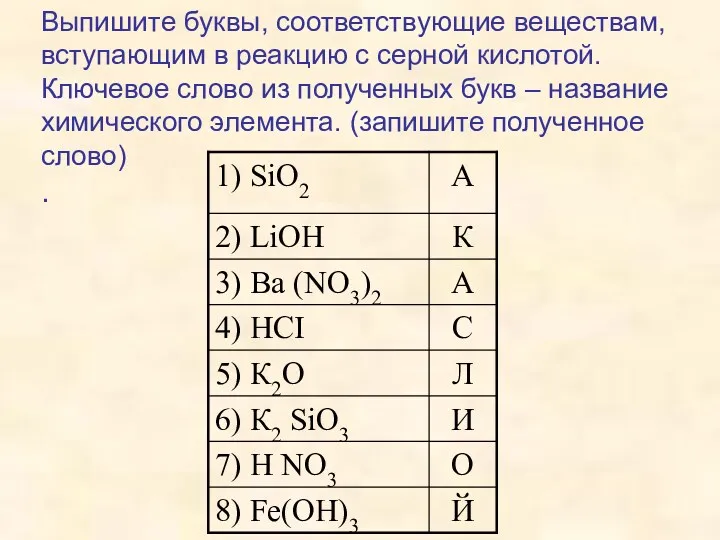
- 11. Выпишите буквы, соответствующие веществам, вступающим в реакцию с серной кислотой. Ключевое слово из полученных букв –
- 12. Составьте 1 возможное уравнение в ионном виде для реакции взаимодействия перечисленных веществ с раствором серной кислоты
- 14. Скачать презентацию






 Генетическая связь между классами органических веществ
Генетическая связь между классами органических веществ Біріншілік алкилсульфаттар және алкилэтоксисульфаттар немесе біріншілік спирттегі сульфоэфирдің тұздары. 4 Лекция
Біріншілік алкилсульфаттар және алкилэтоксисульфаттар немесе біріншілік спирттегі сульфоэфирдің тұздары. 4 Лекция Технологии повышения конструкционной прочности сталей
Технологии повышения конструкционной прочности сталей Приготовление растворов с определенной массовой долей растворенного вещества. Практическая работа
Приготовление растворов с определенной массовой долей растворенного вещества. Практическая работа Алюминий. Строение и свойство атомов
Алюминий. Строение и свойство атомов Типы химических соединений, номенклатура, свойства
Типы химических соединений, номенклатура, свойства Основные классы неорганических соединений
Основные классы неорганических соединений Химическая взрывчатка
Химическая взрывчатка Практична робота 3 Самедова Софія (1)
Практична робота 3 Самедова Софія (1) Карбоновые кислоты. Строение
Карбоновые кислоты. Строение Кафедра химической технологии лекарственных веществ (ХТЛВ)
Кафедра химической технологии лекарственных веществ (ХТЛВ) Метод нейтрализации. Расчёты в методе нейтрализации. Ионное произведение воды. Понятие Рн
Метод нейтрализации. Расчёты в методе нейтрализации. Ионное произведение воды. Понятие Рн Основные классы химических соединений
Основные классы химических соединений Алкены. Этилен, его получение
Алкены. Этилен, его получение Хлороводород, соляная кислота. Химические свойства соляной кислоты
Хлороводород, соляная кислота. Химические свойства соляной кислоты Бензол
Бензол Теория диаграмм состояния
Теория диаграмм состояния Одноосновные карбоновые кислоты. Строение, физические свойства, номенклатура
Одноосновные карбоновые кислоты. Строение, физические свойства, номенклатура Состав и свойства чая
Состав и свойства чая Теория растворов. Растворы электролитов
Теория растворов. Растворы электролитов Степень окисления
Степень окисления Залежність фізичних властивостей речовин від типу кристалічних ґраток
Залежність фізичних властивостей речовин від типу кристалічних ґраток Nucleic acids
Nucleic acids Самородные элементы
Самородные элементы Решение расчетных задач по уравнениям реакций
Решение расчетных задач по уравнениям реакций Круговорот воды в природе
Круговорот воды в природе Энергетика химических реакций
Энергетика химических реакций Щелочные АКБ
Щелочные АКБ