Слайд 2

По физическим свойствам соляная кислота – бесцветный газ с резким запахом,
который тяжелее воздуха. Химическая связь – ковалентная полярная.
Хорошо растворим в воде.
Соляная кислота = хлороводородная кислота. Эта кислота одноосновная.
Слайд 3

В разбавленном растворе легко диссоциирует.
HCl=H++Cl-
Слайд 4

Главная характеристика для кислот – окраска индикатора: лакмус станет красным, метилоранж
– розовым, фенолфталеин – бесцветным, индикаторная бумага – красный.
Слайд 5

1)Соляная кислота взаимодействует с металлами, которые стоят в ряду активности до
водорода. В этих реакциях водород выступает окислителем.
2HCl+Mg=MgCl2+H2
2)Соляная кислота реагирует с оксидами металлов:
2HCl+MgO=MgCl2+H2O
2H++MgO=Mg2++H2O
3)Соляная кислота реагирует со щелочами и нерастворимыми основаниями, где будет образовываться соль+вода. Такая реакциях называется реакцией нейтрализации.
HCl+KOH=KCl+H2O
H++OH-=H2O
4) Соляная кислота реагирует с солями. НО есть условие: осадок, газ или вода.
K2CO3+2HCl=2KCl+H2O+CO2
2H++CO32-=H2O+CO2
Слайд 6

ЗАДАЧИ НА ИЗБЫТОК/
НЕДОСТАТОК
Слайд 7

Пример: Произошла реакция между соляной кислотой массой 23,5 г и гидроксидом
бария массой 54,25 г. Найти массу образовавшейся соли.
2HCl+Ba(OH)2=BaCl2+2H2O
Зная массу, можно найти химической количество веществ.
n(HCl)= 23,5/36,5=0,6438 моль
n(Ba(OH)2)=54,25/171=0,317 моль
Сравним химическое количество:
0,6438 0,317 х
2HCl+Ba(OH)2=BaCl2+2H2O
2 1 1
0,6438 и 0,317
2 1
0,3219 и 0,317
избыток недостаток
Решаем по недостатку:
0,317 = х
1 1
х=0,317 моль
n(BaCl2)=0,317 моль
M(BaCl2)=208 г/моль
m(BaCl2)=n*M=0,317*208=65,936 г
Ответ: 65,936 г.
Слайд 8

Сборник задач 9 класс: №264, №265.
Задачи:
1. На 47 г оксида
калия подействовали раствором, содержащим 40 г соляной кислоты. Найдите массу образовавшегося хлорида калия.
2. На 24 г металлического магния подействовали 100 г 30%-го раствора соляной кислоты. Найдите массу образовавшегося хлорида магния.
3. На 36 г алюминия подействовали 64 г соляной кислотой. Найдите массу образовавшейся соли.
4. На раствор, содержащий 53 г карбоната натрия, подействовали раствором, содержащим 49 г соляной кислоты. Найдите массу образовавшейся соли.







 Гетероциклдық қосылыстардың туындылары
Гетероциклдық қосылыстардың туындылары Классы неорганических соединений. 8 класс
Классы неорганических соединений. 8 класс Figure
Figure Методы выращивания монокристаллов кремния. Сравнение. Сферы применения монокристаллов, выращенных различными методами
Методы выращивания монокристаллов кремния. Сравнение. Сферы применения монокристаллов, выращенных различными методами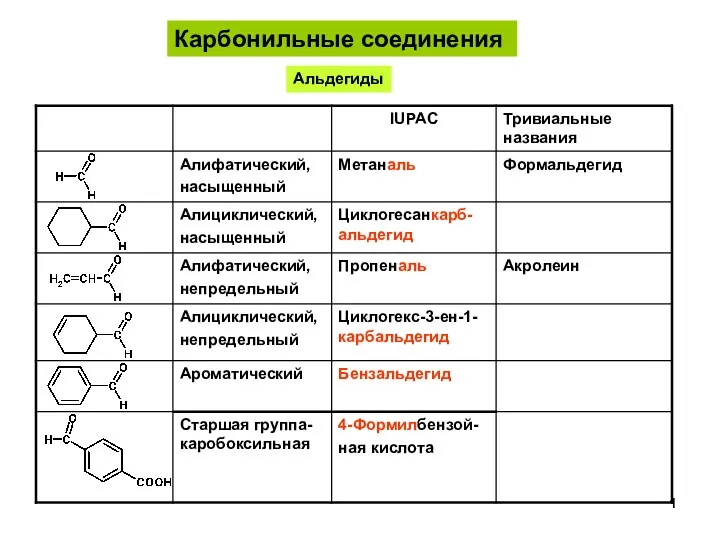 АльдегидыКетоны-1
АльдегидыКетоны-1 Серная кислота и её свойства
Серная кислота и её свойства Жиры. Сложные эфиры глицерина и высших карбоновых кислот
Жиры. Сложные эфиры глицерина и высших карбоновых кислот Типы химических реакций
Типы химических реакций Соли. CaSO4 - Сульфат кальция
Соли. CaSO4 - Сульфат кальция Каменный уголь
Каменный уголь Механизмы органических реакций
Механизмы органических реакций ПОЛИСАХАРИДЫ
ПОЛИСАХАРИДЫ Химическая посуда и ее назначение (4)
Химическая посуда и ее назначение (4) Обобщающий урок по теме: Металлы
Обобщающий урок по теме: Металлы Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Кристаллические решетки
Кристаллические решетки Химия нефти и газа. Свойства нефти и нефтепродуктов. Свойства газов
Химия нефти и газа. Свойства нефти и нефтепродуктов. Свойства газов D-элементы VII-В группы. Марганец
D-элементы VII-В группы. Марганец Гидродинамические свойства полимеров. Полиэлектролиты
Гидродинамические свойства полимеров. Полиэлектролиты Изомеры – это вещества, имеющие одинаковый состав
Изомеры – это вещества, имеющие одинаковый состав Классы неорганических веществ
Классы неорганических веществ Залізо. Фізичні та хімічні властивості
Залізо. Фізичні та хімічні властивості Электрофильное замещение в ароматических соединениях, SE
Электрофильное замещение в ароматических соединениях, SE Вещества и физические тела
Вещества и физические тела Сложные эфиры
Сложные эфиры Тірі ағзада жүретін процесстер – физика-химиялық интерпретация
Тірі ағзада жүретін процесстер – физика-химиялық интерпретация Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды