Содержание
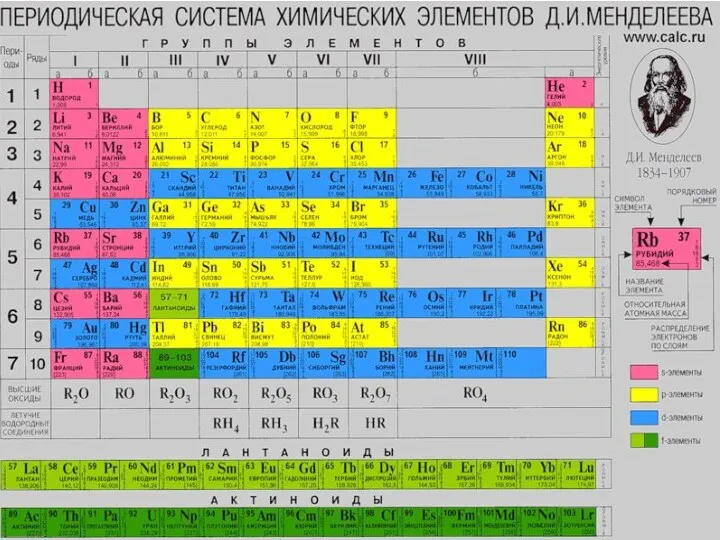
- 3. Элементы VIIВ группы
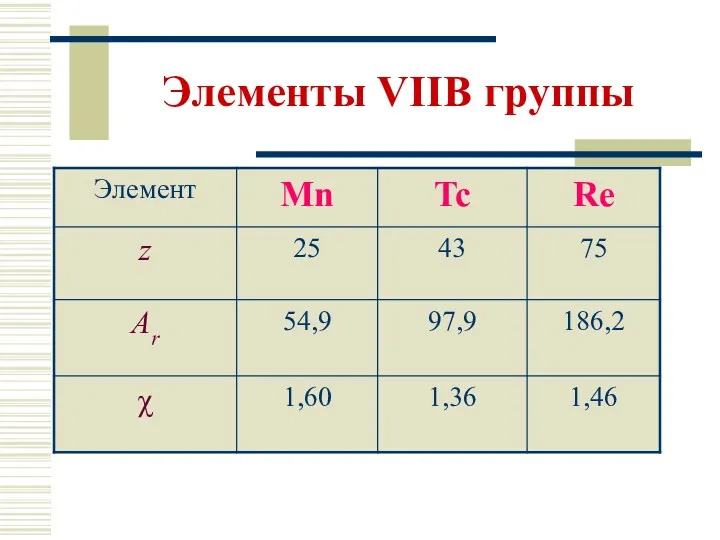
- 4. Элементы VIIВ группы Общая электронная формула: […] ns2 (n–1)d5 Степени окисления: +II ÷ +VII КЧ 4,
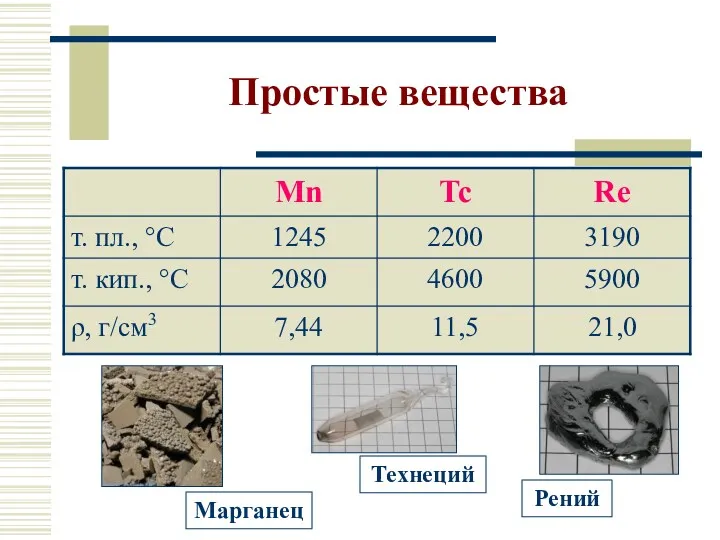
- 5. Простые вещества
- 6. В ЭХРН: … Mn …H ... Re …Tc Mn2+/Mn ReO4–/Re TcO4–/Tc ϕ°, В: –1,19 +0,37 +0,47
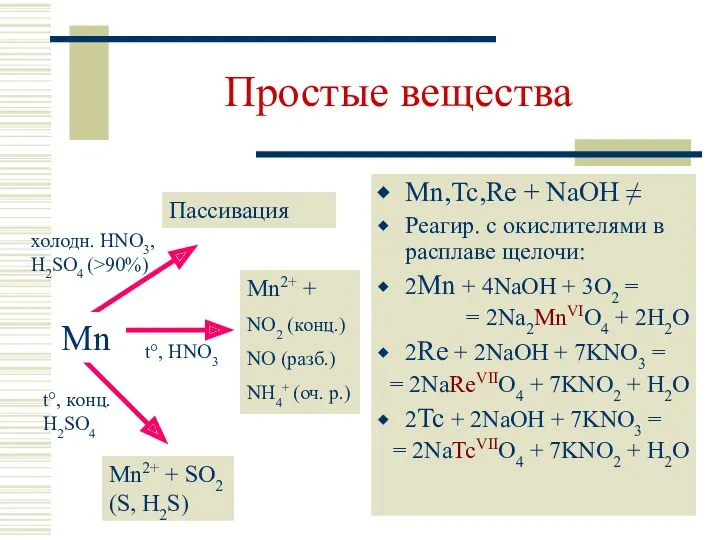
- 7. Простые вещества Mn,Tc,Re + NaOH ≠ Реагир. с окислителями в расплаве щелочи: 2Mn + 4NaOH +
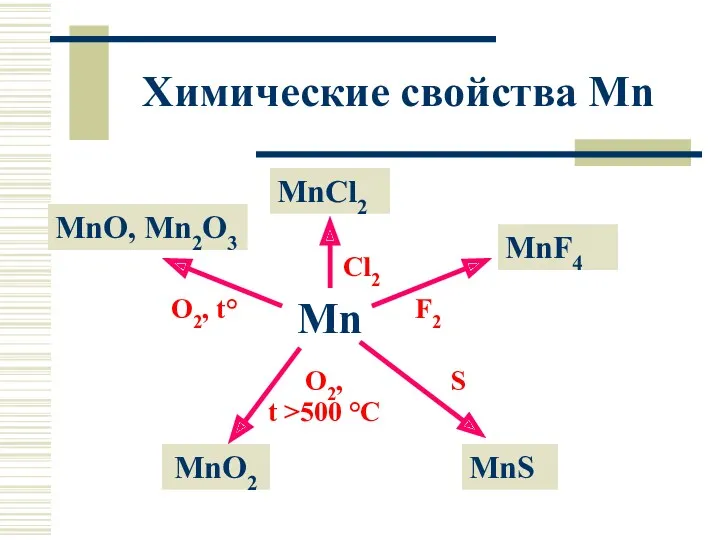
- 8. Химические свойства Mn Mn MnCl2 MnO, Mn2O3 MnF4 MnO2 MnS
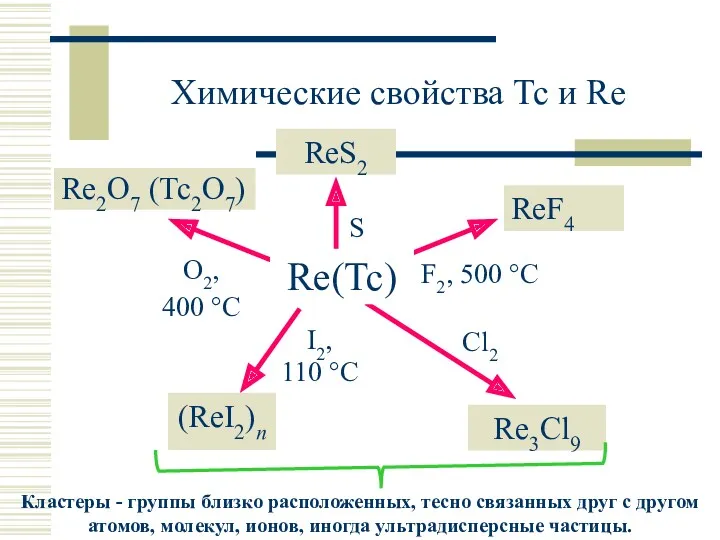
- 9. Химические свойства Tc и Re ReS2 Re2O7 (Tc2O7) ReF4 (ReI2)n Re3Cl9 Re(Tc)
- 10. Строение [Re3Cl9]
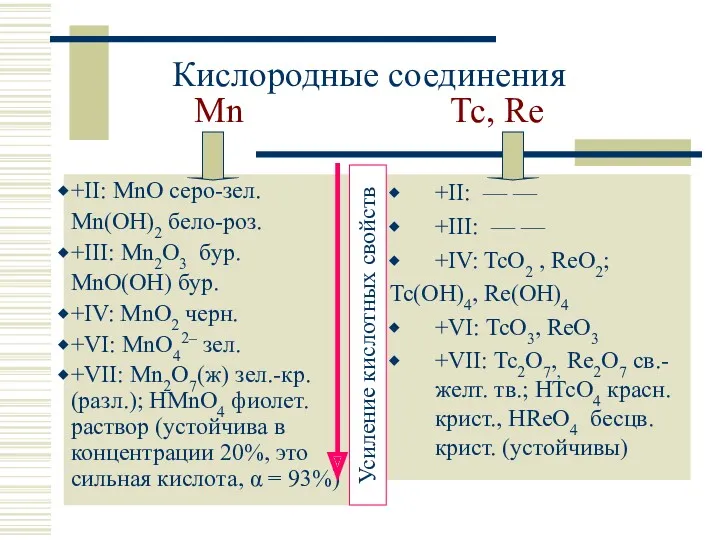
- 11. Кислородные соединения Mn Tc, Re +II: MnO серо-зел. Mn(OH)2 бело-роз. +III: Mn2O3 бур. MnO(OH) бур. +IV:
- 12. Распространение в природе и важнейшие минералы 14. Mn 0,085 % масс. 81. Re – редкий рассеянный
- 13. Минералы марганца Пиролюзит MnO2 Гаусманит (MnIIMn2III)O4 Манганит MnO(OH) Родохрозит MnCO3 Гюбнерит MnWO4 Вольфрамит (Mn, Fe)WO4 Псиломелан
- 14. Получение металлов Mn: а) электролиз раствора MnSO4 б) MnO2 + Si = Mn + SiO2 3MnO2
- 15. Марганец Активный металл. Устойч. ст.ок. +II (в кисл. среде) и +IV. В ст.ок. +II похож на
- 16. Марганец(II) MnO1÷1,13 – нестехиом. (изб. O–II, до 6,5% ат. Mn в крист. реш. имеют ст.ок.+III); полупроводник.
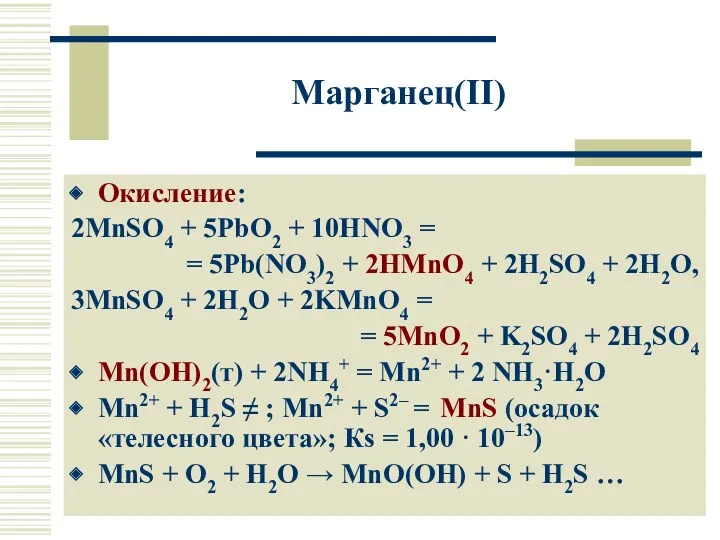
- 17. Марганец(II) Окисление: 2MnSO4 + 5PbO2 + 10HNO3 = = 5Pb(NO3)2 + 2HMnO4 + 2H2SO4 + 2H2O,
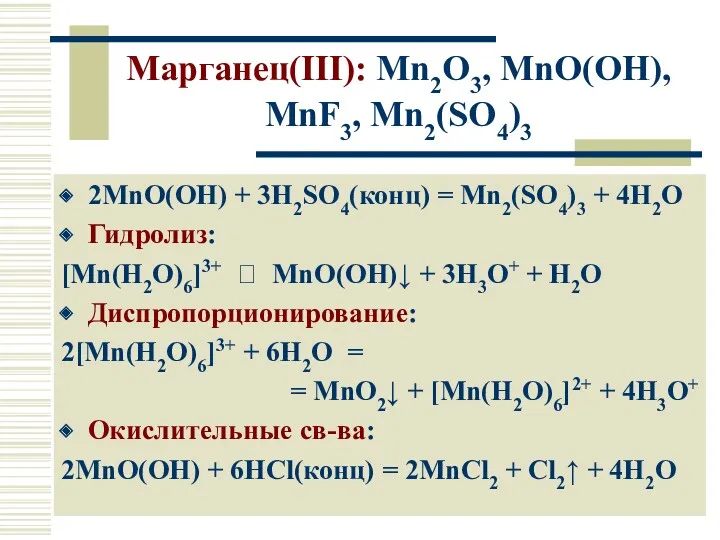
- 18. Марганец(III): Mn2O3, MnO(OH), MnF3, Mn2(SO4)3 2MnO(OH) + 3H2SO4(конц) = Mn2(SO4)3 + 4H2O Гидролиз: [Mn(H2O)6]3+ ⮀ MnO(OH)↓
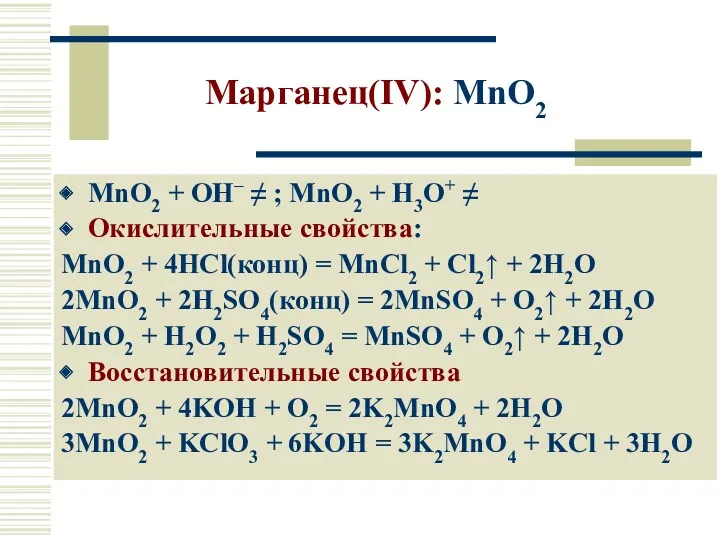
- 19. Марганец(IV): MnO2 MnO2 + OH– ≠ ; MnO2 + H3O+ ≠ Окислительные свойства: MnO2 + 4HCl(конц)
- 20. Марганец(IV): MnO2 Получение MnO2 : 3MnCO3 + KClO3 = 3MnO2 + KCl + 3CO2↑ MnO2 –
- 21. Марганец(VI) В сильнощел. среде уст. соли, напр. K2MnO4. В растворе – диспропорционирует: 3MnO42− + 2H2O =
- 22. Марганец(VII) Mn2O7 – маслянистая жидк. Получение (видео): 2KMnO4 + 2H2SO4 = = Mn2O7 + 2KHSO4 +
- 23. Окислительные свойства рН MnO4– + 8H+ + 5e– = Mn2+ + 4H2O; Е° = +1,53 B
- 25. Скачать презентацию
![Элементы VIIВ группы Общая электронная формула: […] ns2 (n–1)d5 Степени](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/217319/slide-3.jpg)

![Строение [Re3Cl9]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/217319/slide-9.jpg)









 Классификация органических соединений
Классификация органических соединений Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Химическая технология органических веществ
Химическая технология органических веществ Цікаві історичні факти з походження назв хімічних елементів
Цікаві історичні факти з походження назв хімічних елементів Хімічні властивості карбонових кислот
Хімічні властивості карбонових кислот Серная кислота и её свойства
Серная кислота и её свойства Хімія в житті людини
Хімія в житті людини Органические высокомолекулярные реагенты
Органические высокомолекулярные реагенты Геохимия ландшафтов
Геохимия ландшафтов Коррозия металлов
Коррозия металлов Пластмаси, синтетичні каучуки, гума, штучні й синтетичні
Пластмаси, синтетичні каучуки, гума, штучні й синтетичні Why use plastics
Why use plastics Физические явления – основа разделения смесей в химии (урок химии в 8 классе)
Физические явления – основа разделения смесей в химии (урок химии в 8 классе) Фізичні властивості та хімічний склад природних вод
Фізичні властивості та хімічний склад природних вод Тренинг. Практическая химия (8-9 классы)
Тренинг. Практическая химия (8-9 классы) Происхождение, состав и свойства минералов
Происхождение, состав и свойства минералов Степень окисления – Условный заряд атомов химического элемента в соединении
Степень окисления – Условный заряд атомов химического элемента в соединении Взрывчатые вещества. Пероксид ацетона и пикриновая кислота
Взрывчатые вещества. Пероксид ацетона и пикриновая кислота Гидроксид аммония
Гидроксид аммония Титриметрический анализ. (Лекция 22)
Титриметрический анализ. (Лекция 22) Типы химических реакций
Типы химических реакций Псевдоморфозы. Образование псевдоморфоз
Псевдоморфозы. Образование псевдоморфоз Строение электронных оболочек атомов химических элементов
Строение электронных оболочек атомов химических элементов Конструкционные и функциональные волокнистые композиты
Конструкционные и функциональные волокнистые композиты Общая характеристика металлов главных подгрупп I-III групп ПСХЭ Д.И. Менделеева
Общая характеристика металлов главных подгрупп I-III групп ПСХЭ Д.И. Менделеева Подготовка к ГИА. А2. Периодический закон и Периодическая система химических элементов Д.И. Менделеева
Подготовка к ГИА. А2. Периодический закон и Периодическая система химических элементов Д.И. Менделеева Основные положения ТЭД
Основные положения ТЭД Золь-гель технология. Прорыв XXI века
Золь-гель технология. Прорыв XXI века