Содержание
- 2. Репетиторский центр «РадиусК» – ради успешной карьеры! Внимание! Практические задания по типу «ОГЭ»
- 3. Репетиторский центр «РадиусК» – ради успешной карьеры! Внимание! Практические задания по типу «ОГЭ»
- 4. Репетиторский центр «РадиусК» – ради успешной карьеры! Для того, чтобы решить задания Вспомним качественные реакции на
- 5. Репетиторский центр «РадиусК» – ради успешной карьеры! 1. Качественные реакции Качественные реакции – это реакции, позволяющие
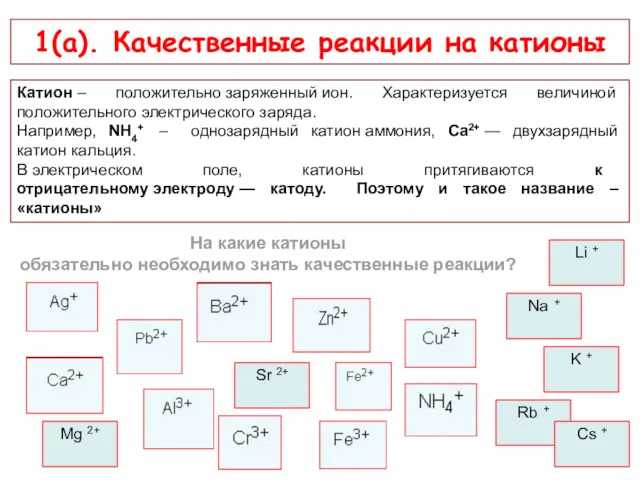
- 6. Репетиторский центр «РадиусК» – ради успешной карьеры! 1(а). Качественные реакции на катионы Катион – положительно заряженный
- 7. Репетиторский центр «РадиусК» – ради успешной карьеры! Катионы металлов IА группы Na + K + Rb
- 8. Репетиторский центр «РадиусК» – ради успешной карьеры! Катион аммония NH4+, катион Н+ H + Внимание! Индикаторы!
- 9. Репетиторский центр «РадиусК» – ради успешной карьеры! Катионы металлов IIА группы Mg 2+ Sr 2+ Ba
- 10. Репетиторский центр «РадиусК» – ради успешной карьеры! Элементы-металлы, соединения которых проявляют амфотерные свойства Можно записать Na[Al(OH)4]
- 11. Репетиторский центр «РадиусК» – ради успешной карьеры! Другие катионы (d-элементы) https://www.youtube.com/watch?v=YJJHouSU8uw CuCl2 + 2NaОН = Cu(ОН)2
- 12. Репетиторский центр «РадиусК» – ради успешной карьеры! Другие катионы (d-элементы) https://www.youtube.com/watch?v=hLBSwoHS23s https://www.youtube.com/watch?v=t3uV5O3Sar4 https://www.youtube.com/watch?v=2_NbvHE-zuI Чудо-опыт с роданидом!
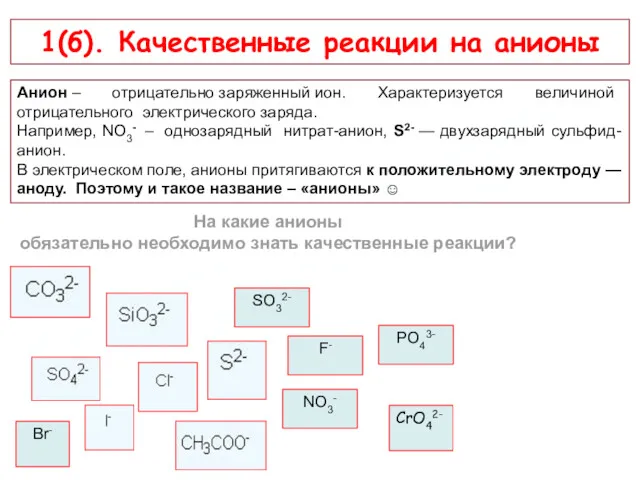
- 13. Репетиторский центр «РадиусК» – ради успешной карьеры! 1(б). Качественные реакции на анионы Анион – отрицательно заряженный
- 14. Качественные реакции на галогены (Cl-, Br-, I-) + F- Br- F- NaCl + AgNO3 = AgCl
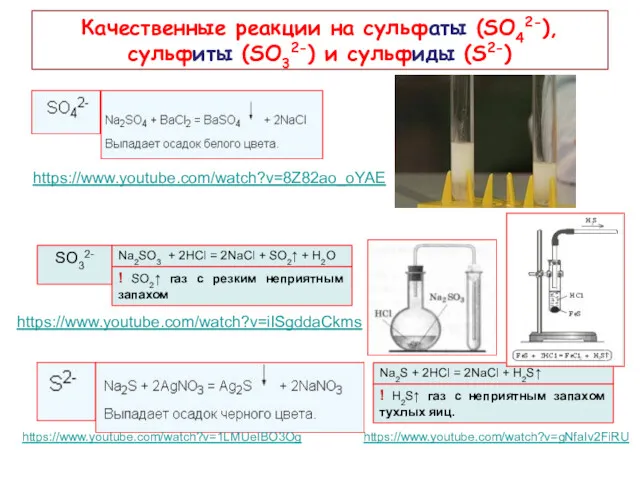
- 15. Качественные реакции на сульфаты (SО42-), сульфиты (SО32-) и сульфиды (S2-) SO32- Na2SO3 + 2HCl = 2NaCl
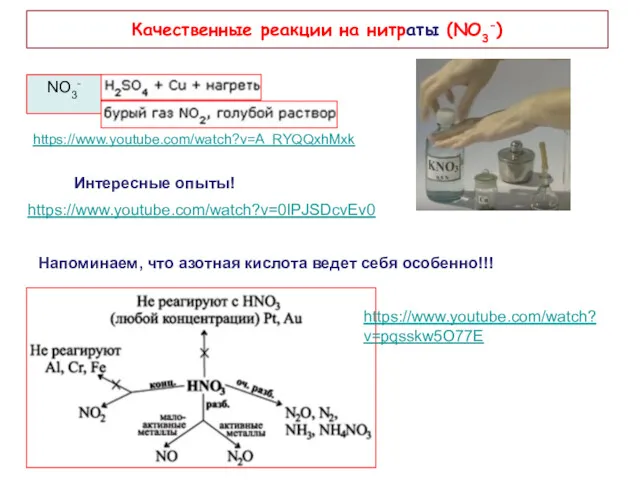
- 16. Качественные реакции на нитраты (NO3-) NO3- https://www.youtube.com/watch?v=A_RYQQxhMxk https://www.youtube.com/watch?v=0IPJSDcvEv0 Интересные опыты! Напоминаем, что азотная кислота ведет себя
- 17. Качественные реакции на карбонаты (CО32-) и силикаты (SiО32-) Na2SiO3 + 2HCl = H2SiO3 ↓+ 2NaCl !
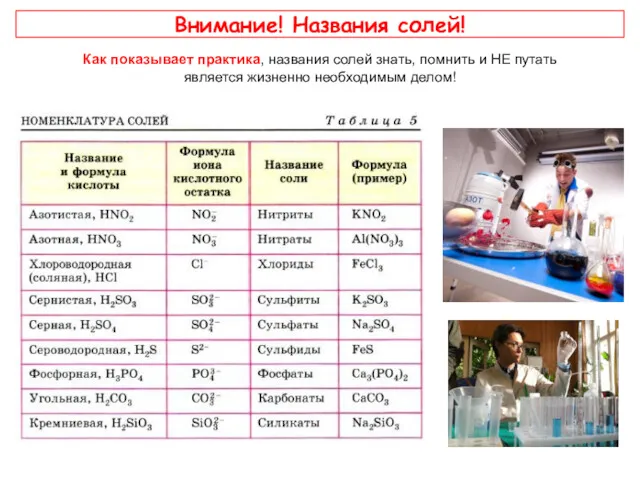
- 18. Внимание! Названия солей! Как показывает практика, названия солей знать, помнить и НЕ путать является жизненно необходимым
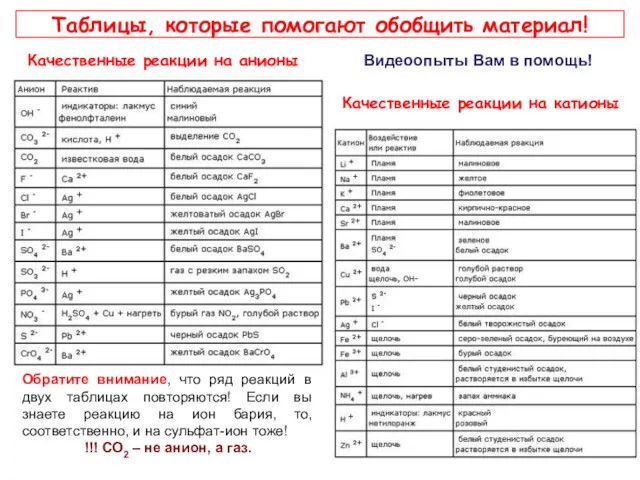
- 19. Таблицы, которые помогают обобщить материал! Качественные реакции на анионы Качественные реакции на катионы Обратите внимание, что
- 20. В данном случае приводятся сокращенные ионные уравнения, которые иллюстрируют суть процесса, т.е. показывают какие ионы «связываются»!
- 21. Репетиторский центр «РадиусК» – ради успешной карьеры! Спасибо за внимание! Материал тренировочной презентации НЕ является исчерпывающим!
- 22. Источники (изображения) Изображение «Хлорид серебра» data:image/jpeg;base64,/R06j3Kkzn0L0LYNp7D1peLJ9Wn6Kl9kZ Изображение «Иодид свинца» http://ege-study.ru/wp-content/uploads/2015/11/Chemistry_color_13.jpg Изображение «Осадок гидроксида меди (II)» http://chemistry-chemists.com/N1_2015/P11/copper_II_hydroxide-48.jpg
- 24. Скачать презентацию















 Железо. Fe (лат. Феррум)
Железо. Fe (лат. Феррум) Узагальнення й систематизація знань з теми Початкові хімічні поняття
Узагальнення й систематизація знань з теми Початкові хімічні поняття Аминокислоты. Пептиды. Хроматографические методы исследования
Аминокислоты. Пептиды. Хроматографические методы исследования Химическая связь
Химическая связь Розв'язування задач за рівнянням хімічних реакцій
Розв'язування задач за рівнянням хімічних реакцій NaHSO4. Гидросульфат натрия
NaHSO4. Гидросульфат натрия Молекулярно-массовые характеристики высокомолекулярных соединений
Молекулярно-массовые характеристики высокомолекулярных соединений Общие проблемы определения низких концентраций
Общие проблемы определения низких концентраций Ионные уравнения
Ионные уравнения Реакции ионного обмена
Реакции ионного обмена Установка производства олефинов для синтеза линейных алкилбензолов
Установка производства олефинов для синтеза линейных алкилбензолов Практикум по органической и биоорганической химии
Практикум по органической и биоорганической химии Строение вещества. Химические элементы
Строение вещества. Химические элементы Применение солей
Применение солей Обзор электродных процессов
Обзор электродных процессов Спроби класифікації хімічних елементів
Спроби класифікації хімічних елементів Металловедение. Классификация металлов
Металловедение. Классификация металлов Физико-химические методы в анализе ЛВ. Метод ионометрии в анализе ЛВ. Определение спирта в фармацевтических препаратах
Физико-химические методы в анализе ЛВ. Метод ионометрии в анализе ЛВ. Определение спирта в фармацевтических препаратах Окислительновосстановительное титрование
Окислительновосстановительное титрование Активационный анализ
Активационный анализ Твердотільний ямр
Твердотільний ямр Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение
Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение Наноматериалы. Свойства наноматериалов. Особенности свойств
Наноматериалы. Свойства наноматериалов. Особенности свойств Карбоновые кислоты
Карбоновые кислоты Значение периодического закона и периодической системы Д.И. Менделеева
Значение периодического закона и периодической системы Д.И. Менделеева Способы получения металлов
Способы получения металлов Химическая связь
Химическая связь Закон сохранения массы вещества. Химические уравнения
Закон сохранения массы вещества. Химические уравнения